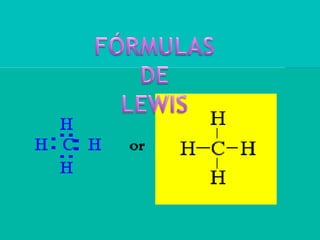
FÓRMULAS DE LEWIS: CONCEPTOS BÁSICOS DE ENLACES IÓNICOS Y COVALENTES
- 1. FÓRMULAS DE LEWIS
- 2. CONCEPTOS BÁSICOS ELECTRONES DE VALENCIA Electrones de un átomo en suúltimonivel de energía (de mayor energía). El grupo del elemento en la tablaperiódica, nos dice la valencia de uno de susátomos. REGLA DEL OCTETO Un átomotiende a formar enlaces hastaque se rodea de 8 electrones de valencia. Se forma un enlace covalente entre dos átomos, cuando no hay suficientes e paraquecadaátomo complete suoctetoindividualmente.
- 3. GASES NOBLES G. VIII Ultimo nivelcompleto: Ocho (8) electrones de valencia en suúltimonivel (Excepto el He) Configuraciónelectrónicamásestable, pocoreactivos, bajaenergía. ESTADO IDEAL DE UN ÁTOMO!
- 5. COVALENTE
- 6. METÁLICO
- 8. ENLACE IÓNICO Los electrones son transferidos de un átomo a otro, resultando en la formación de dos especies iónicas: cationes y aniones. Las atracciones electrostáticas entre los iones negativos (aniones) e iones positivos (cationes) mantienen unido el compuesto. “Los opuestos se atraen” Cl- Na+
- 9. ENLACE IÓNICO Se da entre elementos con baja E de ionización y alta afinidad electrónica. Entre elementos de los Grupos IA o IIA y los del Grupo VIIA u Oxígeno ppalmente.
- 10. ENLACE IÓNICO Realice la configuración electrónica para cada pareja de átomos y deduzca el compuesto que forman, según los electrones que requieran dar o recibir para completar el octeto: Na y Cl Mg y O Ca y Cl K y O
- 11. MANERA DE ESCRIBIR FÓRMULAS DE LEWIS Elija un esqueletorazonable (simétrico) para la molécula o ión, así: Elemento central: el menos electronegativo. Los átomos de O no se enlazan entre sí. Si hay más de un átomo central, se emplea el esqueleto más simétrico posible. C2H4, P2O7 2. Se calcula N: total de e de valencia que requieren todos los átomos. 3. Se calcula A: número de e disponibles en las capas de valencia de todos los átomos. 4. Se calcula S: número total de e compartidos y se colocan en el esqueleto con puntos o guiones. 5. Se colocan los e adicionales como pares no compartidos.
- 12. LIMITACIONES DE LA REGLA DEL OCTETO PARA LAS FÓRMULAS DE LEWIS El Hidrógeno: tiene 1 e de valencia, requiere 2 El Berilio: tiene 2 e de valencia, requiere 4. El Boro: tiene 3 e de valencia, requiere 6. Compuestos con número impar de e, NO, NO2 Cuando el átomo central comparte más de 8 electrones, se añaden dos reglas: a) Si S es menor que el número de e necesarios para enlazar todos los átomos, S se incrementa.
- 13. ejercicios Escriba las estructuras de Lewis para las siguientes moléculas e iones: NCl3 CH3COOH NF3 HNO3 CO3(-2)
- 14. CIBERGRAFIA http://www.chemguide.co.uk/atoms/bondingmenu.html#top http://www.ndt-ed.org/EducationResources/CommunityCollege/Materials/Structure/bonds.htm CHANG, R. QUÍMICA. 10ª edición. Mc Graw Hill. México, 2010.