Hemija - Karboksilne kiseline - Aneta Kostić
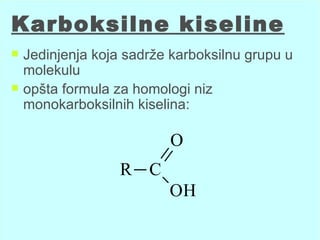
- 1. Karboksilne kiseline Jedinjenja koja sadrže karboksilnu grupu u molekulu opšta formula za homologi niz monokarboksilnih kiselina: O R C OH
- 2. Nomenklatura Trivijalna imena Nazivaju se još i masne kiseline, jer su prvi put izolovane iz prirodnih izvora, naročito hidrolizom masti i voskova Davana su im imena koja su označavala mesto njihovog nalaženja (mravlja, sirćetna, buterna, itd.) IUPAC imena za kiseline iznad C10 sa neparnim brojem C-atoma daju se radije nego uobičajena imena. Razlog: samo su kiseline sa parnim brojem C-atoma nađene u mastima, a sa neparnim brojem su dobivane sintezom. Ime margarinska kiselina (C27) izgleda predstavlja jedini izuzetak. Kao i kod ostalih homologih serija, ona jedinjenja koja imaju izopropil grupu na kraju normalnog ugljovodoničnog niza mogu dobiti prefiks izo na uobičajeno ime; na pr. (CH3)2CHCOOH - izobuterna kiselina
- 3. Nomenklatura (nastavak) Kao derivati normalnih kiselina Kao osnovna supstanca se uzima CH3COOH, a jedinjenja se nazivaju kao derivati kod kojih su H-atomi CH3-grupe u CH3COOH zamenjeni drugim grupama 5 4 3 2 1 δ γ β α CH3 CH2 CH CH COOH CH3 CH3 metil-sek-butilsirćetna kiselina
- 4. Nomenklatura (nastavak) IUPAC sistem Uzima se ime zasićenog ugljovodonika koji ima isti broj C-atoma kao i najduži niz koji sadrži karboksilnu grupu, pa se njemu doda nastavak -ska kiselina. Primer: 5 4 3 2 1 CH3 CH2 CH CH COOH CH3 CH3 2,3-dimetilpentanska kiselina
- 5. IUPAC nomenklatura (nastavak) Zasićene ciklične kiseline imenuju se kao cikloalkankarboksilne kiseline Odgovarajuće aromatične kiseline su benzoeve kiseline COOH Cl CH3CH2CH2 HO Br CH2 CH CHCH2CH2CH2COOH 5-propil-6-heptenska kiselina COOH 1-brom-2-hlorociklopentan- 2-hidroksibenzoeva kiselina karboksilna kiselina
- 6. Opšte metode za dobijanje Iz Grinjarovog reagensa O O O C O HX MgX2 + RMgX R C OMgX R C OH + Oksidacijom primarnih alkohola RCH2-OH + 2[O] → RCOOH + H2O Hidroliza nitrila (ORA 963) H+ R C N + 2H2O RCOOH + H2O + NH3
- 7. Ostale metode Oksidacijom aldehida Dekarboksilacijom malonskih kiselina Hidrolizom: anhidrida acil-halogenida estara amida masti i ulja, itd.
- 8. Fizičke osobine Tačke ključanja karboksilnih kiselina rastu prosečno oko 18°C za svaku metilensku grupu, isto kao i kod alkohola T.k. su, međutim, abnormalnije od onih za alkohole: etanol ključa na 78°C, a mravlja kiselina, HCOOH, koja ima istu molekulsku masu, na 101°C Objašnjenje - asocijacija molekula pomoću vodoničnih veza - građenje dimera O H O R C C R O H O
- 9. Rastvorljivost Zbog delimične jonizacije u vodi, karboksilne kiseline su jače hidratisane od alkohola i stoga pokazuju veću rastvorljivost u vodi Monokarboksilne kiseline se obično rastvaraju u organskim rastvaračima
- 10. Reakcije karboksilnih kiselina Građenje soli Jače su kiseline od alkohola zbog: dopunskog kiseonikovog atoma rezonancijom stabilizovanog karboksilatnog jona O O- O R C R C ili R C - O- O O Stoga reaguju: sa hidroksidima i grade soli R-COOH + NaOH → RCOONa + H2O
- 11. Reakcije karboksilnih kiselina sa karbonatima ili bikarbonatima, zato što CO2, zbog slabe rastvorljivosti u vodenom rastvoru kiseline, pomera ravnotežu udesno R-COOH + NaHCO3 → RCOONa + ↑CO2 + H2O 2R-COOH + Na2CO3 → 2RCOONa + ↑CO2 + H2O Zamena hidroksilne grupe halogenom (ORA 909) Koriste se neorganski halogenidi, najčešće PX3, PX5 i SOCl2 i dobijaju se acil-halogenidi PCl3 3 RCOOH 3 RCOCl + P(OH)3 RCOOH + SOCl2 → RCOCl + ↑SO2 + HCl
- 12. Acil-halogenidi Dobijanje acil-halogenida reakcijom karboksilnih kiselina sa halogenidima neorganskih kiselina (zamena hidroksilne grupe halogenom) Reakcija je opisana kod karboksilnih kiselina Nomenklatura Po IUPAC nomenklaturi ova grupa jedinjenja se imenuje tako što se trivijalnom nazivu acil-grupe doda naziv odgovarajućeg halogenida. Trivijalno ime acil-grupe dobija se od korena trivijalnog naziva odgovarajuće kiseline (na engleskom)kome se doda nastavak –il ili –oil.
- 13. TRIVIJALNO IME TRIVIJALNO IME BR. C- SISTEMSKO IME ACIL- ATOMA SRPSKO ENGLESKO GRUPE 1 METANSKA KISELINA MRAVLJA KISELINA FORMIC ACID FORMIL 2 ETANSKA KISELINA SIRĆETNA KISELINA ACETIC ACID ACETIL 3 PROPANSKA KISELINA PROPIONSKA KISELINA PROPIONIC ACID PROPIONIL 4 BUTANSKA KISELINA BUTERNA KISELINA BUTYRIC ACID BUTIRIL 5 PENTANSKA KISELINA VALERIJANSKA KISELINA VALERIC ACID VALERIL 12 DODEKANSKA KISELINA LAURINSKA KISELINA LAURIC ACID LAUROIL 14 TETRADEKANSKA KISELINA MIRISTINSKA KISELINA MYRISTIC ACID MIRISTOIL 16 HEKSADEKANSKA KISELINA PALMITINSKA KISELINA PALMITIC ACID PALMITOIL 18 OKTADEKANSKA KISELINA STEARINSKA KISELINA STEARIC ACID STEAROIL 18 CIS-9-OKTADECENSKA KISELINA OLEINSKA KISELINA OLEIC ACID OLEOIL CIS,CIS-9,12-OKTADEKADIENSKA 18 LINOLNA KISELINA LINOLIC ACID LINOLOIL KISELINA CIS,CIS,CIS-9,12,15- 18 OKTADEKATRIENSKA LINOLENSKA KISELINA LINOLENIC ACID LINOLENOIL KISELINA
- 14. Posebno je izraženo dejstvo nitro-grupe u orto- položaju, zbog malog rastojanja na kome ona deluje svojim jakim –I efektom na karboksilnu grupu, a verovatno i zbog sternih faktora Hidroksi- i metoksi- (odnosno u opštem slučaju alkoksi, -OR) grupe, kao i halogeni, pokazuju –I efekat (povećava aciditet kiseline) i +R efekat (smanjuje aciditet). Kod benzoevih kiselina koje u para-položaju imaju ove supstituente, dolazi upravo do izražaja +R efekat, koji može postati i preovlađujući.
- 15. Konstante aciditeta (Ka × 105) pojedinih supstituisanih benzoevih kiselina na 25°C u vodi SUPSTITUENT CH3 NO2 OCH3 H OH F Cl Br I POLOŽAJ orto 6,27 12,35 671 101 8,06 54,1 114 140 137 meta 6,27 5,35 32,1 8,27 8,17 13,6 14,8 15,8 14,1 para 6,27 4,24 37,0 2,95 3,38 7,22 10,5 10,7 -
- 16. 2. Esterifikacija Ako nema supstituenata u orto-položajima, esterifikacija karboksilne grupe odvija se kao i kod alifatičnih kiselina Ako je jedan orto- položaj supstituisan, brzina esterifikacije je znatno smanjena, dok ako su oba orto- položaja zauzeta, do esterifikacije ne dolazi (Viktor-Majerovo pravilo esterifikacije). Zapaženo je da pomenuti efekti ne zavise od prirode supstituenata, što upućuje na zaključak da se radi o sternom efektu.
- 17. 3. Građenje acil-halogenida Ide teže nego kod alifatičnih kiselina, pa se umesto PCl3 koristi PCl5 Acil-halogenidi su nerastvorni u vodi i vrlo sporo reaguju s njom
- 18. 4. Dekarboksilacija Pri topljenju soli aromatičnih karboksilnih kiselina sa nekom jakom bazom, dolazi do dekarboksilacije, pri čemu baza vezuje ugljen-dioksid u obliku karbonata i izdvaja se benzen COONa ∆ + Na2CO 3 + NaOH Ovoj reakciji podležu i soli alifatičnih kiselina, ali osim što CH3COONa daje metan, ostale soli daju niz drugih proizvoda, pa je ova reakcija u alifatičnoj seriji ostala bez praktične primene.