Estructura química del agua y sus propiedades
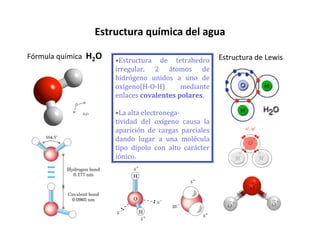
- 1. Estructura química del agua Fórmula química H2O •Estructura de tetrahedro Estructura de Lewis irregular. 2 átomos de hidrógeno unidos a uno de oxígeno(H‐O‐H) mediante enlaces covalentes polares. •La alta electronega‐ tividad del oxígeno causa la aparición de cargas parciales dando lugar a una molécula tipo dipolo con alto carácter iónico.
- 2. Puente de Hidrógeno Fuerza intermolecular débil que se produce entre un átomo de H enlazado covalentemente a un átomo muy electronegativo (F, O, N) y un par de e‐ solitarios de otro átomo electronegativo. El agua forma una gran red de interacciones de enlaces de hidrógeno. Resultado: Cada molécula de H2O en cualquier edo, es capaz de formar y aceptar 2 enlaces de hidrógeno (4 total), lo cual le conMiere las sig prop. FQs: •El agua tiene un anormal alto punto de ebullición y de fusión •El agua sólida (hielo) es menos densa que líquida •El agua tiene una alta tensión superCicial
- 5. Comparación de las propiedades del agua con moléculas similares: Puntos de fusión y ebullición El agua tiene altos puntos de fusión y ebullición.
- 7. Tensión superficial •Elevada tensión superCicial. Cantidad de energía necesaria para aumentar su super7icie por unidad de área. El agua es adhesiva y elástica. Las moléculas de la superMicie pierden puentes Capilaridad. Capacidad del agua para de H, por lo que son jaladas hacia el interior de avanzar a través de un canal minúsculo. la solución. Se resiste a aumentar la superMicie.
- 8. Solvente universal •Elevada constante dieléctrica. •Solvente universal. Excelente solvente debido a su polaridad. Es capaz de disolver un gran no. de compuestos POLARES (Sales, azúcares, DNA). Solvatación: Proceso de atracción y asociación de moléculas de un disolvente con las del soluto. Las moléculas de solvente rodean a los iones, dispersándolos y disolviéndolos. Re7leja el número de dipolos de una molécula. Medida de las propiedades El agua disuelve las sales, hidratándolas y estabilizando del solvente para mantener cargas los iones resultantes, debilitando sus interacciones opuestas separadas. electrostáticas.
