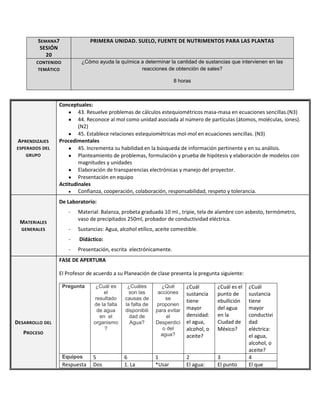
Determinación de pH y conductividad eléctrica
- 1. SEMANA7 SESIÓN 20 PRIMERA UNIDAD. SUELO, FUENTE DE NUTRIMENTOS PARA LAS PLANTAS CONTENIDO TEMÁTICO ¿Cómo ayuda la química a determinar la cantidad de sustancias que intervienen en las reacciones de obtención de sales? 8 horas APRENDIZAJES ESPERADOS DEL GRUPO Conceptuales: 43. Resuelve problemas de cálculos estequiométricos masa-masa en ecuaciones sencillas.(N3) 44. Reconoce al mol como unidad asociada al número de partículas (átomos, moléculas, iones). (N2) 45. Establece relaciones estequiométricas mol-mol en ecuaciones sencillas. (N3) Procedimentales 45. Incrementa su habilidad en la búsqueda de información pertinente y en su análisis. Planteamiento de problemas, formulación y prueba de hipótesis y elaboración de modelos con magnitudes y unidades Elaboración de transparencias electrónicas y manejo del proyector. Presentación en equipo Actitudinales Confianza, cooperación, colaboración, responsabilidad, respeto y tolerancia. De Laboratorio: - Material: Balanza, probeta graduada 10 ml., tripie, tela de alambre con asbesto, termómetro, vaso de precipitados 250ml, probador de conductividad eléctrica. - Sustancias: Agua, alcohol etílico, aceite comestible. - Didáctico: - Presentación, escrita electrónicamente. MATERIALES GENERALES FASE DE APERTURA El Profesor de acuerdo a su Planeación de clase presenta la pregunta siguiente: Pregunta ¿Cuál es el resultado de la falta de agua en el organismo ? ¿Cuáles son las causas de la falta de disponibili dad de Agua? ¿Qué acciones se proponen para evitar el Desperdici o del agua? ¿Cuál sustancia tiene mayor densidad: el agua, alcohol, o aceite? ¿Cuál es el punto de ebullición del agua en la Ciudad de México? Equipos 5 Dos 6 1. La 1 *Usar 2 El agua: 3 El punto DESARROLLO DEL PROCESO Respuesta ¿Cuál sustancia tiene mayor conductivi dad eléctrica: el agua, alcohol, o aceite? 4 El que
- 2. terceras partes del cuerpo humano está compuest o por agua, de allí la importanci a de mantener el cuerpo en constante hidratació n para que funcione de manera optima. La deshidrata ción provoca alteracion es en diferentes órganos de nuestro cuerpo, tales como: Sistema circulatori o. Sistema urinario. Sistema nervioso. Entre algunos efectos provocado contamina cion 2. EL aumento de la poblacion 3. Su mal uso 4. La escases ( porque solo tenemos el 3°/. del aagua de todo el planeta) 5. Las construcci ones que contamina n el agua 6. Porque las desperdici aomos 7. La tala de arboles 8. por el calentami ento global cubetas 1g/cm3 de agua cuando se lava el coche. * Tener recolector es de agua en temporad a de lluvias. * Cerrar la ducha mientras te jabonas * Verificar no tener fugas en casa, trabajo, escuela, etc. * Reusó de agua jabonosa para actividade s de limpieza. * Cerrar el grifo mientras te cepilles los dientes hasta el momento de enjuagarte * Regar las plantas y césped apenas se pierda el sol, para evitar que el agua se de ebullición del agua en la Cd. De México es de 90 grados centígrado s. tiene mayor conductivi dad es el alcohol.
- 3. s por falta de agua en el cuerpo a tal punto de provocar deshidrata ción, están los siguientes: Estomatiti s (inflamaci ón de la boca). Faringitis (inflamaci ón de la faringe). Diabetes. Enfermed ades pulmonar es. evapore del jardín * Con el agua que lavas las verduras podes regar las plantas. * Lavar el auto con menor frecuencia * Utilizar programas cortos en el lavado de ropa automátic oy mejorar la calidad de los jabones. * Lavar el auto con menos frecuencia Problemas renales. Cada equipo lee diferente contenido sobre la misma pregunta. - FASE DE DESARROLLO - � partir del ejemplo de obtención de un fertilizante, organizar un trabajo de A - discusión colectivo para interpretar cuantitativamente la ecuación química en - función del mol como la unidad de medida de la cantidad de sustancia: - - Análisis de la ecuación ya balanceada en función del número de partículas - participantes; por ejemplo, una molécula de X reacciona con dos moléculas - de Y. - - Escalar el número de partículas participantes; por ejemplo, dos moléculas - de X reaccionan con cuatro moléculas de Y, una docena de moléculas de X
- 4. - reaccionan con dos docenas de moléculas de Y. - - Definir el mol como una unidad asociada al número de partículas, que es de - gran utilidad en química. - - Lectura de ecuaciones químicas balanceadas en función de la unidad mol - (un mol de X reacciona con dos mol de Y). - Relacionar la masa de las sustancias participantes en la reacción química - con su número de moles, considerando al mol como la masa molecular de - una sustancia expresada en gramos (masa molar). - (A44) - � Realizar ejercicios de cálculos estequiométricos mol-mol que impliquen la - obtención de sales. (A45) Material: Capsula de porcelana, indicador universal, papel indicador de pH Sustancias: las naranjas, los limones y las mandarinas, solución del suelo: abajo, en medio, arriba. Indicadores, agua destilada. - - PROCEDIMIENTO: Ver los colores que tiene cada indicador disponible en medio ácido y en el básico. Colocar en la capsula de porcelana cinco gotas de la sustancia, medir el pH con la tira indicadora, enseguida adicionar tres gotas del indicador universal, anotar el color inicial y final. Averiguar si un producto desconocido se comporta como ácido o básico. Detectar en el jugo de cada cítrico. Y su conductividad eléctrica. Detectar en la Disolución de la germinación de cada suelo y su conductividad eléctrica Sustancia Nombre O Formula Ionización Y pH Color inicial Color Final Tipo de susta ncia Acido, sal, hidróx ido Conductividad eléctrica Naranja Ácido ascórbico pH:3 Naranja pálido. Naranja Ácido Si hay pH:2 Verde Claro Naranja fuerte Acido Alta C6H8O6 Limón C6H8O7
- 5. Mandarina Solución del suelo abajo Ácido cítrico. C6H8O7 pH:4 Cloruros Naranja fuerte Ácido pH: 7 transparente Verde oscuro sal Baja conductividad pH:7 Café claro verde sal Sin conductividad pH: 6 Amarillo verdoso Verde obscuro Sal Sin conductividad (Cl) En medio Arriba Naranja claro OHH+ +H2O Tiene conductividad 1electrica Después discuten y sintetizan el contenido. Se preparan para mostrarlo a los demás equipos. Observaciones y conclusiones: En la clase de hoy pudimos apreciar de forma clara la organización en los equipos así como la forma en el que cada uno analizó el tema y posteriormente lo desarrollo. Se llegó a la conclusión de la importancia que tiene el pH en la vida cotidiana y como ejemplo tenemos a las muestras del invernadero. Fotos:
- 8. Para simular el procedimiento se les proporciona el nombre del programa crocodrile para que lo localicen en la Red y lo utilicen, es gratuito. FASE DE CIERRE Los equipos presentan su información a los demás. Al final de las presentaciones se lleva a cabo una discusión extensa, en la clase con el profesor, de lo que se aprendió. Actividad Extra clase: Los alumnos llevaran la información a su casa e indagaran los temas siguientes de acuerdo al cronograma. Elaboraran su informe, en un documento electrónico, para registrar los resultados en su Blog. EVALUACIÓN Producto: Presentación del producto. Resumen de la indagación bibliográfica. Actividad de Laboratorio. Tabulación y graficas elaboradas por el grupo. Indagación del programa crocodrile.