La formación de amoniaco 1
•Descargar como DOCX, PDF•
0 recomendaciones•915 vistas
Denunciar
Compartir
Denunciar
Compartir
Más contenido relacionado
La actualidad más candente
La actualidad más candente (20)
AMONIACO - OBTENCION A PARTIR DEL GAS DE SINTESIS (H2)

AMONIACO - OBTENCION A PARTIR DEL GAS DE SINTESIS (H2)
Más de Ruziel Ruiz Antonio
Más de Ruziel Ruiz Antonio (6)
Último
Último (20)
Generalidades de Anatomía - Ayudantía de Cátedra AHCG .pdf

Generalidades de Anatomía - Ayudantía de Cátedra AHCG .pdf
PARES CRANEALES. ORIGEN REAL Y APARENTE, TRAYECTO E INERVACIÓN. CLASIFICACIÓN...

PARES CRANEALES. ORIGEN REAL Y APARENTE, TRAYECTO E INERVACIÓN. CLASIFICACIÓN...
conocer los modelos atómicos a traves de diversos ejemplos y características

conocer los modelos atómicos a traves de diversos ejemplos y características
DESPOTISMO ILUSTRADOO - copia - copia - copia - copia.pdf

DESPOTISMO ILUSTRADOO - copia - copia - copia - copia.pdf
Woods, Thomas E. - Cómo la Iglesia construyó la Civilización Occidental [ocr]...![Woods, Thomas E. - Cómo la Iglesia construyó la Civilización Occidental [ocr]...](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
![Woods, Thomas E. - Cómo la Iglesia construyó la Civilización Occidental [ocr]...](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
Woods, Thomas E. - Cómo la Iglesia construyó la Civilización Occidental [ocr]...
ECOGRAFIA RENAL Y SUS VARIANTES ANATOMICAS NORMALES

ECOGRAFIA RENAL Y SUS VARIANTES ANATOMICAS NORMALES
Perfiles NEUROPSI Atención y Memoria 6 a 85 Años (AyM).pdf

Perfiles NEUROPSI Atención y Memoria 6 a 85 Años (AyM).pdf
Ensayo ENRICH (sesión clínica, Servicio de Neurología HUCA)

Ensayo ENRICH (sesión clínica, Servicio de Neurología HUCA)
Gribbin, John. - Historia de la ciencia, 1543-2001 [EPL-FS] [2019].pdf![Gribbin, John. - Historia de la ciencia, 1543-2001 [EPL-FS] [2019].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
![Gribbin, John. - Historia de la ciencia, 1543-2001 [EPL-FS] [2019].pdf](data:image/gif;base64,R0lGODlhAQABAIAAAAAAAP///yH5BAEAAAAALAAAAAABAAEAAAIBRAA7)
Gribbin, John. - Historia de la ciencia, 1543-2001 [EPL-FS] [2019].pdf
Informe Aemet Tornados Sabado Santo Marchena Paradas

Informe Aemet Tornados Sabado Santo Marchena Paradas
Tema 1. Generalidades de Microbiologia Universidad de Oriente

Tema 1. Generalidades de Microbiologia Universidad de Oriente
La formación de amoniaco 1
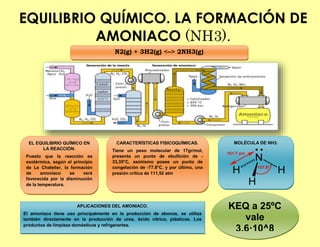
- 1. EQUILIBRIO QUÍMICO. LA FORMACIÓN DE AMONIACO (NH3). N2(g) + 3H2(g) <–> 2NH3(g) EL EQUILIBRIO QUÍMICO EN LA REACCIÓN. Puesto que la reacción es exotérmica, según el principio de Le Chatelier, la formación de amoniaco se verá favorecida por la disminución de la temperatura. CARACTERÍSTICAS FISICOQUÍMICAS. Tiene un peso molecular de 17gr/mol, presenta un punto de ebullición de - 33,35°C, asimismo posee un punto de congelación de -77.8°C, y por último, una presión crítica de 111,52 atm MOLÉCULA DE NH3. APLICACIONES DEL AMONIACO. El amoniaco tiene uso principalmente en la producción de abonos, se utiliza también directamente en la producción de urea, ácido nítrico, plásticos. Los productos de limpieza domésticos y refrigerantes. KEQ a 25ºC vale 3,6·10^8
