Θερμοδυναμική
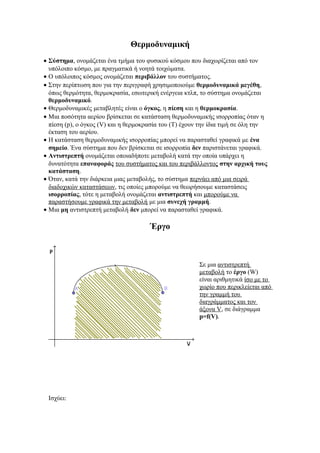
- 1. Θερμοδυναμική • Σύστημα, ονομάζεται ένα τμήμα του φυσικού κόσμου που διαχωρίζεται από τον υπόλοιπο κόσμο, με πραγματικά ή νοητά τοιχώματα. • Ο υπόλοιπος κόσμος ονομάζεται περιβάλλον του συστήματος. • Στην περίπτωση που για την περιγραφή χρησιμοποιούμε θερμοδυναμικά μεγέθη, όπως θερμότητα, θερμοκρασία, εσωτερική ενέργεια κτλπ, το σύστημα ονομάζεται θερμοδυναμικό. • Θερμοδυναμικές μεταβλητές είναι ο όγκος, η πίεση και η θερμοκρασία. • Μια ποσότητα αερίου βρίσκεται σε κατάσταση θερμοδυναμικής ισορροπίας όταν η πίεση (p), ο όγκος (V) και η θερμοκρασία του (T) έχουν την ίδια τιμή σε όλη την έκταση του αερίου. • Η κατάσταση θερμοδυναμικής ισορροπίας μπορεί να παρασταθεί γραφικά με ένα σημείο. Ένα σύστημα που δεν βρίσκεται σε ισορροπία δεν παριστάνεται γραφικά. • Αντιστρεπτή ονομάζεται οποιαδήποτε μεταβολή κατά την οποία υπάρχει η δυνατότητα επαναφοράς του συστήματος και του περιβάλλοντος στην αρχική τους κατάσταση. • Όταν, κατά την διάρκεια μιας μεταβολής, το σύστημα περνάει από μια σειρά διαδοχικών καταστάσεων, τις οποίες μπορούμε να θεωρήσουμε καταστάσεις ισορροπίας, τότε η μεταβολή ονομάζεται αντιστρεπτή και μπορούμε να παραστήσουμε γραφικά την μεταβολή με μια συνεχή γραμμή. • Μια μη αντιστρεπτή μεταβολή δεν μπορεί να παρασταθεί γραφικά. Έργο Σε μια αντιστρεπτή μεταβολή το έργο (W) είναι αριθμητικά ίσο με το χωρίο που περικλείεται από την γραμμή του διαγράμματος και τον άξονα V, σε διάγραμμα p=f(V). Ισχύει:
- 2. Άρα: Επομένως, το έργο είναι ίσο με την πίεση που ασκείται στο αέριο, επί την μεταβολή του όγκου του αερίου. Συμπερασματικά, το έργο θα είναι θετικό όταν το αέριο εκτονώνεται και αρνητικό όταν το αέριο συμπιέζεται. • Για ισόθερμη μεταβολή ισχύει: • Για ισόχωρη μεταβολή ισχύει: • Για ισοβαρή μεταβολή ισχύει: • Για αδιαβατική μεταβολή ισχύει: Εσωτερική Ενέργεια • Εσωτερική ονομάζουμε το άθροισμα των ενεργειών που εμπεριέχει κάθε σώμα, εξαιτίας της σχετικής κίνησης των σωματιδίων, που το απαρτίζουν, ως προς το κέντρο μάζας του σώματος αυτού. Ισχύει: Για Ν μόρια αερίου, η εσωτερική ενέργεια είναι: Αλλά: Επομένως: Η μεταβολή της εσωτερικής ενέργειας (ΔU) εξαρτάται μόνο από την αρχική και τελική κατάσταση του συστήματος.
- 3. • Για όλες τις μεταβολές ισχύει: • Για ισόθερμη μεταβολή ιδιαίτερα ισχύει: • Για αδιαβατική μεταβολή, επίσης ισχύει: Θερμότητα Θερμότητα (Q) ονομάζεται η ενέργεια που μεταφέρεται λόγω της διαφοράς θερμοκρασίας δύο σωμάτων. Η Θερμότητα (Q) είναι μορφή ενέργειας. Η θερμοκρασία (T) είναι φυσικό μέγεθος. • Σύμφωνα με τον Πρώτο Θερμοδυναμικό Νόμο: Το πόσο Θερμότητας (Q) που απορροφά ή αποβάλλει ένα θερμοδυναμικό σύστημα είναι ίσο με το αλγεβρικό άθροισμα της μεταβολής της εσωτερικής του ενέργειας και του έργου που παράγει ή δαπανά το σύστημα. Δηλαδή: Q=ΔU+W Ο Πρώτος Θ.Ν. είναι απόρροια της Α.Δ.Ε. • Για την ισόθερμη ισχύει: • Για την ισόχωρη ισχύει: • Για την ισοβαρή ισχύει κανονικά ο Πρώτος Θ.Ν: • Για την αδιαβατική ισχύει: Ειδικές μεταβολές 1. Αδιαβατική μεταβολή Αδιαβατική ονομάζεται η μεταβολή κατά την οποία δεν υπάρχει ανταλλαγή Θερμότητας μεταξύ του συστήματος και του περιβάλλοντος. Νόμος του Poisson:
- 4. 2. Κυκλική μεταβολή Κυκλική ονομάζεται η μεταβολή στην οποία το σύστημα, μετά από μια διεργασία, επιστρέφει στην αρχική κατάσταση. Για την κυκλική μεταβολή ισχύει: • Η ΔU είναι ίση με το μηδέν. • Το W είναι ίσο με το χωρίο που περικλείεται από την γραφική παράσταση της μεταβολής Γραμμομοριακές Ειδικές Θερμότητες Ισχύει: A , c= ειδική θερμότητα του υλικού. Άρα: , C= γραμμομοριακή ειδική θερμότητα του υλικού. • Η γραμμομοριακή ειδική θερμότητα C εκφράζει το ποσό θερμότητας που πρέπει να προσφερθεί σε 1 mol του σώματος, για να αυξηθεί η θερμοκρασία του κατά ένα βαθμό. Στα στερεά και τα υγρά η Γ.Ε.Θ. εξαρτάται αποκλειστικά από το υλικό. Στα αέρια εξαρτάται επίσης από τον τρόπο με τον οποίο θερμαίνονται. Συγκεκριμένα: • Θέρμανση με σταθερό όγκο Όμως, κατά την ισόχωρη μεταβολή το W είναι μηδέν. Επομένως: Άρα, από τι παραπάνω σχέσεις(1):
- 5. • Θέρμανση με σταθερή πίεση (2): Το παραγόμενο έργο είναι: Από καταστατική έχουμε: Δηλαδή (3): Από τον Π.Θ.Ν.: Με την χρήση των σχέσεων (1),(2) και (3), ο Π.Θ.Ν μετασχηματίζεται: Με απλοποίηση, τελικά: Υπολογισμός Cp και CV Ισχύει: και Άρα: Με απλοποίηση: Με την χρήση του τύπου: Έχουμε: Τέλος, το γ, που βρήκαμε στην αδιαβατική, υπολογίζεται με τον τύπου: • Για τα πραγματικά αέρια η τιμή του γ εξαρτάται από την ατομικότητα και το είδος των δεσμών που συγκρατούν τα άτομα σε μόρια του αερίου.
- 6. Θερμικές μηχανές • Θερμική μηχανή ονομάζουμε την διάταξη που μετατρέπει την θερμότητα σε μηχανικό έργο. Κατά την διάρκεια μιας κυκλικής μεταβολής του μέσου, η μηχανή: 1. Απορροφά Θερμότητα (Qh) από μια δεξαμενή υψηλής Θερμοκρασίας (Th). 2. Παράγει Έργο (W). 3. Αποβάλλει Θερμότητα (Qc) σε μια δεξαμενή χαμηλότερης Θερμοκρασίας (Tc). • Ο συντελεστής απόδοσης (e) οποιασδήποτε μηχανής, είναι ο λόγος του Έργου (W) που παράγει η μηχανή προς την Ενέργεια που δαπανάται (Qh) για την λειτουργία της. Δηλαδή: Το Έργο (W), είναι ίσο: Άρα (4): Δεύτερος Θερμοδυναμικός Νόμος Κατά Kelvin και Planck: • Είναι αδύνατο να κατασκευαστεί θερμική μηχανή που να μετατρέπει εξ ολοκλήρου τη θερμότητα σε ωφέλιμο έργο. Κατά Clausious: • Είναι αδύνατο να κατασκευαστεί μηχανή που να μεταφέρει θερμότητα από ένα ψυχρό σε ένα θερμότερο σώμα, χωρίς να δαπανάται ενέργεια για την λειτουργία της. Μηχανή Carnot • Δεν μπορεί να υπάρξει θερμική μηχανή που να έχει μεγαλύτερη απόδοση από μια μηχανή Carnot, η οποία λειτουργεί ανάμεσα στις ίδιες θερμοκρασίες. Ο Κύκλος Carnot αποτελείται από: 1. Μια ισόθερμη εκτόνωση Α→Β, με Th και Qh. 2. Μια αδιαβατική εκτόνωση Β→Γ, με Tc. 3. Μια ισόθερμη συμπίεση Γ→Δ, με Tc και Qc. 4. Μια αδιαβατική συμπίεση Δ→Α, με Th.
- 7. Για την μηχανή Carnot ισχύει: Αντικαθιστώντας στην (4), για την Carnot ισχύει: