UNIDADES QUIMICAS DE MASA.pptx
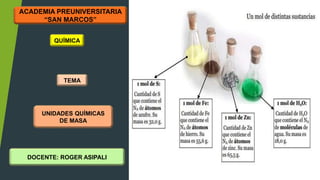
- 1. ACADEMIA PREUNIVERSITARIA “SAN MARCOS” QUÍMICA TEMA UNIDADES QUÍMICAS DE MASA DOCENTE: ROGER ASIPALI
- 2. Tema: Unidades Químicas de masa Es el estudio de las unidades estructurales que conforma o presenta una especie química (átomos,moléculas,iones,etc). Conceptos previos: 1) Unidad de Masa Atómica (UMA) (u) Se define como la doceava parte de la masa de Carbono – 12. Gráficamente:
- 3. 2) ¿Qué es el mol? Para el sistema Internacional (S.I), el mol indica la cantidad de sustancia. Para la cuantificación de la materia, el mol es la cantidad de unidades estructurales que tiene una especie química (átomos, moléculas,etc) como tantas unidades elementales existe en el carbono – 12. También el mol se denomina como Número de Avogadro (𝑁𝐴), siendo su equivalencia: 1mol = 6,023.1023 1 mol = 6.1023 (forma práctica) 1 mol = Número de Avogadro ( 1mol = 𝑁𝐴) Ejemplos: 1 mol de átomos de P = 6,023x1023 átomos de P = 𝑁𝐴 átomos de P 1 mol de átomos de K = 6,023x1023 átomos de K = NA átomos de K 1 mol de moléculas de C𝑂2 = 6,023x1023 moléculas de 𝐶𝑂2= NA moléculas de 𝐶𝑂2 1 mol de moléculas de 𝐶𝐻4 = 6,023x1023 moléculas de 𝐶𝐻4 = NA moléculas de 𝐶𝐻4
- 4. 3) Masa atómica Promedio. (Peso atómico (P.A)) Cuando se conoce la cantidad de isótopos de un elemento, su masa en UMA y sus porcentajes de abundancia se puede calcular una masa atómica promedio que vendría a ser el peso atómico del elemento. Ejemplo: Determinar el peso atómico del cloro a partir de los siguientes datos que se muestra a continuación en el siguiente cuadro:
- 5. Resolución:
- 6. 4) Átomo – gramo (at-g) 1 at-g (Mg) = 24g (Mg) = 1 mol de átomos (Mg) 1 at-g (Ca) = 40g (Ca) = 1 mol de àtomos (Ca) 1 at-g (K) = 39g ( K ) = 1 mol de átomos ( K ) 1 at-g (P) = 31g (P) = 1 mol de átomos ( P) ¿Cuántos at-g de Magnesio existe en 480g de dicho elemento? P.A(Mg)= 24 Resolución: #at-g (E) = 𝑚𝑎𝑠𝑎 𝑀 #At-g(Mg)= 480 24 = 20 at-g (Mg) 1 at-g (E) = P.A(E)g = 1 mol átomos ( E) (E): Elemento
- 7. 5) Molécula – gramo (mol – g) (X): Compuesto Químico Ejemplos: 𝑴(𝑪𝑯𝟒): (12) + 4 (1) = 16 𝑀 (𝑆𝑂2): (32) + 2 (16) = 64 𝑀 (𝐻2S𝑂4): 2(1) + 32 + 4(16) = 98 𝑀 (CaC𝑂3): (40) + (12) + 3(16) = 100 𝑀 (𝐶𝑎3 𝑃𝑂4 2): 3(40) + 2(31) + 8 (16)= 310 1mol-g (X) = 𝑀(X)g = 1 mol moléculas (X)
- 8. 6) Número de moles (n) Se tiene 24x1023 moléculas de 𝑆𝑂3, entonces determine la masa que contiene dicha sustancia química. PA (S=32;0=16) 𝑁𝐴= 6x1023 Resolución: 𝑀(𝑆𝑂3): (32) +3 (16)= 80 Luego: n= 𝑚𝑎𝑠𝑎 𝑀 = #𝑚𝑜𝑙é𝑐𝑢𝑙𝑎𝑠 𝑁𝐴 ⇒ 𝑀𝐴𝑆𝐴 80 = 24𝑥1023 6𝑥1023 MASA= 320g 𝑆𝑂3 PROBLEMAS PROPUESTOS 01.- ¿Cuánto pesa 5 at-g de carbono? P.A ( C )= 12 Resolución: 5at-g (C) = 5 x (12g) = 60g 5 at-g ( C ) = 60g de carbono n= 𝑚𝑎𝑠𝑎 𝑀 = #𝑚𝑜𝑙é𝑐𝑢𝑙𝑎𝑠 𝑁𝐴
- 9. 02.- ¿Qué molécula presenta mayor masa molecular? Resolución: a) Agua 𝑀 (𝐻2O): 2(1) + (16) = 18 b) Ozono 𝑀 (𝑂3): 3 (16) = 48 c) Amoniaco 𝑀 (𝑁𝐻3): (14) + 3 (1) = 17 d) dioxígeno 𝑀 (𝑂2): 2 (16): 32 e) Nitrógeno gas 𝑀 (𝑁2): 2 (14) = 28 El compuesto que presenta mayor masa molecular es el ozono.
- 10. 03.- ¿Cuántas moles existen en 900 de agua? P.A (H=1;O=16) Resolución: 𝑀(𝐻2O) : 2(1) + 16 = 18 Luego: n = 900 18 = 50 Existen en total 50 moles en 900g de agua. 04.- Calcule la masa de 24.1024 moléculas de metano (𝐶𝐻4). P.A (C=12; H=1) 𝑁𝐴=6.1023 Resolución: 𝑀(𝐶𝐻4): 12 + 4(1)= 16 n= 𝑚𝑎𝑠𝑎 16 = 24.1024 6.1023 luego: masa = 16x40= 640g de metano.