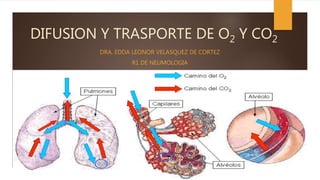
Dfusion y transporte de o2 y co2
- 1. DIFUSION Y TRASPORTE DE O2 Y CO2 DRA. EDDA LEONOR VELASQUEZ DE CORTEZ R1 DE NEUMOLOGIA
- 2. DIFUSION Movimiento de moléculas a través de una membrana semi-permeable desde una zona en la que un gas determinado ejerce una presión parcial elevada a una zona en la que se ejerce una presión parcial inferior.
- 3. DIFUSION El movimiento de un gas por difusión es por lo tanto diferente del movimiento de los gases a través de las vías de conducción que se produce mediante un ¨flujo de masa¨ (MOVIMIENTO DE MASA O CONVECCION). Durante el flujo de masa, el movimiento del gas se produce por diferencias de presión total, y las moléculas de gases diferentes se mueven juntas a lo largo del gradiente de presión total. Durante la difusión, cada gas se desplaza en función de sus propios gradientes de presión parcial.
- 4. DIFUSION La transferencia de gases durante la difusión se produce por un movimiento molecular aleatorio, depende, por lo tanto de la temperatura, ya que el movimiento molecular aumenta cuando se incrementa la temperatura.
- 5. DIFUSION POR LA LEY DE FICK El oxigeno llega a los alveolos mediante un flujo de masa a través de las vías respiratorias de conducción y al fluir aire por estas durante la inspiración, la velocidad lineal del flujo de masa disminuye a medida que el aire se acerca a los alveolos.
- 6. En el momento que el aire llega a los alveolos, es probable que cese el flujo de masa y que el movimiento de gases posterior se produzca por difusión. DIFUSION POR LA LEY DE FICK ENTONCES EN FASE GASEOSA EL OXIGENO SE DESPLAZA POR LOS ALVEOLOS DE ACUERDO CON SU PROPIO GRADIENTE DE PRESION PARCIAL LA DISTANCIA DEL CONDUCTO ALVEOLAR A LA INTERFASE ALVEOLOCAPILAR SUELE SER MENOS DE 1MM SE SUPONE QUE LA DIFUSION EN LA FASE GASEOSA ALVEOLAR DEPENDE DE LAS PULSACIONES DEL CORAZON Y EL FLUJO SANGUINEO, QUE SE TRASMITEN A LOS ALVEOLOS Y AUMENTA EL MOVIMIENTO MOLECULAR
- 7. DIFUSION POR LA LEY DE FICK A CONTINUACION EL OXIGENO SE DIFUNDE ATRAVES DE LA INTERFASE ALVEOLOCAPILAR PASA DE UNA FASE GASEOSA A UNA LIQUIDA CONFORME LA LEY DE HENRY LEY DE HENRY. LA CANTIDAD GAS ABSORVIDA POR UN LIQUIDO CON EL QUE NO SE COMBINA A NIVEL QUIMICO ES DIRECTAMENTE PROPORCIONAL A LA PRESION PARCIAL DEL GAS A LA CUAL ESTA EXPUESTO EL LIQUIDO Y A LA SOLUBILIDAD DEL GAS EN EL LIQUIDO
- 8. EL O2 DEBE DISOLVERSE EN LA DELGADA CAPA DE TENSOACTIVO PULMONAR ATRAVESAR EL EPITELIO ALVEOLAR EL INSTERTICIO EL ENDOTELIO CAPILAR LUEGO SE DIFUNDIRA ATRAVES DEL PLASMA DONDE PERMANECERA DISUELTO LA MAYOR PARTE SE INTRODUCE EN EL ERITROCITO Y SE COMBINA CON LA HEMOGLOBINA DESPUES LA SANGRE TRASPORTA EL OXIGENO FUERA DEL PULMON POR UN FLUJO DE MASA Y LO DISTRIBUYE AL RESTO DEL CUERPO DIFUSION POR LA LEY DE FICK
- 9. DIFUSION POR LA LEY DE FICK EL O2 DIFUNDE DESDE EL ERITROCITO ATRAVES DEL PLASMA EL ENDOTELIO CAPILAR EL INSTERTICIO LA MEMBRANA CELULAR HISTICA AL INTERIOR DE LAS CELULAS Y DE LA MEMBRANA MITOCONDRIAL
- 10. FACTORES QUE DETERMINAN LA VELOCIDAD DE DIFUSION DE UN GAS A X D X (P1 - P2) Vgas = _________________ T ATRAVES DE LA BARRERA ALVEOLOCAPILAR SE DESCRIBEN MEDIANTE: Se supone que el área de la barrera hematogaseosa es de cuando menos 70 m2 en un adulto sano de estatura media, en reposo, es decir, cerca de 70 m2 de superficie potencial es ventilada y perfundido en reposo.
- 11. El grosor de la barrera de difusión alveolo- capilar es apenas de 0.2 a 0.5 µm Puede aumentar en caso de fibrosis, o edema intersticial e interferir con la difusión. DIFUSION POR LA LEY DE FICK Si se reclutan más capilares como en el ejercicio, el área disponible para la difusión aumenta. Si el retorno venoso desciende, debido a una hemorragia o si la presión alveolar se eleva por ventilación a presión positiva entonces se DESRRECLUTAN CAPILARES, y entonces puede descender la superficie disponible para la difusión.
- 12. DIFUSION POR LA LEY DE FICK DIFUSIBILIDAD DE UN GAS O CONSTANTE DE DIFUSION Es directamente proporcional a la solubilidad del gas en la barrera de difusión e inversamente proporcional a la raíz cuadrada del peso molecular del mismo. Solubilidad D α _________________ MW
- 13. DIFUSION POR LA LEY DE FICK LA LEY DE GRAHAM ESTABLECE: Que las velocidades de difusión relativas de dos gases son inversamente proporcionales a las raíces cuadradas de sus pesos moleculares, si todo lo demás es igual. = 𝑀𝑊 𝑂2 𝑀𝑊 𝐶𝑂2 = 0.85 En el caso de los dos casos de mayor interés en el pulmón:
- 14. DIFUSION POR LA LEY DE FICK Debido a que las velocidades de difusión relativas son inversamente proporcionales a la relación de las raíces cuadradas, de sus pesos moleculares: Velocidad de difusión para el O2 1 ____________________________________________ α ____________ = 1.17 Velocidad de difusión para el CO2 0.85
- 15. DIFUSION POR LA LEY DE FICK El oxigeno es menos denso que el dióxido de carbono, se difundirá 1.2 veces mas rápido que el dióxido de carbono, mientras atraviesa el alveolo. Sin embargo en la barrera alveolocapilar se consideraran también las solubilidades relativas del oxigeno y dióxido de carbono. En la fase liquida la solubilidad del CO2 es cerca de 24 veces la del O2 y por ello el CO2 se difunde unas 0.85 x 24 o unas 20 veces mas rápido, a través de la barrera alveolocapilar que el oxigeno.
- 16. LIMITACIONES DE LA TRANSFERENCIA DE GASES
- 17. LIMITACIONES DE LA DIFUSION La afinidad del monóxido de carbono por la hemoglobina es casi 210 veces la del oxigeno por la hemoglobina. La presión parcial alveolar es diferente para cada uno de los tres gases.
- 18. LIMITACIONES DE LA PERFUSION La presión parcial del oxido nitroso en la sangre capilar pulmonar se equilibra muy rápido con la presión parcial de oxido nitroso en el alveolo debido a que este se desplaza a través de la barrera alveolocapilar con mucha facilidad y porque no se combina a nivel químico con la hemoglobina de los eritrocitos.
- 21. MEDIDAS DE LA CAPACIDAD DE DIFUSION
- 22. Mide la velocidad con la que el CO pasa desde el alvéolo a la sangre. Informa sobre el volumen del lecho capilar pulmonar en contacto con los alvéolos ventilados, la superficie alveolar útil y el espesor de la membrana alvéolo-capilar. La forma de medir la DLCO más usada es la de la respiración única con apnea. Método: Espiración forzada máxima hasta VR y posterior inspiración al máximo hasta alcanzar la CPT inhalando un gas compuesto por He 10% y CO al 0,3%. Mantener la apnea 10 segundos. Posteriormente se mide la cantidad de CO en el aire exhalado y la diferencia entre la que inhaló y la exhalada representa la cantidad de CO absorbida. La DLCO se calcula con la siguiente fórmula: DLCO= (V alveolar x T apnea x Fracción inicial de CO) / ((Patm – 47) x ( fracción alveolar final de CO)) CAPACIDAD DE DIFUSIÓN DEL MONÓXIDO DE CARBONO
- 23. CAPACIDAD DE DIFUSIÓN DEL MONÓXIDO DE CARBONO Si los pulmones son normales, el CO del aire inspirado se absorbe bien. Si esto no ocurre significa que el intercambio del CO y por lo tanto del oxígeno entre los pulmones y la sangre es anormal. La capacidad de difusión es anormal en personas con enfermedades como la fibrosis pulmonar, enfisema y otros trastornos que afectan a los vasos sanguíneos pulmonares. La duración del examen es de aproximadamente 20 minutos.
- 24. La DLCO se encuentra aumentada en estas enfermedades: 1) Policitemia. 2) Vasculitis 3) Hemorragias alveolares. La DLCO puede disminuir en las siguientes enfermedades: 1) Enfisema pulmonar. 2) Neumopatías intersticiales. 3) Hipertensión pulmonar. CAUSAS QUE ALTERAN LA DIFUSION DE MONOXIDO DE CARBONO
- 25. La capacidad de Difusión es muy útil en el diagnóstico diferencial de obstrucción crónica de la via aérea en fumadores. Los valores estan reducidos en enfisema y normal o altos en asma. Puede estar disminuido en asmaticos cuando existe obstrucción y mala distribución de la ventilación y la perfusión. En pacientes con diagnóstico previo de asma, no es considerada una prueba útil. DIFUSION DE MONOXIDO DE CARBONO
- 26. SITUACIONES QUE REDUCEN LA CAPACIDAD DE DIFUSION ENGROSAMIENTO DE LA BARRERA Edema intersticial o alveolar Fibrosis intersticial o alveolar Sarcoidosis Esclerodermia DISMINUCION DE LA SUPERFICIE Tumores Enfisema Gasto cardiaco bajo Volumen sanguíneo capilar bajo DISMINUCION EN LA CAPTACION DE ERITROCITOS Anemia Volumen sanguíneo capilar pulmonar bajo DESAJUSTE VENTILACION - PERFUSION
- 27. TRANSPORTE DE OXIGENO ATRAVES DE LA SANGRE A una temperatura de 37°C, 1 ml de plasma contiene 0.00003 ml O2/mmHg de PO2. La sangre arterial normal con una PO2 aproximada de 100 mmHg contiene solo cerca de 0.003 ml de O2/ml de sangre o 0.3 ml O2/ml de sangre. El oxigeno disuelto físicamente en la sangre no basta para satisfacer las demandas de oxigeno del organismo (a FiO2 y presiones barométricas normales), El consumo de O2 en reposo de un adulto es cercano a 250 a 300 ml/O2/min.
- 28. TRANSPORTE DE OXIGENO ATRAVES DE LA SANGRE Si los tejidos pudieran eliminar los 0.3 ml de O2/100 ml de flujo sanguíneo que reciben, el gasto cardiaco tendría que ser más o menos 83.3 L/min. Durante el ejercicio la demanda de O2 puede aumentar incluso 16 veces, hasta 4 litros o más, en este caso el gasto cardiaco tendría que superar los 100 L/min. El gasto cardiaco máximo para adultos normales durante el ejercicio intenso esta entorno a los 25 L/min.
- 29. FISIOLOGIA DE LA HEMOGLOBINA La hemoglobina es una molécula compleja cuyo peso molecular aproximado es de 64,500. 141 aminoácidos 146 aminoácidos cada cadena se une a un grupo protorpofirina (hemo) cada una de las 4 cadena polipeptídicas puede ligar una molécula de oxigeno o de monóxido de carbono al átomo de hierro en el grupo hemo
- 30. FISIOLOGIA DE LA HEMOGLOBINA REACCION QUIMICA DEL OXIGENO Y DE LA HEMOGLOBINA La rápida combinación del oxigeno con la hemoglobina es reversible y es la reversibilidad de la reacción la que permite que el oxigeno sea liberado a los tejidos. La reacción es muy rápida con una semivida de 0.01 segundos o menos. Cada gramo de hemoglobina es susceptible de combinarse con cerca de 1.39 ml de oxigeno en condiciones optimas. Parte de la hemoglobina es una metahemoglobina (en la que el átomo de hierro esta en estado férrico) o se combina con monóxido de carbono, en cuyo caso no puede unirse al oxigeno.
- 31. REACCION QUIMICA DEL OXIGENO Y DE LA HEMOGLOBINA La capacidad de transporte de oxigeno de la hemoglobina es de 1.34 ml O2/g Hb. Una persona con 15 g Hb / 100 ml de sangre tiene una capacidad de transporte de oxigeno 20.1 ml O2/ 100 ml de sangre. La reacción de la hemoglobina con el oxigeno se expresa de manera convencional: Hb + O2 HbO2 FISIOLOGIA DE LA HEMOGLOBINA
- 32. INFLUENCIAS SOBRE LA CURVA DE DISOCIACION DE LA HEMOGLOBINA Una forma de expresar la proporción de hemoglobina se une al oxigeno, es el porcentaje de saturación, que es igual al contenido de oxigeno en la sangre, dividido entre la capacidad de trasporte de oxigeno de la hemoglobina en la sangre por 100%: % de saturación de Hb = O2 unido a Hb X 100 Capacidad de transporte de O2 de Hb Tanto el contenido como la capacidad, se expresa en milímetros de oxigeno por 100 ml de sangre. El % de saturación de la hemoglobina expresa solo un porcentaje y no una cantidad o volumen de oxigeno, de modo que el % de saturación no es intercambiable con contenido de oxigeno.
- 33. INFLUENCIAS SOBRE LA CURVA DE DISOCIACION DE LA HEMOGLOBINA La relación entre PO2 y la HbO2 no es lineal es una curva en forma de S, pronunciada para PO2 menores y casi plana cuando la PO2 rebasa los 70 mmHg. La razón de esto es que se trata de la representación de 4 reacciones, mas que de una sola, cada una de las 4 subunidades de la hemoglobina se puede combinar con una molécula de oxigeno: Hb4 + 4O2 Hb4O8
- 34. CARGA DE OXIGENO EN EL PULMON La sangre venosa mixta que entra en los capilares pulmonares tiene una PO2 aproximada de 40 mmHg. A una PO2 de 40 mmHg, la hemoglobina tiene una saturación de oxigeno cerca de 75%. Suponiendo que la concentración de hemoglobina en la sangre sea de 15 gr de Hb / 100 ml de sangre. Corresponde a 15.08 ml de O2 / 100 ml de sangre unida a hemoglobina mas 0.12 ml de O2 / 100 ml de sangre físicamente disuelta adicionales o un contenido total de oxigeno aproximado de 15.2 ml O2 / 100 de sangre. A medida que pasa por los capilares pulmonares se equilibra con la PO2 alveolar de unos mmHg. A una PO2 de 100 mmHg la saturación de oxigeno de la hemoglobina es de 97.4% INFLUENCIAS SOBRE LA CURVA DE DISOCIACION DE LA HEMOGLOBINA
- 35. DESCARGA DE OXIGENO EN LOS TEJIDOS La carga de PO2 de los capilares varia de un tejido a otro siendo muy baja en algunos (miocardio) y un elevada en otros (riñón). La curva de disociación de la oxihemoglobina es muy pronunciada en el intervalo de 40 a 10 mmHg. Un pequeño descenso en la PO2 puede provocar una importante disociación adicional de oxigeno y la hemoglobina, descargando mas oxigeno para ser utilizado en los tejidos. INFLUENCIAS SOBRE LA CURVA DE DISOCIACION DE LA HEMOGLOBINA
- 36. INFLUENCIAS EN LA CURVA DE DISOCIACION DE LA OXIHEMOGLOBINA El ph bajo la PCO2 alta y los niveles elevados de 2,3 BPG desvían la curva de disociación de la hemoglobina a la derecha, es decir: Para cualquier PO2 determinada hay menos oxigeno combinado a nivel químico con la hemoglobina a: Temperaturas altas, Ph bajos, PO2 altas Niveles elevados de 2,3 BPG.
- 37. INFLUENCIAS EN LA CURVA DE DISOCIACION DE LA OXIHEMOGLOBINA
- 38. INFLUENCIAS EN LA CURVA DE DISOCIACION DE LA OXIHEMOGLOBINA • La temperatura elevada desvían la curva a la derecha y las bajas a la izquierda. • A temperaturas sanguíneas muy bajas la afinidad de la hemoglobina por el oxigeno es tan elevada que este no se libera, ni siquiera a PO2S muy bajas • A temperaturas inferiores a la corporal normal el oxigeno es mas soluble en el agua que en el plasma a modo que a 20°C se disolverá en el plasma casi un 50% mas.
- 39. El 2,3 difosfoglicerato es producido por los eritrocitos durante su glucolisis normal y en los hematíes su concentración es bastante elevada (15 mmol/gr Hb). El 2,3 DPG se une a la hemoglobina en los eritrocitos reduciendo su afinidad por el oxigeno. Se produce mas en estados hipoxicos crónicos, desviando la curva a la derecha INFLUENCIAS EN LA CURVA DE DISOCIACION DE LA OXIHEMOGLOBINA
- 40. A medida que la sangre entra en tejidos con actividad metabólica, se expone a un ambiente que no es igual al del árbol arterial. La PCO2 es mas elevada, el Ph bajo, la temperatura es superior a la de la sangre arterial, el aumento de 2,3 DPG. DESVIAN LA CURVA DE DISOCIACION DE LA HEMOGLOBINA A LA DERCHA. Cuando la sangre venosa retorna al pulmón y el CO2 sale de la sangre (aumenta el Ph), la afinidad de la Hb por el oxigeno se incrementa, a medida que la curva se desvia a la izquierda. CONSECUENCIAS FISIOLOGICAS DE LOS EFECTOS DE LA TEMPERATURA, EL PH, LA PCO2, EL 2,3 DPG Se omitieron algunos factores importantes: La curva corresponde a: PCO2 40 mmhg, Ph 7.4, y temperatura de 37°C.
- 41. CONSECUENCIAS FISIOLOGICAS DE LOS EFECTOS DE LA TEMPERATURA, EL PH, LA PCO2, EL 2,3 DPG
- 42. OTROS FACTORES QUE AFECTAN EL TRASPORTE DE OXIGENO ANEMIA : Casi ninguna anemia afecta la curva de disociación, es la cantidad de hemoglobina lo que se reduce no el % ni la po2 arterial sin embargo el contenido arterial de oxigeno se disminuye, menor cantidad de hemoglobina reduce su capacidad para transportarla MONOXIDO DE CARBONO: Tiene una afinidad mucho mayor para la hemoglobina que el oxígeno, puede bloquear de manera efectiva la combinación del oxígeno con la hemoglobina porque el oxígeno no puede estar unido a átomos de hierro ya combinada con monóxido de carbono.
- 43. El monóxido de carbono es particularmente peligroso por varias razones. Una persona que respira concentraciones muy bajas de monóxido de carbono puede alcanzar lentamente niveles que amenazan la vida de carboxihemoglobina (COHb) en la sangre porque el monóxido de carbono tiene una alta afinidad por la hemoglobina. El efecto es acumulativo. Lo que es peor es que una persona respirar el monóxido de carbono no tiene conocimiento, el gas es incoloro, inodoro e insípido y no provoca ningún reflejo de tos o el estornudo, aumento de la ventilación, o sensación de dificultad para respirar. OTROS FACTORES QUE AFECTAN EL TRASPORTE DE OXIGENO
- 44. OTROS FACTORES QUE AFECTAN EL TRASPORTE DE OXIGENO OXIDO NITRICO: La hemoglobina dentro de los eritrocitos puede captar rápidamente el óxido nítrico (NO). El NO puede reaccionar con la oxihemoglobina para formar metahemoglobina y nitrato o reaccionar con desoxihemoglobina para formar un complejo de hemoglobina-óxido nítrico. Cuando la hemoglobina se une al oxígeno, la formación de este S-nitrosotiol se mejora; cuando la hemoglobina libera oxígeno, el óxido nítrico podría ser liberado. Por lo tanto, en las regiones donde la PO2 es baja, el NO un vasodilatador potente podría ser liberado.
- 45. METAHEMOGLOBINA HEMOGLOBINAS DIFERENTES A LA HBA MIOGLOBINA La mioglobina (Mb), una proteína hemo que se produce naturalmente en las células musculares, consta de una sola cadena de polipéptido unido a un grupo hemo. Por lo tanto, puede combinarse químicamente con una sola molécula de oxígeno y es estructuralmente similar a una sola subunidad de la hemoglobina. A menor PO2, mucho más oxígeno permanece unido a la mioglobina. Por lo tanto, la mioglobina puede actuar de transportador y almacenar oxígeno en el músculo esquelético. Cuando la sangre pasa a través del músculo, el oxígeno deja la hemoglobina y se la mioglobina. Puede ser liberado de la mioglobina cuando las condiciones hacen q descienda la PO2. OTROS FACTORES QUE AFECTAN EL TRASPORTE DE OXIGENO
- 46. SANGRE ARTIFICIAL Los fluorocarbonos pueden llegar a ser útiles como sustitutos de la sangre de emergencia, para las transfusiones, y para aumentar el transporte de la sangre en pacientes con anemia o durante la cirugía. CIANOSIS La cianosis realidad no es una influencia en el transporte de oxígeno, sino más bien es un signo de deficiencia en el transporte de oxígeno. La cianosis se produce cuando más de 5 g de Hb / ml de sangre arterial está en el estado desoxi. OTROS FACTORES QUE AFECTAN EL TRASPORTE DE OXIGENO
- 47. TRANSPORTE DE BIOXIDO DE CARBONO A TRAVES DE LA SANGRE El dióxido de carbono es 20 veces mas soluble en el plasma (y en el interior de los eritrocitos) que el oxigeno. De 5 a 10% del dióxido de carbono total transportado por la sangre se transporta en solución física. Cerca de 0.0006 ml de CO2 / mmHg PCO2 se disolverán en 1 ml de plasma 37°C, así que un centenar de mililitros de plasma o sangre entera a una PCO2 de 40 mmHg contienen cerca de 24 ml de CO2 en solución física.
- 48. COMPUESTO CARBAMILO El dióxido de carbono puede combinarse químicamente con los grupos amino terminales en proteínas de la sangre, formando compuestos carbamino. La reacción se produce rápidamente; no hay enzimas necesarias. Cuando se libera un ion de hidrógeno se forma un compuesto carbamino. Debido a que la proteína que se encuentra en mayor concentración en la sangre es la globina de la hemoglobina, la mayor parte del dióxido de carbono transportado de esta manera está unido a los aminoácidos de la hemoglobina ("carbaminohemoglobina").
- 49. BICARBONATO El restante 80% a 90% del dióxido de carbono transportado por la sangre se realiza en forma de ion bicarbonato. La hemoglobina también desempeña un papel integral en el transporte de dióxido de carbono, ya que puede aceptar el ion hidrógeno liberado por la disociación del ácido carbónico, lo que permite que la reacción continúe.
- 50. CURVA DE DISOCIACION DEL BIOXIDO DE CARBONO El contenido total de CO2 en sangre entera es de mas o menos 48 ml CO2 / 100 ml de sangre a 40 mmHg, de modo que un 5% del dióxido de carbono transportado en la sangre arterial esta en solución física. En el intervalo fisiológico normal de la PCO2s la curva es casi una línea recta, sin pendientes ni mesetas.
- 51. EXPLICACION DE LOS EFECTOS BOHR Y HALDANE EFECTO HALDANE La curva se desvía a la derecha a niveles superiores de oxihemoglobina y a la izquierda a niveles superiores de desoxihemoglobina. Esto permite que la sangre cargue mas dióxido de carbono en los tejidos donde hay mas desoxihemoglobina y libere mas dióxido de carbono en los pulmones donde hay mas oxihemoglobina.
- 52. EXPLICACION DE LOS EFECTOS BOHR Y HALDANE EFECTO BOHR Los iones de hidrógeno liberados por la disociación de ácido carbónico y la formación de compuestos carbaminos se unen a residuos de aminoácidos específicos en las cadenas de globina y facilitan la liberación de oxígeno de la hemoglobina.
- 53. EXPLICACION DE LOS EFECTOS BOHR Y HALDANE Se explican juntos porque la desoxihemoglobina es un acido mas débil que la oxihemoglobina, es decir la desoxihemoglobina acepta con mas facilidad el ion hidrogeno liberado por disociación del acido carbónico, permitiendo así que mas dióxido de carbono sea transportado en forma de ion bicarbonato: DESVIACION ISOHIDRICA. Por el contrario, la asociación de iones de hidrógeno con los aminoácidos de la hemoglobina reduce la afinidad de la hemoglobina por el oxígeno, desplazando por lo tanto la curva de disociación de oxihemoglobina a la derecha a valores de pH bajos o altos PCO2s.
- 54. EXPLICACION DE LOS EFECTOS BOHR Y HALDANE
- 55. EXPLICACION DE LOS EFECTOS BOHR Y HALDANE
Notes de l'éditeur
- Esto es volumen de gas por unidad de tiempo que se mueve a través de la barrera alveolocapilar es directamente proporcional al área de la barrera. La difusibilidad y la diferencia de concentración entre ambos lados, pero es inversamente proporcional al grosor de la barrera.
- Las moléculas ligeras se trasladan a mayor velocidad, tienen colisiones mas frecuentes y se difunden con mayor rapidez.
- 1 y 2 son propiedades físicas de la barrera: pueden modificarse por cambios en el volumen sanguíneo capilar pulmonar, el gasto cardiaco, la presión de la arteria pulmonar, cambios en el volumen pulmonar. 3 es determinante principal de la velocidad de difusión.
- Las reacciones de las cuatro subunidades de la hemoglobina con el oxigeno no parecen ocurrir de forma simultanea, se cree siguen una secuencia de 4 pasos (cooperación positiva).
- La influencia del PH y PCO2 en la curva de disociación de la hemoglobina se conoce como efecto Bohr Ph altos y PCO2 bajas la desvían a la izquierda (ambos efectos suelen presentarse juntos)
- La sangre almacenada en bancos de apenas una semana tiene concentraciones muy bajas de 2,3 DPG, de modo que la transfusión puede resultar en una disminución importante de la liberación de oxigeno en los tejidos.
- La P50 es la PO2 en la que 50% de la hemoglobina presente en la sangre está en el estado desoxihemoglobina y 50% está en el estado de la oxihemoglobina. A una temperatura de 37 °C, un pH de 7,4, y una PCO2 de 40 mm Hg, la sangre humana normal tiene una P50 de 26 o 27 mm Hg. Si la curva de disociación de oxihemoglobina se desplaza a la derecha, aumentara la P50. Si se desplaza a la izquierda, el P50 disminuye.
- Algunos investigadores han propuesto que este mecanismo desempeña un papel importante en la vasodilatación inducida por hipoxia o de eliminación de óxido nítrico que por la hemoglobina juega un papel en la vasoconstricción pulmonar hipóxica, pero esto aún no ha sido establecida.
- La metahemoglobina es la hemoglobina con hierro en estado férrico (Fe3 +). Puede ser causado por el envenenamiento por nitrito o por reacciones tóxicas para oxidante drogas, o se puede encontrar congénita en pacientes con átomos de hemoglobina M. hierro en el estado Fe3 + no se combinará con oxígeno. La mioglobina (Mb), una proteína hemo que se produce naturalmente en las células musculares, consta de una sola cadena de polipéptido unido a un grupo hemo. Por lo tanto, puede combinarse químicamente con una sola molécula de oxígeno y es estructuralmente similar a una sola subunidad de la hemoglobina.
- El oxígeno se puede unir de forma reversible a las emulsiones de fluorocarbonos. Aunque estas emulsiones de fluorocarbono NO tienen la capacidad de transporte de oxígeno casi tanto como lo hace la hemoglobina a PO2 normal, que pueden llevar significativamente más oxígeno que el plasma. CIANOSIS Su ausencia, sin embargo, no excluye la hipoxemia porque un paciente anémico con hipoxemia puede no tener suficiente hemoglobina para aparecer cianótico. Los pacientes con niveles anormalmente altos de hemoglobina en la sangre arterial, tales como aquellos con policitemia, pueden aparecer cianosis sin hipoxemia.
- En reposo el metabolismo histico de una persona de 70 kg produce 200 a 250 ml de dióxido de carbono por minuto, y deben ser transportados por la sangre venosa al pulmón para que se eliminen del organismo. Por lo tanto a un gasto cardiaco de 5 LTS/MIN cada 100 ml de sangre que pasa por los pulmones debe descargar de 4 a 5 ml de dióxido de carbono.
- Como la hemoglobina en la sangre venosa entra en el pulmón y se combina con oxígeno, se libera dióxido de carbono de sus grupos amina terminales. Cerca de 5% a 10% del contenido total de dióxido de carbono de la sangre se encuentra en la forma de compuestos carbamino.
- El dióxido de carbono puede combinarse con agua para formar ácido carbónico, que luego se disocia en un ion de hidrógeno y un ion bicarbonato. Muy poco de ácido carbónico se forma por la asociación de agua y dióxido de carbono sin la presencia de la enzima anhidrasa carbónica porque la reacción se produce muy lentamente. La anhidrasa carbónica, que está presente en alta concentración en los eritrocitos (pero no en el plasma), hace que la reacción proceda de aproximadamente 13.000 veces más rápido.
- En los tejidos, la PO2 es baja y la PCO2 es alta. El dióxido de carbono se disuelve en el plasma, y algunos se difunde en el eritrocito. Parte de este dióxido de carbono se disuelve en el citosol, algunas formas carbamino compuestos con la hemoglobina, y algunos se hidrata la anhidrasa carbónica para formar ácido carbónico. A baja PO2, hay cantidades sustanciales de desoxihemoglobina en los eritrocitos y la desoxihemoglobina es capaz de aceptar los iones de hidrógeno liberados por la disociación de ácido carbónico y la formación de compuestos carbamino. Los iones de hidrógeno liberados por la disociación de ácido carbónico y la formación de compuestos carbaminos se unen a residuos de aminoácidos específicos en las cadenas de globina y facilitan la liberación de oxígeno de la hemoglobina (el efecto Bohr). Los iones de bicarbonato se difunden fuera del eritrocito a través de la membrana de la célula mucho más fácilmente que los iones de hidrógeno. Debido a que más iones bicarbonato que los iones de hidrógeno salen de los eritrocitos, la neutralidad eléctrica es mantenida por el intercambio de iones cloruro para iones de bicarbonato por la proteína portadora de bicarbonato-cloruro. Este es el "cambio de cloruro." Pequeñas cantidades de agua también se mueven en la célula para mantener el equilibrio osmótico.
- En el pulmón, la PO2 es alta y la PCO2 es baja. Como el oxígeno se combina con la hemoglobina, los iones de hidrógeno que fueron tomadas cuando ella estaba en el estado deoxyhemoglobin son liberados. Se combinan con iones de bicarbonato, formando ácido carbónico. Esto se descompone en dióxido de carbono y agua. Al mismo tiempo, el dióxido de carbono también se libera de los compuestos carbaminos. El dióxido de carbono se difunde fuera de las células rojas de la sangre y el plasma y en los alvéolos. Un cambio opuesto cloruro en dirección a la de los tejidos también se produce para mantener la neutralidad eléctrica.
