Laboratorio 6
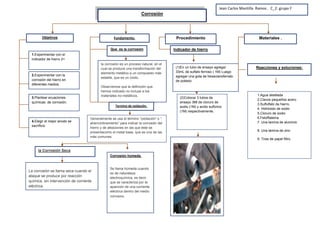
- 1. Corrosión Objetivos ProcedimientoFundamento. Materiales . 2.Experimentar con la corrosión del hierro en diferentes medios. 3.Plantear ecuaciones químicas de corrosión. 4.Elegir el mejor anodo se sacrificio Que es la corrosión la corrosión es un proceso natural, en el cual se produce una transformación del elemento metálico a un compuesto más estable, que es un óxido. Observemos que la definición que hemos indicado no incluye a los materiales no-metálicos. Indicador de hierro (1)En un tubo de ensayo agregar 33mL de sulfato ferroso ( 1M) Luego agregar una gota de hexacianoferrato de potasio Jean Carlos Mantilla Ramos . C_2: grupo F 1.Experimentar con el indicador de hierro 2+ Corrosión húmeda. Se llama húmeda cuando es de naturaleza electroquímica, es decir que se caracteriza por la aparición de una corriente eléctrica dentro del medio corrosivo. La corrosión se llama seca cuando el ataque se produce por reacción química, sin intervención de corriente eléctrica. Termino de oxidación. Generalmente se usa el término “oxidación” o “ aherrumbramiento” para indicar la corrosión del hierro y de aleaciones en las que éste se presentacomo el metal base, que es una de las más comunes. Reacciones y soluciones: 1.Agua destilada 2.Clavos pequeños acero 3.Sulfulfato de hierro. 4. Hidróxido de sodio 5.Cloruro de sodio 6.Felolftaleina. 7. Una lamina de aluminio 8. Una lámina de zinc 9. Tiras de papel filtro. (2)Colocar 3 tubos de ensayo 3Ml de cloruro de sodio (1M) y acido sulfúrico (1M) respectivamente. la Corrosión Seca
