Segunda ley de la termodinamica
- 1. UNIVERSIDAD NACIONAL DE INGENIRIA FACULTAD DE INGENIERIA INDUSTRIAL Y DE SISTEMAS Curso: FISICA I CB 302U 2010 II Profesor: Lic. JOAQUIN SALCEDO jmst5060@gmail.com Tema: Segunda ley Tipler-Mosca, Sears - Semansky, Serway, Benson, Lea - Burke, Ohanian - Markert http://www.sc.ehu.es/sbweb/fisica 1
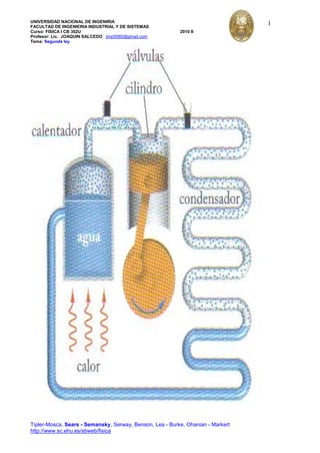
- 2. UNIVERSIDAD NACIONAL DE INGENIRIA FACULTAD DE INGENIERIA INDUSTRIAL Y DE SISTEMAS Curso: FISICA I CB 302U 2010 II Profesor: Lic. JOAQUIN SALCEDO jmst5060@gmail.com Tema: Segunda ley Tipler-Mosca, Sears - Semansky, Serway, Benson, Lea - Burke, Ohanian - Markert http://www.sc.ehu.es/sbweb/fisica 2 Máquina térmica mt Es un dispositivo que transforma calor en trabajo mecánico. Ejemplos: máquina a vapor, motor a gasolina o petróleo,….. Nos ocupamos de las que operan en ciclo repetitivo Sin especificar detalles podemos hacer afirmaciones generales Usamos el esquema de una mt que opera entre dos depósitos uno caliente Tc y otro frío Tf. En cada ciclo la máquina absorbe calor de un deposito caliente Tc, parte de ese calor sirve para realizar trabajo W En un ciclo completo. El cambio de energía interna es nulo. Y el trabajo hecho por la mt es igual al calor neto que fluye hacia ella. 0 neto C FU W Q Q Q En un diagrama PV es el área encerrada
- 3. UNIVERSIDAD NACIONAL DE INGENIRIA FACULTAD DE INGENIERIA INDUSTRIAL Y DE SISTEMAS Curso: FISICA I CB 302U 2010 II Profesor: Lic. JOAQUIN SALCEDO jmst5060@gmail.com Tema: Segunda ley Tipler-Mosca, Sears - Semansky, Serway, Benson, Lea - Burke, Ohanian - Markert http://www.sc.ehu.es/sbweb/fisica 3 Eficiencia de una máquina térmica Es la razón lo de se consigue y a que precio. 1C F F mt C C C Q Q Qconsigo W precio Q Q Q Enunciados de la 2da ley Es imposible que todo el calor del deposito caliente se transforme en trabajo La eficiencia debe ser menor que uno. El calor perdido no puede ser nulo … Un motor a gasolina de un camión toma 10,000 J de calor y produce 2000 J de trabajo mecánico por ciclo. El calor se obtiene quemando gasolina, cuyo calor de combustión es Lc = 5.0 X 104 J/g. a) Calcule la eficiencia térmica del motor b) ¿Cuánto calor se desecha en cada ciclo? c) ¿Cuánta gasolina se quema en cada ciclo? d) Si el motor ejecuta 25 ciclos por segundo, ¿qué potencia desarrolla en watts y en hp? e) ¿Cuánta gasolina se quema por segundo? ¿Por hora? a) 2000 0.2 10000c W Q b) 8000c f fW Q Q Q J c) 4 10000 0.2 5 10 / c c c c Q Q mL m g L x J g d) 2000 (25 ) 50 1 50000 67 746 J ciclos P kW ciclo s hp W hp W e) 0.2 (25 ) 5 3600 5 ( ) 18000 18 1 g ciclos g ciclo s s g s g kg s h h h Procesos reversibles e irreversibles. Un proceso reversible es uno que puede efectuarse de manera tal que, a su conclusión, tanto el sistema como sus alrededores, hayan regresado a sus condiciones iniciales exactas. Todos los procesos naturales son irreversibles. …. Algunos son casi reversibles.
- 4. UNIVERSIDAD NACIONAL DE INGENIRIA FACULTAD DE INGENIERIA INDUSTRIAL Y DE SISTEMAS Curso: FISICA I CB 302U 2010 II Profesor: Lic. JOAQUIN SALCEDO jmst5060@gmail.com Tema: Segunda ley Tipler-Mosca, Sears - Semansky, Serway, Benson, Lea - Burke, Ohanian - Markert http://www.sc.ehu.es/sbweb/fisica 4 Si un proceso real ocurre muy lentamente, de manera que el sistema siempre este virtualmente en equilibrio. Ejemplo un gas se comprime depositando algunos granos de arena sobre un embolo sin fricción. Una característica general de un proceso reversible es que es posible que no haya efectos disipativos, como turbulencia o fricción, que conviertan la energía mecánica en energía térmica. La máquina de Carnot. En 1824 Sadi Carnot describió una máquina teórica que es fundamental en comparación de rendimientos como cota superior. El ciclo consta de: 1 Expansión isotérmica a temperatura caliente Tc a b 2. Expansión adiabática b c 3. Compresión isotérmica a temperatura fría Tf c d 4. Compresión adiabática d a
- 5. UNIVERSIDAD NACIONAL DE INGENIRIA FACULTAD DE INGENIERIA INDUSTRIAL Y DE SISTEMAS Curso: FISICA I CB 302U 2010 II Profesor: Lic. JOAQUIN SALCEDO jmst5060@gmail.com Tema: Segunda ley Tipler-Mosca, Sears - Semansky, Serway, Benson, Lea - Burke, Ohanian - Markert http://www.sc.ehu.es/sbweb/fisica 5 Hallar la eficiencia del ciclo de Carnot El calor de entrada 1C F F Carnot C C C Q Q QW Q Q Q (*) ln B C AB C A V Q W nRT V El calor de salida ln C F CD F D V Q W nRT V La razón de los calores ln ln ln ln C C F F F D D B BC C C A A V V nRT T Q V V V VQ nRT T V V
- 6. UNIVERSIDAD NACIONAL DE INGENIRIA FACULTAD DE INGENIERIA INDUSTRIAL Y DE SISTEMAS Curso: FISICA I CB 302U 2010 II Profesor: Lic. JOAQUIN SALCEDO jmst5060@gmail.com Tema: Segunda ley Tipler-Mosca, Sears - Semansky, Serway, Benson, Lea - Burke, Ohanian - Markert http://www.sc.ehu.es/sbweb/fisica 6 Ejercicio verifica que C B D A V V V V Tomando logaritmos ln lnA D B C V V V V Aplicando (*) 1 F Carnot C T T Conclusiones. Todas las máquinas de Carnot que operan de modo reversible entre las mismas temperaturas tienen la misma eficiencia. La eficiencia de cualquier maquina reversible que opera entre dos temperaturas es mayor que la eficiencia de cualquier maquina real que opere entre dichas temperaturas. Demostración: la razón de los volúmenes de expansión y compresión son iguales C B D A V V V V BC y AD son adiabáticos En los procesos adiabáticos 1 PV cte TV cte En BC 1 1 C B F CT V T V En AD 1 1 C A F DT V T V Haciendo la razón . 1 1 1 1 1 1 1 1 C A F D A D A D C B F C B C B C T V T V V V V V T V T V V V V V * Una máquina de vapor opera entre 27ºC y 227ºC a) ¿cuál es la eficiencia térmica máxima? b) Halle el trabajo máximo que la máquina puede efectuar en cada ciclo si absorbe 200J La máxima eficiencia esta dada por Carnot.
- 7. UNIVERSIDAD NACIONAL DE INGENIRIA FACULTAD DE INGENIERIA INDUSTRIAL Y DE SISTEMAS Curso: FISICA I CB 302U 2010 II Profesor: Lic. JOAQUIN SALCEDO jmst5060@gmail.com Tema: Segunda ley Tipler-Mosca, Sears - Semansky, Serway, Benson, Lea - Burke, Ohanian - Markert http://www.sc.ehu.es/sbweb/fisica 7 ) 27 273 300 227 273 500 300 1 0 0,41 50 F c F Carnot C a T T T T ) 0,4 0 0 2 8 0 mt C W W W Q Jb *Una máquina de Carnot toma 2000 J de calor de un depósito a 500 K, realiza trabajo, y desecha calor a un depósito a 350 K. ¿Cuánto cuánto calor expulsa, cuánto trabajo efectúa, y qué eficiencia tiene? 1 1 1400F F F C F C C C C Q T T Q Q J Q T T 2000 1400 600C FW Q Q J 350 1 1 0.3 500 F C C T T *Suponga que 0.2 mol de un gas diatómico con comportamiento ideal ( 1.4 ) efectúa un ciclo de Carnot con temperaturas de 227°C y 27°C. La presión inicial es 5 10 10 Paap x y, durante la expansión isotérmica a la temperatura superior, el volumen se duplica a) Calcule la presión y el volumen en los puntos a, b, c y d del diagrama PV b) Calcule , ,Q W U para cada paso y para el ciclo c) Halle la eficiencia de dos maneras diferentes a) 4 3 5 4 3 5 4 3 5 4 3 5 8.31 10 10 10 16.6 10 5 10 59.6 10 0.84 10 29.8 10 1.67 10 a a a b b a c c a d d a V x m p x P V x m p x P V x m p x P V x m p x P b) PROCESO Q W U ab 576J 576J O b c O 832J -832J c d -346 J -346 J O d a O -832 J 832 J Total 230J 230J O c) 0.4 1 f c c TW Q T
- 8. UNIVERSIDAD NACIONAL DE INGENIRIA FACULTAD DE INGENIERIA INDUSTRIAL Y DE SISTEMAS Curso: FISICA I CB 302U 2010 II Profesor: Lic. JOAQUIN SALCEDO jmst5060@gmail.com Tema: Segunda ley Tipler-Mosca, Sears - Semansky, Serway, Benson, Lea - Burke, Ohanian - Markert http://www.sc.ehu.es/sbweb/fisica 8 Refrigeradores y bombas de calor. Son mt al revés. Se invierte el diagrama anterior Para estos en lugar eficiencia se usa el coeficiente de rendimiento CdR Un refrigerador absorbe calor del depósito frío gracias al trabajo sobre ella F refri Qconsigo CdR precio W Una bomba calienta el foco caliente necesitando trabajo. C bom Qconsigo CdR precio W Si el ciclo descrito se efectúa hacia atrás como refrigerador Halla el coeficiente de rendimiento de dos maneras 346 1.5 230 300 1.5 500 300 f f c f Q CdR W T CdR T T
- 9. UNIVERSIDAD NACIONAL DE INGENIRIA FACULTAD DE INGENIERIA INDUSTRIAL Y DE SISTEMAS Curso: FISICA I CB 302U 2010 II Profesor: Lic. JOAQUIN SALCEDO jmst5060@gmail.com Tema: Segunda ley Tipler-Mosca, Sears - Semansky, Serway, Benson, Lea - Burke, Ohanian - Markert http://www.sc.ehu.es/sbweb/fisica 9 *Halle la eficiencia térmica de una máquina que opera n moles de gas ideal diatómico en el ciclo 1 2 3 4 1 0 0 0 2 0 3 2 v p H 12 23 v 2 0 p 2 0 0 0 0 0 0 0 0 0 H p V T =2T T =4T 5 7 C C 2 2 19 Q =Q +Q =nC (T -T )+nC (T -T )= p V 2 W=(2p -p )(2V -V )=p V 2 10.5% Q 19 nRT R R W e
- 10. UNIVERSIDAD NACIONAL DE INGENIRIA FACULTAD DE INGENIERIA INDUSTRIAL Y DE SISTEMAS Curso: FISICA I CB 302U 2010 II Profesor: Lic. JOAQUIN SALCEDO jmst5060@gmail.com Tema: Segunda ley Tipler-Mosca, Sears - Semansky, Serway, Benson, Lea - Burke, Ohanian - Markert http://www.sc.ehu.es/sbweb/fisica 10 Motores térmicos más conocidos OTTO Describa el ciclo y halle su eficiencia, identifique máquinas reales relacionadas 1 1 1 r DIESSEL Describa el ciclo y halle su eficiencia, identifique máquinas reales relacionadas
- 11. UNIVERSIDAD NACIONAL DE INGENIRIA FACULTAD DE INGENIERIA INDUSTRIAL Y DE SISTEMAS Curso: FISICA I CB 302U 2010 II Profesor: Lic. JOAQUIN SALCEDO jmst5060@gmail.com Tema: Segunda ley Tipler-Mosca, Sears - Semansky, Serway, Benson, Lea - Burke, Ohanian - Markert http://www.sc.ehu.es/sbweb/fisica 11 STIRLING Describa el ciclo y halle su eficiencia, identifique máquinas reales relacionadas Entropía Es una función de estado relacionada con la segunda ley. A nivel macroscópico (Rudolf Clausius) Sea un proceso infinitesimal en un sistema entre dos estados de equilibrio. Si dQr, es la cantidad de energía térmica que se transferiría si el sistema hubiera seguido una trayectoria reversible, entonces el cambio de entropía dS, independiente de la trayectoria real seguida, es igual a la cantidad de energía térmica transferida a lo largo de la trayectoria reversible dividida entre la temperatura del sistema. rdQ dS T Mas enunciados de la segunda ley. Los sistemas aislados tienden al desorden, y la entropía es una medida de dicho desorden. La entropía del sistema aumenta en todos los procesos. Para un proceso finito. f f i i dQ S ds T (trayectoria reversible) El cambio de entropía de un sistema solo depende solo de las propiedades del estado de equilibrio inicial y final 2da ley sin referencia a dispositivo o proceso, en función de una variable de estado
- 12. UNIVERSIDAD NACIONAL DE INGENIRIA FACULTAD DE INGENIERIA INDUSTRIAL Y DE SISTEMAS Curso: FISICA I CB 302U 2010 II Profesor: Lic. JOAQUIN SALCEDO jmst5060@gmail.com Tema: Segunda ley Tipler-Mosca, Sears - Semansky, Serway, Benson, Lea - Burke, Ohanian - Markert http://www.sc.ehu.es/sbweb/fisica 12 Un sistema en un estado de equilibrio puede caracterizarse por los valores que toman sus variables de estado: P,V,T,n,U … El cambio de las variables tras un ciclo completo es iguala cero. El sistema vuelve a su estado inicial. 0, 0, 0, 0T U P V Las variables Q y W no son variables de estado En general en un ciclo 0, 0Q W Nueva variable de estado: la entropía Un sistema a temperatura T experimenta un proceso infinitesimal en el que absorbe reversiblemente una cantidad de calor dQ Def. El cambio de entropía f i dQ dQ dS S Sf Si T T La suma infinitesimal se evalúa para un proceso reversible que conecte los dos extremos Se puede usar cualquier camino reversible (similar conservativoF ) Hallar la relación entre temperatura y calor en un ciclo de Carnot 1 , 1F F Carno CC F C C t FQ T T TQ T Q Q Demostrar para un ciclo reversible (Carnot) 0S 0 f CF i F C QQdQ S T T T Un ciclo reversible cualquiera puede representarse mediante un conjunto de ciclos de Carnot
- 13. UNIVERSIDAD NACIONAL DE INGENIRIA FACULTAD DE INGENIERIA INDUSTRIAL Y DE SISTEMAS Curso: FISICA I CB 302U 2010 II Profesor: Lic. JOAQUIN SALCEDO jmst5060@gmail.com Tema: Segunda ley Tipler-Mosca, Sears - Semansky, Serway, Benson, Lea - Burke, Ohanian - Markert http://www.sc.ehu.es/sbweb/fisica 13 Solo depende de los estados inicial y final. Un proceso puede ser reversible o irreversible, cuasiestático o explosivo Para los cálculos imagina un proceso reversible. ?S en varios casos Cambio de fase. Un cubo de hielo de 0.12kg a 0ºC se coloca en un recipiente con agua a 0ºC, se agita de modo que la temperatura no cambia Imaginamos una fuente cuya temperatura sea insignificativamente mayor que la del hielo 3 0.12(0.33 40.5) 40.2 10 273 2 147 f kJQ mL Q x S J KT Cambio de temperatura Si 1 kg. de agua se calienta de 10 a 95 ºC a presión atmosférica. Imagina una serie de fuentes T+dT y proceso reversible. edQ mc dT 368 1(4.2) 1100 283 f f f e ei i i TdQ dT J S mc mc ln ln T T T K Cambio de volumen N moles de un gas ideal se encuentra a temperatura T ocupando un volumen V1 y experimenta una expansión libre hasta un volumen V2. Imagine un proceso reversible. 0dQ dU dW pdV dQ pdV nRT dV dV nR T T V T V f f f i i i VdQ dV S nR nRln T V V En un expansión libre la entropía aumenta
- 14. UNIVERSIDAD NACIONAL DE INGENIRIA FACULTAD DE INGENIERIA INDUSTRIAL Y DE SISTEMAS Curso: FISICA I CB 302U 2010 II Profesor: Lic. JOAQUIN SALCEDO jmst5060@gmail.com Tema: Segunda ley Tipler-Mosca, Sears - Semansky, Serway, Benson, Lea - Burke, Ohanian - Markert http://www.sc.ehu.es/sbweb/fisica 14 Entropía en una mezcla *0.3kg de agua a 90ºC y 0.7kg a10ºC se mezclan en un recipiente aislado Hallamos la temperatura de equilibrio. 1 2 1 2 0.3 (90 ) 0.7 ( 10) 34 307 307 0.3(4.2) 210 363 307 0.7(4.2) 240 283 30 / p p f f f p pi i i f p i c T c T T C K TdQ dT J S mc mc ln ln T T T K T J S mc ln ln T K S S S J K Observe que la entropía de una parte puede disminuir. La entropía en las mezclas aumenta La entropía y la segunda ley Un sistema y su entorno (parte relevante) constituyen el universo universo sistema alrededorS S S En todos los cálculos se halla que la entropía del universo aumenta o permanece constante Segunda ley: En cualquier proceso la entropía de universo aumenta (irreversible) o permanece constante (reversible) 0universoS El calor fluye irreversiblemente desde temperaturas más altas a mas bajas La “dirección del tiempo” apunta en la dirección en que la entropía aumenta Según la entropía aumenta hay menos trabajo disponible. El aumento de entropía corresponde a aumentar desorden Muerte térmica del universo …. En verdad les digo que el adiós no existe: si se pronuncia entre dos seres que nunca se encontraron, es una palabra innecesaria; si se dice entre dos seres que fueron uno, es una palabra sin sentido Khalil Gibran “El Profeta”