Reticolo golgi secrezione 2012
- 2. Le proteine mitocondriali sono importate: nella matrice nello spazio intermembrana. grazie a segnali di indirizzamento, posti nella porzione amino- terminale. Nella matrice: il peptide segnale si lega ad un recettore sulla membrana mitocondriale esterna e la proteina viene traslocata grazie alla presenza di un secondo traslocatore sulla membrana interna: si crea un punto di contatto tra le due membrane. Le proteine sono traslocate “non ripiegate”. Intervengono in questo processo le proteine chaperonine, come hsp70, che mantengono le proteine srotolate. L’idrolisi dell’ATP viene usata per staccare l’hsp70 e fornire energia motrice per importare la proteina attraverso il traslocatore.
- 3. Organizzazione dei mitocondri Sequenza segnale per l’importazione di proteine mitocondriali
- 4. Tre proteine traslocatrici mitocondriali
- 5. Importazione di proteine nei mitocondri, la sequenza segnale è riconosciuta dalla proteina TOM.
- 6. Ruolo dell’energia nell’importazione di proteine nella matrice mitocondriale 1) La proteina hsp70 citosolica attaccata è rilasciata dalla proteina in un passaggio che Diprende Dall’idrolisi di ATP 2) Traslocazione nella matrice grazie ad un gradiente protonico 3) l’hsp mitocondriale si lega alla catena polipetidica in regioni strategiche trascinandola Nella Matrice ed è poi rimossa grazie ad idrolisi di ATP
- 7. La traslocazio ne delle proteine nella membrana mitocondria le interna e nello spazio intermembr ana richiede: la sequenza segnale una sequenza di aa idrofobica dopo il peptide segnale, che funziona da nuovo peptide segnale quando il primo è stato tagliato via dalla peptidasi (meccanismo simile alla traslocazione nell’ER)
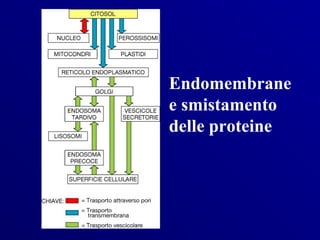
- 8. Endomembrane della cellula eucariotica
- 9. Membrane biologiche e loro interazioni
- 10. Nucleo Poro Nucleare RE
- 14. Meccanismo di trasporto attivo attraverso i pori nucleari
- 15. Traffico di Materiale attraverso I Pori Nucleari
- 16. Reticolo Endoplasmatico
- 20. LE MEMBRANE DEL SER STBILISCONO CON GRANDE EFFICIENZA GRADIENTI DI CA++ CHE SVOLGONO UN RUOLO DECISIVO NELLA TRASDUZIONE DEI SEGNALI NELLO STIMOLO NERVOSO E NELLA CONTRAZIONE MUSCOLARE
- 21. IL SER E’ RESPONSABILE DELLA SINTESI DI TRIACILGLICEROLI CHE VENGONO ACCUMULATI NEL LUME, CON PRODUZIONE DI GOCCIOLINE LIPIDICHE. NEGLI ADIPOCITI LE GOCCIOLINE LIPIDICHE OCCUPANO QUASI TUTTO LO SPAZIO DEL CITOPLASMA
- 22. IL SER PARTECIPA ALLA SINTESI DI STEROLI COME IL COLESTEROLO IL COLESTEROLO VIENE SINTETIZZATO ATTRAVERSO UNA VIA METABOLICA A PIU’ STADI ALLA QUALE PARTECIPANO ANCHE ENZIMI PRESENTI NEL CITOSOL, OLTRE A QUELLI DEL SER
- 23. LA SPECIE UMANA SINTETIZZA UNA GRAN PARTE DEL SUO COLESTEROLO TUTTE LE CELLULE SONO CAPACI DI PRODURLO, MA LA MAGGIOR PARTE DI ESSO VIENE SINTETIZZATO DALLE CELLULE EPATICHE IL FEGATO UTILIZZA IL COLESTEROLO PER FORMARE GLI ACIDI BILIARI
- 24. NELLA CORTECCIA SURRENALE E NELLE GONADI (REGIONE INTERSTIZIALE DEL TESTICOLO) IL COLESTEROLO E’ UTILIZZATO NELLA PRODUZIONE DEGLI ORMONI STEROIDEI
- 25. IL SER INTERVIENE NEL PRODUZIONE DEGLI ORMONI STEROIDEI NEI MITOCONDRI VIENE SCISSA LA CATENA LATERALE DEL COLESTEROLO, IMPORTATO DAL CITOSOL IL PRODOTTO COSI’ FORMATO LASCIA I MITOCONDRI E PASSA NEL SER DOVE VIENE DI NUOVO MODIFICATO. INFINE, TALE PRODOTTO DAL SER TORNA DI NUOVO NEI MITOCONDRI PER LE M0DIFICAZIONI FINALI COSI’ QUESTI DUE ORGANELLI GIOCANO UNA SORTA DI “PALLA A VOLO” PER PRODURRE L’ORMONE STEROIDEO
- 26. IL SER SINTETIZZA I FOSFOLIPIDI DELLE MEMBRANE CELLULARI IL FOSFOLIPIDE PRINCIPALE PRODOTTO E’ FOSFATIDILCOLINA O LECITINA PUO’ ESSERE FORMATO IN TRE PASSAGGI DA COLINA, DUE ACIDI GRASSI E GLICEROLO FOSFATO
- 28. IL SER CONTIENE UN ENZIMA GLUCOSIO-6-FOSFATASI G6Pase ESSENZIALE PER L’OMEOSTASI DEL GLUCOSIO NEL SANGUE, L’ENZIMA E’ PRESENTE SOLO NELLE CELLULE PARENCHIMALI DEL FEGATO
- 29. LA DETOSSIFICAZIONE E’ SVOLTA DA UN SISTEMA DI ENZIMI CHE TRASFERISCONO L’OSSIGENO (MONOSSIGENASI) E IL CUI COMPONENTE PRINCIPALE E’ IL CITOCROMO P-450 IL SISTEMA DELLE MONOSSIGENASI P-450 E’ FORMATO DA NUMEROSI ISOENZIMI (50- 100) DEL CITOCROMO P-450 (EMO-PROTEINA DI TIPO b), DA UNA SINGOLA REDUTTASI E FOSFOLIPIDE.
- 30. QUESTI ENZIMI SONO PROTEINE INTEGRALI DI MEMBRANA E SONO PREMINENTI NEL SER, MA PRESENTI ANCHE NEI MITOCONDRI IL CITOCROMO P-450 E’ UBIQUITARIO, MA SI TROVA IN CONCENTRAZIONI MOLTO ELEVATE NEL SER DELLE CELLULE EPATICHE RAPPRESENTA CIRCA IL 20% DELLE PROTEINE DEL ER E IL 2-3% DELLE PROTEINE TOTALI DELLA CELLULA
- 32. QUESTI ENZIMI SONO CAPACI DI OSSIDARE MIGLIAIA DI COMPOSTI IDROFOBICI DIFFERENTI CHE CONVERTONO IN DERIVATI PIU’ IDROFILICI E, QUINDI, PIU’ FACILMENTE SECRETI I SUBSTRATI DI TALI ENZIMI SONO IN GRADO DI INDURRE PROLIFERAZIONE DEL SER E CONSEGUENTE AUMENTO DELL’ATTIVITA’ DEGLI ENZIMI
- 33. SONNIFERI A BASE DI FENOBARBITAL (C OSI’ COME CENTINAIA DI ALTRE SOSTANZE CHIMICHE) INDUCONO PROLIFERAZIONE DEL SER E AUMENTO DELL’ATTIVITA’ DELLE MONOSSIDASI NELLE CELLULE EPATICHE IL CONSEGUENTE AUMENTO DELLA CAPACITA’ DI DEGRADARE IL FENOBARBITAL SPIEGA PER QUALE MOTIVO I CONSUMATORI DI SONNIFERO DEVONO ASSUMERNE DOSI SEMPRE PIU’ ELEVATE
- 34. PERTANTO L’ASSUNZIONE CRONICA DI FENOBARBITAL (O ALTRE SOSTANZE) AUMENTA L’EFFICIENZA DI DEGRADAZIONE, DA PARTE DEL FEGATO, DI MOLTI ALTRI FARMACI, TRA CUI SOSTANZE TERAPEUTICAMENTE UTILI, COME ANTIBIOTICI, STEROIDI, ANTICOAGULANTI E NARCOTICI COMUNQUE L’AUMENTATO SVILUPPO DEL SER NON COMPORTA AUMENTO EQUIVALENTE DI TUTTI GLI ENZIMI
- 35. MENTRE L’AZIONE DEL COMPLESSO P-450 E’ NEL COMPLESSO FAVOREVOLE DAL PUNTO DI VISTA FISIOLOGICO, CERTI EVENTI METABOLICI BASATI SUL P- 450 POSSONO PORTARE A SERIE PATOLOGIE
- 36. RETICOLO ENDOPLASMA TICO RUGOSO RER
- 38. Sintesi di proteine a livello del RER
- 39. Sintesi proteica a livello del Reticolo endoplasmatico rugoso
- 40. Modalità di inserzione di una proteina nel bilayer fosfolipidico del RER
- 41. Modalità di inserzione di una proteina nel bilayer fosfolipidico del RER
- 42. Conclusione: Le modalità di inserzione delle proteine nei bilayer fosfolipidici vengono già definite nel RER.
- 43. Glicosilazione a livello del RER
- 45. Membrane biologiche e loro interazioni
- 47. Il percorso delle proteine destinate alla secrezione
- 50. Vescicole di trasporto e proteine associate
- 52. Meccanismo usato per trattenere le proteine residenti nel RER
- 54. Compartimenta lizzazione funzionale del Golgi
- 55. Elementi di Transizione e del reticolo cis del Golgi
- 57. Trasporto selettivo mediato da vescicole rivestite
- 58. Modello del meccanismo di approdo delle vescicole di trasporto
- 59. Fusione di vescicole di trasporto
- 61. Ruolo delle proteine di fusione nell’internalizzazione di virus
- 63. Modello di recupero per proteine residenti nell’ER
- 64. I lisosomi: punti di incontro ove convergono le sostanze che devono Lisosoma essere digerite. Enzimi lisosomali: idrolasi lisosomali Vie per arrivare al lisosoma: Autofagia (ER si trasforma in lisosoma) Fagocitosi Endosoma precoci e tardivi Alcune proteine sono trasportate nel lisosoma direttamente con l’uso di un segnale lisosomale: KFERQ (Lys, Phe, Glut, Arg, glutammina)
- 65. Le idrolasi lisosomiali sono caratterizzate dalla presenza di un gruppo specifico, il mannosio-6-fosfato (M6P), che serve a farle riconoscere da un recettore specifico presente sul trans-Golgi. L’M6P è aggiunto agli oligosaccaridi legati all’asparagina, nel reticolo cis del Golgi. Il recettore è una proteina transmembrana localizzata sul trans Golgi. L’unione con l’idrolasi inizia la formazione di vescicole e si verifica a pH 7. Le idrolasi si dissociano dai recettori negli endosomi tardivi a pH 6. I recettori sono riciclati verso il trans Golgi.
- 67. Riconoscimento di una idrolasi lisosomale
- 68. Trasporto di idrolasi lisosomali di nuova sintesi ai lisosomi
- 69. Tre vie di degradazione dei lisosomi
- 70. Malattie da accumulo lisosomale: le idrolasi lisosomali sono alterate per difetti genetici recessivi. Malattia di Hurler I-cell disease I substrati delle idrolasi si accumulano non digeriti nel lisosomi, per cui si formano inclusioni nelle cellule. Le idrolasi alterate sfuggono ai lisosomi, sono secrete dalla via di default e si accumulano nel sangue: il difetto è dovuto alla mancanza o al difetto di una fosfotransferasi GlcNAc. Le idrolasi sono secrete. Non funziona la via di scavenger (raccolta dei rifiuti) di endocitosi e si accumulano. Nel fegato via alternativa.
- 71. Endocitosi: Dalla superficie cellulare verso i lisosomi. Fagocitosi di grandi particelle (250 nm) svolta da cellule specializzate tramite fagosomi. Le particelle si devono legare ai fagociti: recettori attivati scatenano la risposta . Normalmente sono gli anticorpi che riconoscono le particelle estranee e le presentano ai fagociti. Proteine Fc o complemento.
- 72. Fagocitosi da parte di un macrofago di due globuli rossi chimicamente alterati Frecce rosse = pseudopodi
- 73. Fosse rivestite di clatrina: 2% dell’area di membrana La clatrina forma un cesto o una gabbia sotto la membrana e dà origine ad una vescicola rivestita di clatrina: è un processo rapido e continuo in molti tipi cellulari. Le vescicole si fondono poi negli endosomi precoci. Servono per l’endocitosi in fase fluida e per l’assunzione di specifiche macromolecole dall’esterno. Questo processo è chiamato endocitosi mediata da recettori: processo selettivo che permette di assumere grandi quantità di macromolecole. Es. trasporto del colesterolo. Le cellule assumono colesterolo che serve per assemblare le membrane. Se si blocca l’assunzione, il colesterolo si accumula nel sangue e può formare placche aterosclerotiche. Il colesterolo è trasportato nel sangue associato a proteine LDL (lipoproteine a basse densità).
- 75. Ogni LDL contiene 1500 mol colesterolo esterificato ad acidi grassi
- 76. Le cellule presentano dei recettori per le LDL, che si associano alle zone di membrana ricche in clatrina. L’LDL si lega al recettore e si formano vescicole rivestite che sono internalizzate. Le vescicole perdono il rivestimento in clatrina e si fondono negli endosomi precoci. Le LDL sono portate agli endosomi tardivi ed ai lisosomi, dove gli esteri di colesterolo sono idrolizzati ed il colesterolo liberato per l’incorporazione nelle membrane. Se c’è troppo colesterolo, viene spenta la sintesi di colesterolo e anche di recettori per LDL, per non importarlo più e così il colesterolo si accumula nel sangue. Geni difettosi per le LDL: mancata assunzione del colesterolo, aterosclerosi in età giovanile.
- 81. Recettori delle LDL normali e mutanti
- 82. I recettori per le LDL sono riciclati dagli endosomi e riportati in membrana per essere riutilizzato.
- 83. Deposito di proteine della membrana plasmatica in endosomi riciclati
- 85. Endocitosi di LDL mediata da recettori
- 86. Endocitosi mediata da recettori
- 87. Le vie meglio conosciute di smistamento delle proteine nel reticolo trans del Golgi
- 88. Vie di endocitosi costitutiva e regolata
- 89. Compartimenti intracellulari coinvolti nella vie secretorie e endocitotica
