2 eso.t2.estados de la materia
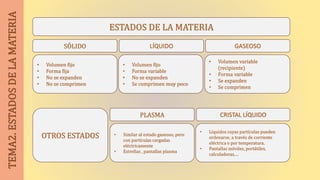
- 1. ESTADOS DE LA MATERIA SÓLIDO GASEOSOLÍQUIDO • Volumen fijo • Forma fija • No se expanden • No se comprimen • Volumen fijo • Forma variable • No se expanden • Se comprimen muy poco • Volumen variable (recipiente) • Forma variable • Se expanden • Se comprimen PLASMA CRISTAL LÍQUIDO • Similar al estado gaseoso, pero con partículas cargadas eléctricamente • Estrellas , pantallas plasma • Líquidos cuyas partículas pueden ordenarse, a través de corriente eléctrica o por temperatura. • Pantallas móviles, portátiles, calculadoras,… OTROS ESTADOS
- 2. TEORÍA CINÉTICA Intenta explicar el comportamiento de los diferentes estados de agregación a partir de unos postulados muy sencillos: La materia está formada por partículas muy pequeñas (que consideraremos esféricas), entre las que existen fuerzas de cohesión (unión) Estas partículas están dotadas de movimiento. El movimiento será mayor cuanto mayor sea la temperatura
- 3. TEORÍA CINÉTICA Y ESTADO SÓLIDO ¿Cómo es su estructura interna? ¿Cómo se explican sus propiedades? Las fuerzas de cohesión son muy grandes, y las partículas están muy próximas entre sí. Los movimientos de las partículas son de vibración (que aumentarán con la temperatura, y viceversa) Al ser las fuerzas que mantienen unidas las partículas muy fuertes, estas no pueden separarse, cambiar de posición, ni tampoco aproximarse entre sí. De ahí que el volumen y forma de los sólidos sean constante, que no puedan comprimirse, expandirse ni deformarse. Al hallarse muy próximas las partículas, la densidad de los sólidos será, por lo general, mayor que la de líquidos y gases Dado que al aumentar la temperatura las partículas vibran más fuertemente, estas se separarán algo más. Esto explica la dilatación de los sólidos. Al disminuir la temperatura, sucederá lo contrario.
- 4. TEORÍA CINÉTICA Y ESTADO LÍQUIDO ¿Cómo es su estructura interna? ¿Cómo se explican sus propiedades? Las fuerzas de cohesión son menores que en sólidos. Las partículas se encuentran en grupos que pueden deslizarse entre sí. Los movimientos de las partículas son de traslación y vibración (que aumentarán con la temperatura, y viceversa) Al ser aún fuertes las fuerzas entre partículas, estas no pueden separarse, por lo que los líquidos no se expanden. La ligera compresión se explica porque las partículas podrán aproximarse ligeramente al no estar rígidamente unidas. Al deslizarse entre sí los grupos de partículas, podrán adaptarse a la forma del recipiente La densidad de los sólidos será, por lo general, menor que la de sólidos, pero mayor que la de gases Dado que al aumentar la temperatura las partículas vibran más, y los desplazamientos de grupos de partículas serán mayores, la densidad disminuirá. Al disminuir la temperatura, sucederá lo contrario.
- 5. TEORÍA CINÉTICA Y ESTADO GASEOSO ¿Cómo es su estructura interna? ¿Cómo se explican sus propiedades? Las fuerzas de cohesión son muy débiles, por lo que las partículas se mueven libremente (por todo el recipiente). Como consecuencia, estarán muy separadas Los movimientos de las partículas son de traslación (que aumentarán con la temperatura, y viceversa) Al ser casi nulas las fuerzas entre partículas, y estar muy separadas entre sí, un cambio en el volumen no modificará las condiciones. Por ello los gases pueden comprimirse y expandirse Por la misma razón, un cambio en la forma del recipiente, no modificará las condiciones. Por ello los gases adoptar la forma del recipiente La densidad de los gases será muy baja, al hallarse las partículas muy dispersas (muy poco agrupadas) Al aumentar la temperatura las partículas se moverán más, aumentando la separación entre ellas, con lo cual la densidad disminuirá. Al disminuir la temperatura, sucederá lo contrario.
- 6. LEYES DE LOS GASES Durante los siglos XVII y XVIII los científicos estudiaron el comportamiento de los gases. Los resultados de estos estudios demostraron que la presión, el volumen y la temperatura (absoluta) a la que se hallaban estaban relacionadas entre sí. Como consecuencia, se obtuvieron una serie de ecuaciones matemáticas, llamadas LEYES DE LOS GASES LEY DE BOYLE-MARIOTTE LEY DE GAY-LUSSAC LEY DE CHARLES La temperatura absoluta o KELVIN es otra escala termométrica, basada en el movimiento de las partículas. Su relación con la escala CELSIUS es: 𝐾 = ℃ + 273´15 ℃ = 𝐾 − 273´15
- 7. LEY DE BOYLE-MARIOTTE Esta ley relaciona la presión y el volumen de un gas, CUANDO LA TEMPERATURA ES CONSTANTE (es decir, no varía) “A temperatura constante, para una misma masa de gas, el producto de la presión de un gas por el volumen que ocupa es un valor constante” Matemáticamente: 𝑝. 𝑉 = 𝑐𝑡𝑒 (𝑇𝑐𝑡𝑒) 𝑝1. 𝑉1 = 𝑝2. 𝑉2 (𝑇𝑐𝑡𝑒) p (atm) V (L) p.V (atm.L) 4 1 4 2 2 4 1 4 4 8 8 20 0´25
- 8. LEY DE GAY-LUSSAC Esta ley relaciona la presión y la temperatura absoluta, CUANDO EL VOLUMEN OCUPADO POR UN GAS ES CONSTANTE (es decir, no varía) “A volumen constante, para una misma masa de gas, el cociente entre de la presión de un gas y la temperatura a la que se encuentra es un valor constante” Matemáticamente: 𝑝 𝑇 = 𝑐𝑡𝑒 (𝑉𝑐𝑡𝑒) 𝑝1 𝑇1 = 𝑝2 𝑇2 (𝑉𝑐𝑡𝑒) p (atm) T (K) p/T (atm/K) 1 400 0´0025 0´75 300 0´0025 0´5 200 0´0025 0´25 100 0´0025 800 1´5 2
- 9. LEY DE CHARLES Esta ley relaciona el volumen y la temperatura absoluta, CUANDO LA PRESIÓN EJERCIDA POR UN GAS ES CONSTANTE (es decir, no varía) “A presión constante, para una misma masa de gas, el cociente entre el volumen de un gas y la temperatura a la que se encuentra es un valor constante” Matemáticamente: 𝑉 𝑇 = 𝑐𝑡𝑒 (𝑃𝑐𝑡𝑒) 𝑉1 𝑇1 = 𝑉2 𝑇2 (𝑃𝑐𝑡𝑒) V (L) T (K) V/T (L/K) 1 500 0´002 0´75 375 0´002 0´5 250 0´25 1000 1´5 2
- 11. FUSIÓN-SOLIDIFICACIÓN Cambios de estado entre sólido y líquido, que se producen A LA MISMA TEMPERATURA, llamada PUNTO DE FUSIÓN (o temperatura de fusión), cuyo valor depende del tipo de sustancia) VAPORIZACIÓN-CONDENSACIÓN Es el cambio general de estado entre líquido y gas. Si el cambio de líquido a gas se realiza únicamente en la superficie del líquido, a cualquier temperatura, el proceso se denomina EVAPORACIÓN Si el cambio de líquido a gas se realiza en todo el líquido, y a una temperatura fija (TEMPERATURA O PUNTO DE EBULLICIÓN), el proceso se denomina EBULLICIÓN
- 12. CURVAS DE CALENTAMIENTO • TRAMO A-B: A medida que se calienta el sólido, este aumenta su temperatura, pero permanece en ese estado. Las partículas aumentan su vibración • TRAMO B-C: Cambio de estado, y como puede verse, NO HAY CAMBIO DE TEMPERATURA mientras se produce. El calor se “invierte” en romper la estructura del sólido • TRAMO C-D: A medida que se calienta el líquido, este aumenta su temperatura, pero permanece en ese estado. Las partículas se mueven más rápido • TRAMO D-E: Cambio de estado, y de nuevo, NO HAY CAMBIO DE TEMPERATURA mientras se produce. El calor se “invierte” en romper la estructura del líquido. • TRAMO E-F: A medida que se calienta el gas, este aumenta su temperatura, pero permanece en ese estado. Las partículas se mueven más rápido
- 13. SITUACIONES “ESPECIALES” EN CAMBIOS DE ESTADO El agua hierve a 100℃ solamente si la presión exterior es de 1atm; pero existen situaciones en las que ese valor de presión varía. P> 1 atm Como sucede en las ollas a presión. En estos casos el agua hierve por encima de los 100℃. El motivo se debe a que para poder “escapar” del líquido, las partículas necesitan mayor energía (lo que se consigue con una mayor temperatura) P< 1 atm Como sucede en zonas de alta montaña. En estos casos el agua hierve por debajo de los 100℃. El motivo se debe a que para poder “escapar” del líquido, las partículas necesitan menos energía (lo que se consigue con una menor temperatura) Fusión del hielo por aumento de presión Un aumento local de presión sobre un trozo de hielo . (LINK)
- 14. CAMBIOS DE ESTADO DEL AGUA Y METEOROLOGÍA NUBES NIEBLA GRANIZO LLUVIA ROCÍO Y ESCARCHA HIELO (HELADAS) ESTELA AVIONES VAHO RESPIRACIÓN