Contenu connexe
Similaire à المحاليل المنظمة ودرجة الأس الهيدروجيني
Similaire à المحاليل المنظمة ودرجة الأس الهيدروجيني (20)
Plus de Univ. of Tripoli (20)
المحاليل المنظمة ودرجة الأس الهيدروجيني
- 1. اٌفظً اٌضبٌش
اٌّؾٍٛي إٌّظُ ٚدسعخ األط اٌٙ١ذسٚع١ٕٟ
األ٠ْٛ
رؼش٠ف األ٠ْٛ :- ػجبسح ػٓ عضا أٚ رسح أٚ ِغّٛػخ ِٓ اٌغضئ١بد أٚاٌزساد اٌزٟ رؾًّ اٌشؾٕبد
اٌىٙشث١خ اٌغبٌجخ أٚ اٌّٛعجخ ، رىٛٔذ ٔز١غخ فمذ أٚ إوزغبة اٌّٛاد اٌزٟ أٔزغذ ٘زٖ األ٠ٛٔبد إٌىزشٚٔب
ٚاؽذ أٚ أوضش.
ٚرٕمغُ األ٠ٛٔبد وبٌزبٌٟ
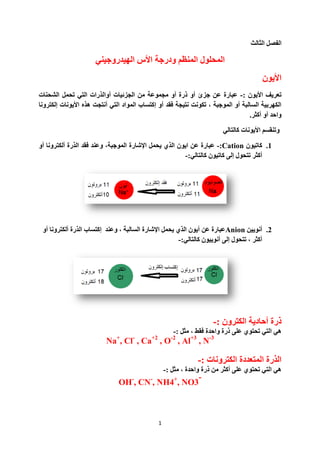
1. وبر١ْٛ -:Cationػجبسح ػٓ ا٠ْٛ اٌزٞ ٠ؾًّ اإلشبسح اٌّٛعجخ، ٚػٕذ فمذ اٌزسح أٌىزشٚٔب أٚ
أوضش رزؾٛي إٌٝ وبر١ْٛ وبٌزبٌٟ:-
2. أٔٛ٠١ٓ Anionػجبسح ػٓ أ٠ْٛ اٌزٞ ٠ؾًّ اإلشبسح اٌغبٌجخ ، ٚػٕذ إوزغبة اٌزسح أٌىزشٚٔب أٚ
أوضش ، رزؾٛي إٌٝ أٔٛ٠١ْٛ وبٌزبٌٟ:-
رسح أؽبد٠خ اٌىزشْٚ :-
ٟ٘ اٌزٟ رؾزٛٞ ػٍٝ رسح ٚاؽذح فمؾ ، ِضً :-
3-Na , Cl , Ca , O , Al+3 , N
+ - 2+ 2-
اٌزسح اٌّزؼذدح اٌىزشٚٔبد :-
ٟ٘ اٌزٟ رؾزٛٞ ػٍٝ أوضش ِٓ رسح ٚاؽذح ، ِضً :-
-
3OH-, CN-, NH4 , NO +
1
- 2. مثال:-
الحل:- عدد البروتونات = ( 13 – 1 = 13 )
مثال :-
الحل:- عدد البروتونات = 31 ( 31 – (-2) = 31)
اٌّشوجبد ٚاٌظ١غخ ٌٍّشوجبد األ٠ٛٔ١خ:- ػجبسح ػٓ ِشوجبد رؾزٛٞ ػٍٝ اٌىبرٛٔبد ٚاأل٠ٛٔ١ٕبد ( أ٠ٛٔبد
عبٌجخ ِٚٛعجخ) ثؾ١ش رغبٚٞ ػذد اٌشؾٕبد اٌىٙشث١خ اٌّٛعجخ ػذد اٌشؾٕبد اٌىٙشث١خ اٌغبٌجخ فٟ
اٌّؼبدٌخ ٚرىْٛ اٌؾظ١ٍخ إٌٙبئ١خ ٌؼذد اٌشؾٕبد اٌّٛعجخ ٚاٌغبٌجخ = طفشا
رأ٠ٓ اٌّبء
(٠زأ٠ٓ ( ٠زفىه ) اٌّبء رأ٠ٕب ػىغ١ب) ٌ١ؼطٟ:
1. أ٠ٛٔبد اٌٙ١ذسٚع١ٓ ( ثشٚرْٛ اٌٙ١ذسٚع١ٓ +)H
-
2. أ٠ٛٔبد اٌٙ١شٚوغ١ً ( )OH
2
- 3. رٛاصْ ِؼبدٌخ ط١غخ اٌّبء
اٌّبء لٍ١ً اٌزأ٠ٓ:- ثبٌشغُ ِٓ ِ١ً اٌّبء اٌمٍ١ً ٌٍزأ٠ٓ ثغجت طغش وزٍخ رسح اٌٙ١ذسٚع١ٓ اٌزٞ ٠شرجؾ
إٌىزشٚٔٗ اٌٛؽ١ذ اسرجبؽب شذ٠ذا ِغ رسح األٚوغ١غ١ٓ فٟ عضا اٌّبء.
اٌزأ٠ٓ اٌزارٟ ٌٍّبء -: ٘ٛ رفبػً و١ّ١بئٟ ٠زُ فٟ اٌّبء إٌمٟ أٚ اٌّؾٍٛي اٌّبئٟ رار١ب ، ؽ١ش ٠ٕزمً
+
ثشٚرْٛ ِٓ عضا اٌّبء إٌٝ عضا آخش ، ف١زىْٛ أ٠ٛٔ١ٓ ّ٘ب اٌٙ١ذسٚٔ١َٛ ٚ H3Oاٌٙ١ذسٚوغ١ذ
−٠ٚ .OHؼذ اٌزأ٠ٓ اٌزارٟ ٌٍّبء ، ِضبي ػٍٝ رؾًٍ اٌجشٚرْٛ اٌزٍمبئٟ ، ٚرّض١ً اٌززثزة (ِزشدد) اٌطج١ؼٟ
ٌٍّبء.
3
- 4. اٌخبط١خ األِفٛر١ش٠خ ٌٍّبء
٠ؼًّ اٌّبء وؾبِغ ٚومبػذح ، ثغجت ٚعٛد أ٠ٛٔبد اٌٙ١ذسٚع١ٓ غ١ش ؽشح، فٙٝ ِشرجطخ ثغضا اٌّبء
( ػذد 2 عضء ِٓ اٌّبء) ٚ٠مٛد ٘زا اإلٔذِبط ٌ١ىْٛ أ٠ْٛ اٌٙ١ذسٚٔ١َٛ ، ٚرؼزجش أ٠ٛٔبد اٌٙ١ذسٚع١ٓ
ؽم١مخ ٌٚ١غذ ؽشح فٟ اٌّؾٍٛي ٌزؼطٟ ٘١ذسٚٔ١َٛ )+ ، (H3Oففٟ ٘زا اٌزفبػً ٠زظشف اٌّبء وؾبِغ
ٚومبػذح أٞ أٔٗ ٌٗ خبط١خ األِفٛر١ش٠خ، ِشرجطخ ثغضا اٌّبء (رفبػً عضئ١ٓ ِٓ اٌّبء)، ٚ٘زا اإلٔذِبط
٠ؼطٟ أ٠ْٛ اٌٙ١ذسٚٔ١َٛ ، فٟ ٘زا اٌزفبػً ٠زظشف اٌّبء ، وؾبِغ ٚومبػذح ، أٞ أْ اٌّبء ٌٗ خبط١خ
األِفٛر١ش٠خ ، ِٚضً عّ١غ اٌزفبػالد اٌؼىغ١خ ،ٚرأ٠ٓ اٌّبء ، ٠ّىٓ أْ ٠زُ ٚطفٗ ثٛاعطخ صبثذ اٌزأئ١ٓ،
ٚ٘زا اٌزأ٠ٓ اٌؼىغٟ ُِٙ عذا ٌذٚس اٌّبء فٟ ٚظبئف اٌخٍ١خ اٌؾ١خ ، ِٚٛلف اإلرضاْ ألٞ رفبػً و١ّ١بئٟ
٠ؼطٝ ثٛاعطخ صبثذ ااٌزأئ١ٓ ٌٍزفبػً اٌؼبَ وبٌزبٌٟ:-
صبثذ اإلرضاْ)ّ٠ (Keqىٓ أْ ٠ؼشف ثٛاعطخ رشاو١ضاٌّٛاد إٌبرغخ) (C and Dػٍٝ رشاو١ض اٌّٛاد
اٌّزفبػٍخ) ( A and Bاٌّٛعٛدح فٟ اإلرضاْ.
اٌؼٛاًِ اٌّؤصشح ػٍٝ ؽبٌخ االرضاْ
1. رشو١ض اٌّٛاد.
2. اٌؼغؾ .
3. دسعخ اٌؾشاسح.
ِجذأ ٌٛشبرٍ١١ٗ
إرا أصش ِؤصش ِب ( ِضً اٌزشو١ض أٚ اٌؼغؾ أٚ دسعخ اٌؾشاسح ) ػٍٝ رفبػً فٟ ؽبٌخ االرضاْ فئْ اٌزفبػً
٠غ١ش فٟ االرغبٖ اٌزٞ ٠مًٍ ف١ٗ ِٓ فؼً ٘زا اٌّؤصش
أٚالً : أصش اٌزشو١ض ػٍٝ ؽبٌخ االرضاْ
ٚعذ ػٍّ١ب ً أٔٗ ثض٠بدح رشو١ض إؽذٜ اٌّٛاد اٌّزفبػٍخ فئْ اٌزفبػً ع١غ١ش فٟ االرغبٖ األطٍٟ ٔؾٛ رىْٛ
اٌّض٠ذ ِٓ اٌّٛاد إٌبرغخ، ٚػٕذ ص٠بدح رشو١ض إؽذٜ اٌّٛاد إٌبرغخ فئْ اٌزفبػً ٠غ١ش فٟ االرغبٖ
اٌؼىغٟ ٔؾٛ رىْٛ اٌّض٠ذ ِٓ اٌّٛاد اٌّزفبػٍخ ، ٚاٌؼىظ ثبٌؼىظ ، ٚفٟ وً اٌؾبالد رجمٝ ل١ّخ
صبثذ االرضاْ Kصبثزخ ال رزغ١ش فزغ١ش اٌزشو١ض ال ٠ؤصش ػٍٝ ل١ّخ صبثذ االرضاْ.
4
- 5. ٚ٠ّىٓ رفغ١ش ٘زا األصش ٚفك ِجذأ ٌٛشبرٍ١١ٗ ػٍٝ اػزجبس أْ ص٠بدح رشو١ض اؽذٜ اٌّٛاد اٌّزفبػٍخ( ِضالً )
٠ؤدٞ إٌٝ اخزالي االرضاْ ف١ىْٛ ٘زا ٘ٛ اٌّؤصش ٌٚىٟ ٠ؾبفع اٌزفبػً ػٍٝ ؽبٌخ االرضاْ فئٔٗ ع١ؼزش٠ٗ
رغ١ش فٟ االرغبٖ اٌزٞ ٠مًٍ ِٓ فؼً ٘زا اٌّؤصش ٚ٘ٛ ٕ٘ب ثغ١ش اٌزفبػً فٟ االرغبٖ االطٍٟ ، فبٌىّ١خ
اٌّؼبفخ ِٓ اٌّبدح اٌّزفبػٍخ عززٛصع فٟ ؽشفٟ اٌّؼبدٌخ (عضء ٠جمٝ ِزفبػالد ٚعضء ٠زؾٛي ٌٕٛارظ )
ٌ١ظً اٌزفبػً إٌٝ ؽبٌخ ارضاْ عذ٠ذح رجمٝ ف١ٙب ل١ّخ صبثذ االرضاْ ٌٍزفبػً صبثزخ ال رزغ١ش.
شىً ( ) ِؼذي عشػخ رفبػً اٌّٛاد اٌذاخٍخ ٚإٌبرغخ
صبٔ١ب ً :رأص١ش اٌؼغؾ ػٍٝ ؽبٌخ االرضاْ
ٌقتصر أثر الضغط فً التفاعالت المتزنة على التفاعالت الغازٌة فقط ووجد عملٌا ً أن أثرالضغط
على حالة االتزان ٌتوقف على نوع التفاعل من حٌث تساوي عدد موالت المواد فً طرفً المعادلة أو
عدم تساوٌها ، ففً التفاعالت التً ٌكون فٌها عدد موالت المواد المتفاعلة ٌساوي عدد موالت المواد
الناتجة وجد أن تغٌر الضغط ال ٌؤثر على حالة االتزان وال على قٌمة ثابت االتزان Kبالطبع .
أما بالنسبة للتفاعالت التً تختلف فٌها عدد موالت المواد فً طرفً المعادلة فوجد أنه بزٌادة
الضغط ( زٌادة الضغط على النظام بالكامل ) فإن التفاعل ٌتجه نحو الطرف الذي ٌكون فٌه عدد موالت
المواد أقل ، وبنقص الضغط ٌتجه التفاعل نحو عدد الموالت األكثر وال تتأثر هنا قٌمة ثابت االتزان K
أٌضا .
ٚ٠ّىٓ رفغ١ش ٘زا األصش ِٓ خالي ِجذأ ٌٛشبرٍ١١ٗ ػٍٝ أعبط أٔٗ ػٕذ ص٠بدح اٌؼغؾ ( ػٍٝ اٌزفبػً
ثبٌىبًِ ) فئْ اٌؼغؾ إٌبشٟء ػٓ اٌّٛاد ( اٌّزفبػٍخ أٚ إٌبرغٗ ) راد ػذد اٌّٛالد األوضش ع١ىْٛ أوجش
( رزوش أْ اٌؼغؾ اٌغضئٟ ٌٍغبصاد ٠ؼزّذ ػٍٝ ػذد اٌغغ١ّبد ٌٚ١ظ ٔٛػٙب ) ف١ىْٛ ٘زا اٌّؤصش ِٚٓ صُ
فئْ سد اٌفؼً ٌٍزمٍ١ً ِٓ ٘زا اٌّؤصش فئْ اٌزفبػً ع١زغٗ ٔؾٛ اٌطشف اٌزٞ رىْٛ ف١ٗ ػذد اٌّٛالد ألً
ٌ١ظً اٌزفبػً إٌٝ ؽبٌخ ارضاْ عذ٠ذح رىْٛ ػٕذ٘ب ل١ّخ صبثذ االرضاْ ِ Kغبٚ٠خ ٌم١ّخ صبثذ االرضاْ لجً
ص٠بدح اٌؼغؾ أٞ أْ ل١ّخ صبثذ االرضاْ ال رزغ١ش ثزغ١ش اٌؼغؾ .
5
- 6. صبٌضب ً : أصش دسعخ اٌؾشاسح ػٍٝ ؽبٌخ االرضاْ
٠زٛلف أصش دسعخ اٌؾشاسح فٟ اٌزفبػالد اٌّزضٔخ ػٍٝ ٔٛع اٌزفبػً ِٓ ؽ١ش اٌّؾزٜٛ اٌؾشاسٞ ففٟ
اٌزفبػالد اٌّبطخ ٌٍؾشاسح ٚعذ ػٍّ١ب ً أْ اسرفبع دسعخ اٌؾشاسح فٟ اٌزفبػً اٌّزضْ رغؼً اٌزفبػً ٠غ١ش
فٟ االرغبٖ األطٍٟ ٔؾٛ رىٛ٠ٓ اٌّض٠ذ ِٓ اٌّٛاد إٌبرغخ ( ػٍٝ ؽغبة اٌّٛاد اٌّزفبػٍخ ) ثّؼٕٝ أٔٗ فٟ
٘زٖ اٌؾبٌخ ع١ضداد رشو١ض اٌّٛاد إٌبرغخ ( اٌّٛعٛدح فٟ ثغؾ لبْٔٛ االرضاْ ) ٚ٠مً رشو١ض اٌّٛاد
اٌّزفبػٍخ ( اٌّٛعٛدح فٟ اٌّمبَ ) ٌزٌه ٔغذ أْ ل١ّخ صبثذ االرضاْ رضداد ثبسرفبع دسعخ اٌؾشاسح فٟ
اٌزفبػالد اٌّبطخ ٌٍؾشاسح ، ٚاٌؼىظ طؾ١ؼ ثخفغ دسعخ اٌؾشاسح .
ٚفٟ اٌزفبػالد اٌطبسدح ٌٍؾشاسح ٚعذ ػٍّ١ب ً أْ اسرفبع دسعخ اٌؾشاسح فٟ اٌزفبػً اٌّزضْ رغؼً
اٌزفبػً ٠غ١ش فٟ االرغبٖ اٌؼىغٟ ٔؾٛ رىْٛ اٌّض٠ذ ِٓ اٌّٛاد اٌّزفبػٍخ ( ػٍٝ ؽغبة اٌّٛاد إٌبرغخ )
ثّؼٕٝ أٔٗ فٟ ٘زٖ اٌؾبٌخ ع١ضداد رشو١ض اٌّٛاد اٌّزفبػٍخ ( اٌّٛعٛدح فٟ ِمبَ لبْٔٛ االرضاْ ) ٚ٠مً
رشو١ض اٌّٛاد إٌبرغخ ( اٌّٛعٛدح فٟ اٌجغؾ ) ٌزٌه ٔغذ أْ ل١ّخ صبثذ االرضاْ رمً ثبسرفبع دسعخ اٌؾشاسح
فٟ اٌزفبػالد اٌطبسدح ٌٍؾشاسح ، ٚاٌؼىظ طؾ١ؼ ثخفغ دسعخ اٌؾشاسح .
تفسٌر أثر الحرارة على حالة االتزان وفق مبدأ لوشاتللٌه على افتراض أننا ٌمكن اعتبار الحرارة
فً التفاعالت الماصة للحرارة وكأنها مادة متفاعلة فعندما نرفع درجة الحرارة نكون كأننا أضفنا كمٌة
من المادة المتفاعلة للتفاعل فٌكون رد فعل التفاعل للتقلٌل من هذا المؤثر هو اتجاه التفاعل فً االتجاه
األصلً . والشًء نفسه ٌحدث فً التفاعالت الطارة للحرارة فٌمكن اعتبار الحرارة هنا وكأنها مادة
ناتجة .
المواد الحافزة وجد عملٌا ً بأنها التؤثر على حالة االتزان اطالقا ً وٌتوقف أثرها على زٌادة سرعة
الوصول إلى حالة االتزان عن طرٌق زٌادة سرعة التفاعلٌٌن العكسٌٌن. ومن ثم فإنها التؤثر على
قٌمة ثابت االتزان Kأٌضا ً. وكذلك السموم فلٌس لها تأثٌر ال على حالة االتزان وال قٌمة ثابت االتزان .
صبثذ اإلرضاْ ٌٍّبء
صبثذ اإلرضاْ ل١ّخ صبثزخ ِّٚ١ضح ألٞ رفبػً و١ّ١بئٟ ٠ؼطٝ ػٕذ دسعخ ؽشاسح ِؾذدح ، ٚ٠ؼشف ِىٛٔبد
خٍ١ؾ اإلرضاْ إٌٙبئٟ ٌٍزفبػً ثغغ إٌظش ػٓ اٌىّ١بد اٌزٟ ثذأٔب ثٙب ِٓ اٌّزفبػالد ٚثغغ إٌظش ػٓ
وّ١بد اٌّٛاد إٌبرغخ ِٓ اٌزفبػً.
اٌزشو١ض
اٌّبء اٌى١ّ١بئٟ إٌمٟ ٌٗ لذسح رٛط١ً وٙشثبئٟ ٠ؼبدي 550.0 ِب٠ىشٚ ع١ّٕض. عُ −1. ٚ٠شعغ رٌه
ٌٛعٛد أ٠ٛٔبد فٟ اٌّبء ٚفمب ٌٕظش٠خ عفبٔذ أٚغغذ أس٠ٕ١ٛط , ٚرٕزظ ٘زٖ األ٠ٛٔبد (عبٌجخ اٌشؾٕخ ،
ِٚٛعجخ اٌشؾٕخ) ِٓ رفبػً اٌزأ٠ٓ اٌزارٟ ٌٍّبء :
6
- 7. ؽ١ش ٠ٕطجك ٘زا اٌزٛاصْ ػٍٝ اٌّبء إٌمٟ ٚأٞ ِؾٍٛي ِبئٟ , ٚ٠ؼطٝ صبثذ اإلرضاْ اٌى١ّ١بئٟ ثبٌؼاللخ
اٌزبٌ١خ :
فٟ ؽبٌخ إرا وبْ رشو١ض اٌّٛاد اٌّزاثخ فٟ اٌّؾٍٛي[ِٕ ] H2 Oخفؼخ ف١ّىٓ اػزجبس٘ب صبثزٗ ٚرغبٚٞ
[5.551[ .٠ٚ ، Mشِض ٌضبثذ رأ٠ٓ اٌّبء (صبثذ اٌزفىه) أٚ صبثذ اٌزأ٠ٓ اٌزارٟ ٌٍّبء ثبٌشِض ٠ٚ Kwؼطٝ
ثبٌؼاللخ اٌزبٌ١خ:
ؽ١ش ]3+ ٛ٘ : [HOرشو١ض أ٠ْٛ اٌٙ١ذسٚع١ٓ أٚ أ٠ْٛ اٌٙ١ذسٚٔ١َٛ ٚ ]−ِ ٛ٘ٚ [OHغبٚ٠ب ٌزشو١ض أ٠ْٛ
اٌٙ١ذسٚوغ١ذ ػٕذ 52 دسعخ ِئٛ٠خ ، ٚصبثذ رأ٠ٓ اٌّبء ٘ٛ
41-01×0.1=Kw
ػٕذ فظً عض٠ئبد اٌّبء إٌٝ وّ١بد ِزغبٚ٠خ ِٓ OH− ٚ H+3Oرىْٛ رشو١ضارٙب ِزغبٚ٠خ
ٚ٠ىْٛ رشو١ض( ) H3+Oفٟ اٌّبء ِغبٚ٠ب ٌزشو١ض )−) OH
اٌّبء إٌمٟ ِزؼبدي ٌىٓ ِؼظُ اٌّ١بٖ رؾزٛٞ ػٍٝ شٛائت ٠ٕزظ ػٕٙب إِب أْ ٠ىْٛ اٌّؾٍٛي ؽّؼٟ أٚ
لبػذٞ اٌزٞ ثذٚسٖ ٠ؤصش ػٍٝ رشو١ض أ٠ْٛ اٌٙ١ذسٚوغ١ذ ٚأ٠ْٛ اٌٙ١ذسٚٔ١َٛ,
ٚرّزض ػ١ٕبد اٌّبء اٌّؼشػخ ٌٍٙٛاء ؽبِغ صبٟٔ أوغ١ذ اٌىشثْٛ ف١ض٠ذ رشو١ض ٠ٚ H3+Oمً رشو١ض
-ٚ OHثبعزّشاس رٌه ٠غزّش إٔزبط [-.]H3+O][OH
7
- 8. أٔٛاع اٌّــــــبء
رزشاٚػ ٔغجخ اٌّبء فٟ اٌخٍ١خ ث١ٓ08 – 09 %, ٚ٠ؼزجش اٌّىْٛ األعبعٟ ٌجمبء اٌخٍ١خ، ٌٚم١بِٙب
ثغّ١غ ٚظبئفٙب ٚأٔشطزٙب اٌشئ١غخ، ٚ٠ٛعذ اٌّبء فٟ اٌظٛس ا٢ر١خ:-
1. اٌّبء اٌؾش: ٠ّأل فغٛاد اٌّبدح اٌغزائ١خ،ٚ٠ؾزفع ثظفبرٗ اٌطج١ؼ١خ؛ ِٓ ؽ١ش وٛٔٗ ِز٠جب
ٌٍغىش٠بد، ٚاألِالػ ٚاألؽّبع راد األٚصاْ اٌغضئ١خ اٌظغ١شح، ٚ٠ؼًّ أ٠ؼب ٚعطب رزٚة ف١ٗ
اٌغشٚ٠بد اٌّؾجخ ٌٍّبء، ِضً: اٌجشٚر١ٕبد ٚاألطّبؽ ٚاٌّشوجبد اٌف١ٌٕٛ١خ، ِىٛٔب ِؾٍٛال غشٚ٠ب.
2. ِبء األدِظبص: ٚعذ ػٍٝ ؽجمخ سل١مخ عذا، ثغّه عضا أٚ ػذح عضئ١بد فٟ داخً ٚخبسط
عطٛػ اٌّٛاد اٌظٍجخ اٌّٛعٛدح؛ وبٌٕشب ٚاٌجىز١ٓ ٚاٌغٍ١ٍٛص ٚاٌجشٚر١ٓ, ِشرطجب ِؼٙب ثمٛح
عزة اٌشٚاثؾ اٌٙ١ذسٚع١ٕ١خ أٚ ثشٚاثؾ أخشٜ رغّٝ لٜٛ اٌفبٔذسٚٚاٌظ.
3. اٌّبء اٌّزؾذ: ٚ٘ٛ اٌغضء ِٓ اٌّبء اٌّزؾذ و١ّبئ١ب ِغ ثؼغ اٌّشوجبد وبٌغٍٛوٛص، ٚثؼغ
األِالػ وٕزشاد اٌجٛربع١َٛ، ٚ٠غّٝ ٘زا اٌّبء ثّبء اٌٙذسارٗ
شىً ( ) أٔٛاع اٌّبء ، 1. اٌّبء اٌّشرجؾ. 2. اٌّبء اٌّزؾشن. 3. اٌّبء األدِظبص. 4. عٍغخ
ثشٚر١ٕ١خ. 5. ِغّٛػخ ؽشح ِؾجخ ٌٍّبء ِشؾٛٔخ ثبٌشؾٕبد اٌىٙشثبئ١خ. 6. عضئ١بد اٌّبء. 7. عضئ١بد
اٌّبء. 8. عضئ١بد اٌّبء اٌؾش
فٟ اٌشىً ( ) ٠ٛػؼ أٔٛاع اٌّبء اٌضالصخ ، اٌؾش ، ٚاٌّشرجؾ ، ٚاألدِظبص ، ِٚذٞ لٛح اسرجبؽٗ
ثبٌجشٚر١ٓ، ػٍٝ عٙخ اٌ١غبس: ِغبِ١غ ِبئ١خ ِشؾٛٔخ فٟ ثشٚر١ٓ اٌؼؼالد رغزة اٌّبء ِىٛٔخ ؽجمخ
ِشرجطخ اسرجبؽب لٛ٠ب ِغ اٌّغّٛػخ اٌّشؾٛٔخ، ٚؽجمخ اٌٛعؾ اسرجبؽ عض٠ئبرٙب الً ثبٌّغّٛػبد
اٌّشؾٛٔخ ، فٟ اٌطجمخ األخ١شح ِٓ اٌّبء ، اسرجبؽٙب ثبٌّغّٛػبد اٌّشؾٛٔخ ػؼ١ف عذا.
8
- 9. اٌّؾبٌ١ً إٌّظّخ
اٌّؾٍٛي إٌّظُ ، ٘ٛ ِؾٍٛي ِبدح ، أٚ خٍ١ؾ ِٓ اٌّٛاد ، رمبَٚ اٌزغ١ش اٌىج١ش فٟ اٌشلُ اٌٙ١ذسٚع١ٕٟ
ٌٍٛعؾ ، ػٕذ إػبفخ وّ١بد لٍ١ٍخ ِٓ اٌؾبِغ ، أٚ اٌمبػذح، ٚرؼزجش اٌّؾبٌ١ً إٌّظّخ ، راد أّ٘١خ
وج١شح فٟ ػٍّٙب ، ثبٌّؾبفظخ ػٍٝ دسعخ األط اٌٙ١ذسٚع١ٕٟ ٌألٔظّخ اٌؾ١خ، ٚرٌه أْ رغ١ش دسعخ األط
اٌٙ١ذسٚع١ٕٟ ، داخً اٌخال٠ب فٟ اٌغٛائً اٌؾ١ٛ٠خ ، رؤدٞ إٌٝ ػؼف ٔشبؽ األٔض٠ّبد، ٚسثّب فمذأٗ
ٚرغ١ش فٟ شىً اٌجشٚر١ٕبد ، ٚسثّب فمذأٙب ٌٍٕشبؽٙب اٌؾ١ٛٞ اٌزٟ رمَٛ ثٙب ، ِضً:- ٔمً ا٢وغغ١ٓ
ِٚمبِٚخ اٌؼذٜٚ اٌخبسع١خ ، ٚاٌؾشوخ، ٚوّب ٠غزفبد ِٓ اٌّؾبٌ١ً إٌّظّخ فٟ اٌّؾبفظخ ػٍٝ دسعخ
األط اٌٙ١ذسٚع١ٕٟ ، أصٕبء إعشاء اٌزغبسة ثؾض١خ ِؼ١ٕخ ، ػٕذ سلُ ِٓ دسعخ األط اٌٙ١ذسٚع١ٕٟ ِؼ١ٓ
دْٚ اٌغّبػ ٌم١ّزٗ ،ثبٌزغ١ش أصٕبء إعشاء اٌزغبسة .
أنواع المحالٌل المنظمة:-
تنقسم المحالٌل المنظمة من حٌث تكوٌنها الكٌمٌائً إلى نوعٌن:-
النوع األول:-المحالٌل المنظمة الحامضٌة :- وهً تتكون من حامض ضعٌف وقاعدته
القرٌنة ) )Conjugatedمثل حامض السترٌك (الخل) الذي ٌتأٌن حسب المعادلة التالٌة:-
وٌفضل استخدام هذه المحالٌل فً األوساط الحامضٌة
إٌٛع اٌضبٟٔ :- اٌّؾبٌ١ً إٌّظّخ اٌمبػذ٠خ :- ٟٚ٘ رزىْٛ ِٓ لبػذح ػؼ١فخ ٚؽبِؼٙب اٌمش٠ٓ ِضً
ِشوجبد اٌؾبٚ٠خ ٌّغّٛػخ أِ١ٕ١خ رٍه اٌّٛعٛدح فٟ األؽّبع األِ١ٕ١خ
9
- 10. ٚ٠فؼً اعزخذاَ ٘زٖ اٌّؾبٌ١ً إٌّظّخ فٟ األٚعبؽ اٌمبػذ٠خ
صبثذ رأ٠ٓ )(pKa
٘ٛ ػبًِ اٌزأ٠ٓ ٚوً ؽبِغ ٌٗ ِؼبًِ رأ٠ٓ صبثذ، ٠خزٍف ػٓ أٞ ؽبِغ أخش، ٚثّؼشفخ رشو١ض
اٌمبػذح اٌمش٠ٕخ ٚاٌخبِغ اٌمش٠ٓ، ٠ّىٓ ؽغبة األط اٌٙ١ذسٚع١ٕٟ ٌٍّؾٍٛي إٌّظُ ، أِضٍخ ٌّؾبٌ١ً
ِٕظّخ فٟ األٔظّخ اٌج١ٌٛٛع١خ
1. اٌّؾٍٛي إٌّظُ اٌفٛعفبرٟ ٚاٌزٞ ٠ٛعذ داخً اٌخال٠ب اٌؾ١خ ٚدسعخ األط اٌٙ١ذسٚع١ٕٟ ٌٗ
68.6 .
2. اٌّؾٍٛي إٌّظُ ٌٍج١ىشثٛٔبد ٚاٌزٞ ٠ٛعذ داخً اٌذَ ٚدسعخ األط اٌٙ١ذسٚع١ٕٟ ٌٗ 4.7 ٚػٕذ
ص٠بدرٗ فٟ اٌذَ ٠غجت ثذاء اٌمٍٛ٠خ ٚAlkalosisػٕذ أخفبػٗ ٠غجت داء اٌؾّٛػخ
.Acidosis
رؾزٛٞ ثشٚر١ٕبد ِظً اٌذَ ػٍٝ أؽّبع أِ١ٕ١خ راد ؽبِؼ١خ ػؼ١فخ ِضً :- ؽبِغ 3.
اٌغٍٛربِ١ه ٚـؾّبع أِ١ٕ١خ راد لبػذ٠خ ػؼ١فخ ِضً اٌال٠غ١ٓ ٘زٖ األؽّبع رظٍؼ أْ رىْٛ
ِؾبٌ١ً ِٕظّخ
ِؼبدٌخ ٕ٘ذسعْٛ ٍ٘غجبن
رغزخذَ ٘زٖ اٌّؼبدٌخ ٌٍشثؾ ث١ٓ سلُ األط اٌٙ١ذسٚع١ٕٟ ٌٍٛعؾ ،اٌم١ّىخ األع١خ ٌضبثذ رأ٠ٓ اٌؾبِغ
أٚ اٌمبػذح ، ٚٔغجخ اٌمبػذح اٌمش٠ٕخ إٌٝ اٌؾبِغ اٌمش٠ٓ.
01
- 11. ثؼغ أِضٍخ ػٍٝ اٌّؾبٌ١ً إٌّظّخ ٚٚظبئفٙب:-
ٔظُ ِؾٍٛي ِٕظُ ِٓ اٌىشثٛٔبد (ِخٍٛؽ ؽّغ اٌىشثٛٔ١ه ٚث١ىشثٛٔبد ) رشو١ض صبٟٔ أوغ١ذ
اٌىشثْٛ فٟ اٌغٛ ٚفٟ اٌّؾ١طبد ٚفٟ اٌغالف اٌؾ١ٛٞ ٌألسع، ٚ٘ٛ ٠شىً أ٠ؼب اٌغضء اٌشئ١غٟ فٟ
ِؾٍٛي ِٕظُ اٌذَ ، ٚ٘ٛ ٠ؾبفع ػٍٝ أْ ٠ىْٛ األط اٌٙ١ذسٚع١ٕٟ (ثب٘بء )pHث١ٓ 53.7 ٚ54.7 ،
ٚ٠ؼبدي رغ١شارٗ ثغجت ػٍّ١خ اٌزّض١ً اٌغزائٟ، ٚػٕذِب رىْٛ ل١ّخ pHفٟ اٌذَ ألً ِٓ 53.7 رغّٝ رٌه
"ؽبِؼ١خ اٌذَ "، ٚػٕذِب رىْٛ ل١ّزٗ أػٍٝ ِٓ 54.7 فزغّٝ رٍه اٌؾبٌخ "لٍٛ٠خ اٌذَ" ، ٚ٠زغجت فٟ
اٌّٛد ػٕذ ل١ّخ pHرؾذ 8.6 أٚ أػٍٝ ِٓ 8 .
رظٕ١ف اٌّؾبٌ١ً إٌّظّخ
رظٕف اٌّؾبٌ١ً إٌّظّخ إٌٝ لغّ١ٓ : ِؾٍٛي ِٕظُ ِغٍك ، ِٚؾٍٛي ِٕظُ ِفزٛػ . (ِضً ِؾٍٛي
ِٕظُ ِٓ ؽّغ اٌخٍ١ه / أع١زبد) رّزض اٌجشٚرٛٔبد ( )+Hأٚ أ٠ٛٔبد ٘١ذسٚوغ١ذ ( )−OHإٌبشئخ
ِٓ رفبػً و١ّ١بئٟ فٟ اٌّؾٍٛي إٌّظُ. ٚرزفبػً ٌزىٛ٠ٓ ؽّغ ِمزشْ أٚ لبػذح إٌّظُ ٚرجمٝ فٟ
اٌّؾٍٛي . أِب فٟ ؽبٌخ اٌّؾٍٛي إٌّظُ اٌّفزٛػ (ِضً ِؾٍٛي ِٕظُ ِٓ ث١ىشثٛٔبد/صبٟٔ أوغ١ذ اٌىشثْٛ
فٟ اٌشئخ) ف١ىْٛ إٌظبَ فٟ خبٌخ رجبدي ِغ اٌٙٛاء . ف١ىْٛ لبدسا ػٍٝ أػظبء ِشوجبد إٌٝ اٌٙٛاء ثؾ١ش
٠ٕؼجؾ ِ ، pHضً خشٚط صبٟٔ أوغ١ذ اٌىشثْٛ 2 COأصٕبء اٌزٕفظ ِغ اٌضف١ش .
ٕ٘بن ٔٛػبْ ِٓ اٌّؾبٌ١ً إٌّظّخ ٟٚ٘ وبٌزبٌٟ:-
1. ِؾٍٛي ِٕظُ ؽبِؼٟ :- ؽبِغ ػؼ١ف + ٍِؼ اٌؾبِغ اٌؼؼ١ف (اٌمبػذح اٌّمزشٔٗ)
2. ِؾٍٛي ِٕظُ لبػذٞ :- لبػذٖ ػؼ١فٗ+ ٍِؼ اٌمبػذٖ اٌؼؼ١فٗ (ؽّغ ِمزشْ)
أِضٍخ ػٍٝ ثؼغ اٌّؾبٌ١ً إٌّظّخ
ِؾٍٛي ؽبِغ اٌخٍ١ه(أعز١ه):- ِؾٍٛي ؽّغ اٌخٍ١ه(أعز١بد) ، أٚ ِؾٍٛي ِٕظُ ؽبِغ
اٌخٍ١ه(األعز١ه) ، ٘ٛ ِؾٍٛي ِٕظُ ِىْٛ ِٓ ِخٍٛؽ ؽّغ اٌخٍ١ه ٚأؽذ أِالؽٗ (أع١زبد) ، ِضً:-
ّ
أع١زبد اٌظٛد٠َٛ ، ٚ٠ّىٓ ؽغبة األط اٌٙ١ذسٚع١ٕٟ ٌّ pHضً ٘زا اٌّؾٍٛي ثّؼبدٌخ ٕ٘ذسعْٛ-
٘بعٍجبٌخ.
ػٕذ إػبفخ أ٠ٛٔبد ٘١ذسٚٔ١َٛ (أٚوغٛٔ١َٛ ) ، أٚ أ٠ٛٔبد ٘١ذسٚوغ١ذ ، ثىّ١بد ٌ١غذ وج١شح
رٕخفغ، أٚ ثبٌزبٌٟ رشرفغ ل١ّخ األط اٌٙ١ذسٚع١ٕٟ اٌّؾٍٛي لٍ١ال عذا، ٚ٘زٖ ٟ٘ اٌخبط١خ ، اٌّّ١ضح
ٌّؾٍٛي ِٕظُ.
ِؾٍٛي ِٕظُ ؽبِغ اٌخٍ١ه/أعز١بد :
11
- 12. ػٕذ إػبفخ أ٠ٛٔبد أٚوغٛٔ١َٛ: - ٠زؼبدي عضء ِٓ أ٠ٛٔبد األٚوغٛٔ١َٛ ِغ اٌمبػذح فٟ اٌّؾٍٛي
ٚ٠زىْٛ اٌّبء ، ٚػٕذ إػبفخ أ٠ٛٔبد ٘١ذسٚوغ١ذ:
أٞ ٠زؼبدي عضء ِٓ أ٠ٛٔبد اٌٙ١ذسٚوغ١ذ ِغ اٌٙ١ذسٚع١ٓ ٚ٠زىْٛ اٌّبء ،ٚ٠ؼطٟ ؽبِغ ػؼ١ف
أ٠ٛٔبد ٘١ذسٚع١ٓ ٌّؼبدٌخ أ٠ٛٔبد اٌٙ١ذسٚوغ١ذ . ٚرزظشف لبػذرٙب اٌمش٠ٕخ (إٌّزغجخ ٌٙب) ِضً آخز
ثشٚرْٛ.
األط اٌٙ١ذسٚع١ٕٟ ٚاٌّؾبٌ١ً إٌّظّخ
٠ؼشف ثبعُ األط اٌٙ١ذسٚع١ٕٟ ، أٚ دسعخ اٌؾّٛػخ ، أٚ اٌجب٘بء ، أٚ اٌمٛح اٌٙ١ذسٚع١ٕ١خ
ثبإلٔىٍ١ض٠خ: )٠ٚ، )power of hydrogen or pHشِض ٌٙب ثبٌشِض ٛ٘ٚ ،pHاٌم١بط اٌزٞ ٠ؾذد ِب
إرا وبْ اٌغبئً ؽبِؼب أَ لبػذح أَ ِزؼبدال.
رؼزجش اٌغٛائً راد دسعخ ؽّٛػخ ألً ِٓ 7 أؽّبػب ، ٚرؼزجش اٌغٛائً راد دسعخ ؽّٛػخ أػٍٝ
ِٓ 7 ِؾٍٛال لٍٛ٠ب أٚ لٛاػذ ، أِب دسعخ اٌؾّٛػخ 7 فٟٙ رؼزجش ِزؼبدٌخ ، ٟٚ٘ رغبٚٞ ؽّٛػخ
اٌّبء إٌمٟ ػٍٝ دسعخ ؽشاسح 52 ِئٛ٠خ، ٚ٠ّىٓ ِؼشفخ دسعخ ؽّٛػخ أٞ ِؾٍٛي ثبعزخذاَ ِؤشش
اٌشلُ اٌٙ١ذسٚع١ٕٟ
رؼش٠ف:- دسعخ اٌؾّٛػخ (٠غّٛٔٙب أؽ١بٔب اٌشلُ اٌٙ١ذسٚع١ٕٟ أٚ األط اٌٙ١ذسٚع١ٕٟ) ٟٚ٘ عبٌت
ٌٛغبس٠ضُ رشو١ض أ٠ْٛ اٌٙ١ذسٚع١ٓ فٟ ِؾٍٛي ِب ٚ٠ش١ش اٌٟ دسعخ ؽّٛػخ رٌه اٌّؾٍٛي ، ٚ٠ّىٓ
ل١بعٗ ػٓ ؽش٠ك ِؤشش اٌشلُ اٌٙ١ذسٚع١ٕٟ.
ٚرؼزجش دسعخ ا٢ط اٌٙ١ذسٚع١ٕٟ أٚ ) ِٓ )pHأُ٘ اٌطشق ٌّؼشفخ رشو١ض أ٠ْٛ اٌٙ١ذسٚع١ٓ أٚ
أ٠ْٛ اٌٙ١ذسٚوغ١ً فٟ أٞ ِؾٍٛي ِبئٟ ، ؽ١ش ٠ٍؼت فٟ اٌّؾبٌ١ً دٚسا اعبع١ب فٟ األٔظّخ اٌج١ٌٛٛع١خ،
ٚ٠ؼشف ثأٔٗ ٌٛغبس٠زُ ِمٍٛة أ٠ْٛ اٌٙ١ذسٚع١ٓ (ٚ٠غزخذَ اٌمبْٔٛ اٌٍٛغبس٠زّٟ ٌزؾذ٠ذ ل١ّخ pH
ثذْٚ ٚؽذاد).
دسعخ األط اٌٙ١ذسٚع١ٕٟ ٌٍّبء = 7-01 ، ٚاٌزٟ رذي ػٍٝ رؼبدي دسعخ رشو١ض االط اٌٙ١ذسٚع١ٕٟ
21
- 13. ٚوٍّب إٔخفؼذ ل١ّخ األط اٌٙ١ذسٚع١ٕٟ ِٓ 7، وٍّب صادد لٛح اٌؾّٛػخ اٌّؾٍٛي ، ٚرؼزجش ل١ّخ دسعخ
األط اٌٙ١ذسٚع١ٕٟ ٌٗ رغبٚٞ 4 أوضش ؽّٛػ١خ ِٓ اٌّؾٍٛي اٌزٞ ل١ّزٗ رغبٚٞ 6.
شىً ( ) ِ١ضاْ دسعخ األط اٌٙ١ذسٚع١ٕٟ
شىً ( ) دسعخ األط اٌٙ١ذسٚع١ٕٟ ٌجؼغ اٌّٛاد ٚاٌغٍغ اٌغزائ١خ
ِؼبدٌخ ٕ٘ذسعْٛ ٍ٘غجبن
رغزخذَ ٘زٖ اٌّؼبدٌخ ٌٍشثؾ ث١ٓ سلُ األط اٌٙ١ذسٚع١ٕٟ ٌٍٛعؾ اٌم١ّىخ األع١خ، ٌضبثذ رأ٠ٓ اٌؾبِغ
أٚ اٌمبػذح ، ٚٔغجخ اٌمبػذح اٌمش٠ٕخ إٌٝ اٌؾبِغ اٌمش٠ٓ.
31
- 14. آٌ١خ ػًّ اٌّؾٍٛي إٌّظُ
1. رأص١ش إػبفخ ؽبِغ HClإٌٝ اٌّؾٍٛي إٌّظُ اٌّىْٛ ِٓ لبػذح ػؼ١فخ ٚؽبِؼٙب اٌّشافك
ّ
:ػٕذ إػبفخ ؽّغ HClرؼٕٟ إػبفخ +ٚ Hاٌزٟ عززفبػً ِغ ٚ OHفك اٌّؼبدٌخ اٌى١ّ١بئ١خ
-
اٌزبٌ١خ :
ٚٚفمب ً ٌّجذأ ٌٛرشبرٍ١١ٗ، ع١زغٗ اٌزفبػً ٔؾٛ اٌ١ّ١ٓ ثزأ٠ٓ اٌّض٠ذ ِٓ 3ٚ ،NHرٌه ٌزؼٛ٠غ إٌمض
- -
فٟ ٚ ،OHثٙزا ٠جمٝ رشو١ض OHصبثزب ً رمش٠جب ً ، ٚثبٌزبٌٟ فئْ ل١ّخ اي PHرىْٛ صبثزخ رمش٠جبً.
2. رأص١ش إػبفخ لبػذح NaOHإٌٝ اٌّؾٍٛي إٌّظُ ، اٌّىْٛ ِٓ لبػذح ػؼ١فخ ، ٚؽبِؼٙب
ّ
اٌّشافك : ػٕذ إػبفخ NaOHرؼٕٟ إػبفخ -٘ٚ OHزا ٠ؼٕٟ ص٠بدح فٟ رشو١ض OHفٟ
-
اٌّؾٍٛي ف١خزً االرضاْ .
-
ٚفمب ً ٌّجذأ ٌٛرشبرٍ١١ٗ ، ع١ٕضاػ اٌزفبػً ٔؾٛ اٌ١غبس ٌٍزخٍض ِٓ OHاٌضائذح ِٓ إػبفخ اٌمبػذح .
ٚثبٌزبٌٟ رجمٝ ل١ّخ PHصبثزخ رمش٠جب ً .
ِٕؾٕ١بد ِؼب٠شح األؽّبع
رؼش٠فٙب:٘ٛ إٌّؾٕٝ إٌبرظ ِٓ اػبفخ رشاو١ض ل١بع١ٗ ِؼٍِٛٗ ِٓ اٌمبػذٖ اٌٝ اٌؾبِغ ٚ ل١بط اٌزغ١١ش
إٌبرظ فٟ اي pHػٕذ اٌم١بط االٌٟٚ.
اّ٘١زٙب: رٛػؼ ِٕؾٕ١بد اٌّؼب٠شٖ ٌالؽّبع ِؼٍِٛبد وض١شٖ رذي ػٍٝ دسعخ اي pHاالٌٚ١ٗ ٌّؾٍٛي
ؽبِغ HAلجً اػبفخ اٌمبػذٖ ٌٗ ، ٚاٌزٞ ٠ذي ػٍٝ رشو١ض ا٠ٛٔبد اٌٙ١ذسٚع١ٓ ، ٚ ِٕٗ ٠ؾغت صبثذ
اٌزفىه ٌٍؾبِغ اٌّؼب٠ش.
ٚػٕذ وً إػبفخ ِٓ اٌمبػذٖ رزؾذ ا٠ٛٔبد اٌٙ١ذسٚوغ١ً ِغ اٌجشٚرٛٔبد اٌؾشح ٌ١ٕزظ ِبء ، ٚ٘ىزا
٠زفىه اٌؾبِغ ، ٌٍّؾبفظٗ ػٍٝ رفىىٗ اٌّزٛاصْ، ٚثؼذ اػبفخ ٔظف اٌىّ١ٗ ِٓ اٌمبػذٖ اٌّىبفئٗ ٠ظً
اٌٝ ٔمطخ ِٕزظف اٌّؼب٠شٖ، ٚنقطة منتصف المعاٌره او نقطة نهاٌة التفاعل:
1. إٌمطخ اٌزٟ ٠ؾذس ػٕذ٘ب رغ١ش ٚاػؼ فٟ ل١ّخ pH
41
- 15. -
2. إٌمطخ اٌزٟ ٠ىْٛ اٌؾبِغ األطٍٟ لذ رفىه ٔظفٗ رّبِب ٚ ٘ىزا فبْ ٠ HAغبٚٞ ٚ Aل١ّخ
اي pHرغبٚٞ ل١ّخ ٌٍ pKؾبِغ اٌّؼب٠ش ، ثبعزّشاس اٌّؼب٠شٖ ٚ إػبفخ وّ١بد اخشٜ ِٓ
اٌمبػذٖ فبْ HAاٌّزجمٟ ٠زؾٛي رّبِب اٌٝ - Aثٛاعطخ ارؾبد ا٠ٛٔبد اٌٙ١ذسٚوغ١ً ِغ
اٌجشٚرٛٔبد اٌؾشح ٌ١ٕزظ ِبء.
ِؼب٠شح ؽبِغ أِ١ٕٟ ػؼ١ف ِغ لبػذح لٛ٠خ ٘١ذسٚوغ١ذ اٌظٛد٠َٛ
ػٕذ ِؼب٠شح لبػذح لٛ٠خ ِضً ٘١ذسٚوغ١ذ اٌظٛد٠َٛ ِغ ؽبِغ ػؼ١ف ِضً ؽبِغ أِ١ٕٟ ، ٠ٕزظ
إٌّؾٕٝ اٌزبٌٟ:
شىً ( ) ِؼب٠شح ؽبِغ أِ١ٕٟ ػؼ١ف ِغ لبػذح لٛ٠خ
ٚ٠ّىٓ رفغ١ش خطٛاد اٌّؼب٠شح ثبٌخطٛاؽ اٌزبٌ١خ:-
1. فٟ اٌجذا٠خ ػٕذ ٚعٛد اٌؾبِغ األِ١ٕٟ أٚ أٞ ؽبِغ أخش ػؼ١ف فٟ اٌذٚسق ثذْٚ إػبغخ
٘١ذسٚوغ١ذ اٌظٛد٠َٛ ٠ؾًّ 001% شؾٕبد وٙشثبئ١خ ِٛعجخ وبٌشىً اٌزبٌٟ:-
51
- 16. • سلُ(1) فٟ إٌّؾٕ١ٝ ٠ذي ػٍٝ ٚعٛد ؽبِغ فمؾ، ، ٌُٚ رؼبف إٌ١ٗ اٌمبػذح ثؼذ,
• ٚػٍ١ٗ ٠ؾًّ اٌؾبِغ األِ١ٕٟ أٚ اٌجشٚر١ٓ اٌشؾٕبد اٌىٙشثبئ١خ اٌّٛعجخ فمؾ ، ٔغجخ
اٌّئٛ٠خ ٌٍزأ٠ٓ= 0.
2. سلُ ( 2) فٟ إٌّؾٕٝ ػٕذ إػبفخ لبػذح لٛ٠خ إٌٝ اٌؾبِغ األِ١ٕٟ ، فمذد ِغّٛع اٌىشثٛوغ١ً
ثشٚرْٛ ثٕغجخ 05% فمؾ (رؼشف ٘زٖ إٌمطخ ثبعُ صبثذ اٌزأ٠ٓ (1pKa1 =2.34 ٚ )pKa
3. سلُ (3) فٟ إٌّؾٕٝ ِغ اعزّشا إػبفخ اٌمبػذح، رأ٠ٕخ 05% اٌجبل١خ ِٓ ِغّٛػخ اٌىشثٛوغ١ً
غ١ش اٌّزأ٠ٕخ ، ٚأطجؾذ ٔغجخ رأ٠ٕٙب 001%، ٚ٠ىْٛ إٌبرظ فٟ ٘زٖ اٌّشؽٍخ وبٌزبٌٟ: (ٚرؼشف
٘زٖ إٌمطخ ثبعُ ٔمطخ اٌزؼبدي اٌىٙشثبئٟ (.)IP
4. سلُ (4) فٟ إٌّؾٕٝ ػٕذ رأ٠ٓ ِغّٛػخ اٌىشثٛوغ١ً ثبٌىبًِ ، ٠جذأ اٌزأ٠ٓ ٌّغّٛػخ األِ١ٓ
3+
ٚ ، NHرفمذ 05% ِٓ ثشٚرٛٔبرٙب ، وّب ٘ٛ ِٛػؼ فٟ اٌشىً اٌزبٌٟ -:
ػٕذ ٘زٖ إٌمطخ ثذا٠خ رغ١ش اٌؾبِغ إٌٝ لبػذح. 69.6=2pKa
61
- 17. 5. سلُ (5) فٟ إٌّؾٕٝ ِغ اعزّشا إػبفخ اٌمبػذح رزأ٠ٓ 05% اٌجبل١خ ِٓ ِغّٛػخ األِ١ٓ غ١ش
اٌّزأ٠ٕخ ٚأطجؾذ ٔغجخ رأ٠ٕٙب 001% ٚ٠ىْٛ إٌبرظ فٟ ٘زٖ اٌّشؽٍخ وبٌزبٌٟ:
ٚػٕذ ٘زٖ إٌمطخ أطجؼ اٌؾبِغ لبػذح ثبٌىبًِ ، ٚ٠ؼشف ٘زا اٌزغ١١ش ثبٌّٛف١زش٠خ)
71