Diluição de Soluções e Alcalimetria
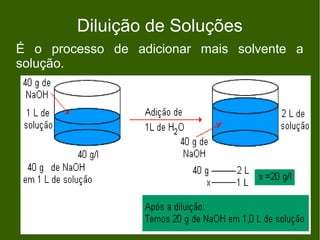
- 1. Diluição de Soluções É o processo de adicionar mais solvente a solução.
- 3. Mistura de duas soluções
- 4. 1 litro 1 litro 2 litro Solução → Final Solução I + Solução II 80g NaOH 50g NaOH 30g NaOH mf = 80 g de NaOH Vf = 2 litros Cf = 80 / 2 = 40 g/L 1 litro 1 litro 2 litro Solução I Solução II Solução → Final + 0,2 mol NaCl 0,4 mol 0,2 mol C12H22O11 0,4 mol C12H22O11 NaCl Para NaCl : C = n1 / V = 0,2 mol / 2 L = 0,1 mol/L Para C H22O11 12 : C = n1 / V = 0,4 mol / 2 L = 0,2 mol/L
- 5. Exercício 81 – página 33 Aquecendo-se 800 ml de solução 0,02 mol/L de fosfato de sódio até que o volume de solução seja reduzido de 600 ml. Qual a concentração em mol/L final? Resolução: C1 . V1 = C2 . V2 C1 = 0,02 mol/L C1 . V1 C2 = V1 = 800 ml V2 C2 = ? ? ? C2 = 0,02 . 800 800 ml – 600 ml = 200 ml 200 V2 = 200 ml C2 = 0,08 mol/L
- 6. Exercício 79 – página 33 Acrescenta-se 300 ml de água a 200 ml de solução 10 g/L de cloreto de sódio. Qual a concentração final dessa solução? Resolução: C1 . V1 = C2 . V2 C1 = 10 g/L C1 . V1 C2 = V1 = 200 ml V2 C2 = ? ? ? C2 = 10 . 200 200 ml + 300 ml = 500 ml 500 V2 = 500 ml C2 = 4 g/L
- 7. Titulação Ácido - Base Equipamentos e Soluções 1. Bureta 2. Erlenmeyer 3. Suporte Universal 4. Solução 0,1 mol/L de HCl 5. Solução de NaOH C = ?? 6. Indicador fenolftaleína.
- 8. HCl (aq) + NaOH (aq) → NaCl (aq) + H2O (l) 1 mol 1 mol 1 mol 1 mol Alcalimetria a) 0,1 mol de HCl reage Titulação completamente com 0,1 mol de NaOH. HCl (0,1 mol/L) b) no ponto de viragem o indicador muda de cor. NaOH Indicador: fenolftaleína + indicador c) no ponto de viragem nácido = nbase
- 9. ALCALIMETRIA: determinação da concentração de uma base. nácido = Cácido . Vácido nbase = Cbase . Vbase No ponto de viragem temos: nácido = nbase No menisco da bureta, devemos fazer a leitura do volume final de ácido gasto na titulação. A concentração do ácido já é No erlenmeyer o mol/L). conhecida (0,1 volume da base já é conhecido. Cácido . Vácido = Cbase . Vbase
- 10. Exercício 91 – página 37 Uma amostra de 25 ml de solução aquosa de H 2SO4 de concentração desconhecida foi titulada com uma solução aquosa 0,1 mol/L de NaOH. Determinou-se que o volume de solução básica necessário para atingir a viragem do indicador foi 20 ml. Calcule a concentração de H 2SO4 em mol/L na solução ácida. 1 H2SO4 (aq) + 2 NaOH (aq) → Na2SO4 (aq) + 2 H2O (l) Resolução: nbase= 2. nácido 2 . Ca . Va = Cb . Vb Ca = ?? Cb . Vb ácido Ca = Va = 25 ml 2. Va Cb = 0,1 mol/L 0,1. 20 = 0,04 mol/L base Ca = Vb = 20 ml 2. 25
