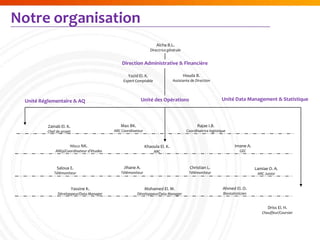
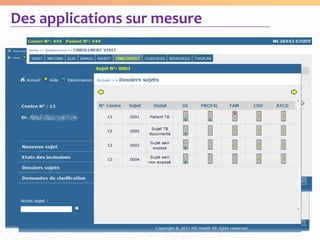
MSH, fondée en novembre 2008 et active à Casablanca, fournit des services complets de gestion d'études cliniques et épidémiologiques, ainsi qu'un accompagnement réglementaire et scientifique. Avec une équipe de 18 personnes, elle gère des projets dans des domaines thérapeutiques variés, y compris l'oncologie et la pneumologie, tout en collaborant avec des partenaires internationaux. MSH se distingue par son approche multidisciplinaire et son engagement envers la qualité et la conformité des projets.