matériaux de base pour ingénieur Test 2 Diagramme de Phases SMC3.ppt
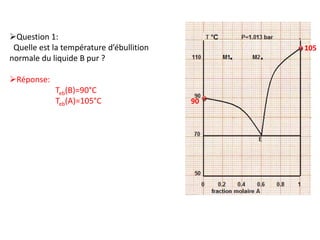
- 1. Question 1: Quelle est la température d’ébullition normale du liquide B pur ? Réponse: Teb(B)=90°C Teb(A)=105°C 90 105
- 2. Question 2: Indexer le diagramme.(sur le diagramme) Réponse: voir diagramme AL + BL (v=1) BL+ V(v=1) AL+V (v=1) V(v=2) Teb(A) Teb(A)
- 3. Question 3: Quel est le liquide le plus volatil ? Réponse: liquide B 90 105
- 4. Question 4: Colorer en rouge la courbe d’ébullition ? Réponse:
- 5. Question 5: les deux liquides A et B sont-ils miscibles en toutes proportions? Réponse: Non AL+BL
- 6. Question 6: A quelle température commence l’ébullition d’un mélange de fraction molaire xA = 0.1, sous 1 atm ? Réponse: T= 70°C 70
- 7. Question 7: Quelles sont, à 100°C et sous 1 atm, les compositions du liquide et de la vapeur en équilibre ? Réponse: XA V =0.7 XA L =1 100 X A V =0.7 X A L =1 AL+V (v=1)
- 8. Question 8: A Quelle température se termine l’ébullition d’un liquide de fraction molaire XA = 0.40 sous 1 atm ? Réponse: T=84°C 84
- 9. Question 9: A quelle température commence à se condenser une vapeur de fraction molaire XA V = 0.5 sous 1 atm ? Réponse: T=79°C 79 X A =0.5
- 10. Question 10: Colorer en bleu la courbe de rosée. Réponse: voir figure
- 11. Question 11: A quelle température se termine la condensation d’une vapeur molaire XA V = 0.6 sous 1 atm ? Réponse: T=70°C 70
- 12. Question 12: Quelle est la composition de la première goutte de liquide (en équilibre avec la vapeur) formée lors de la condensation d’une vapeur de fraction molaire XA = 0.5 sous 1 atm ? Réponse: XA L = 0 X A =0.5 X B =1 BL+ V(v=1)
- 13. Question 13: Quelle est la composition de la dernière goutte de liquide (en équilibre avec la vapeur) restant lors de la vaporisation d’un mélange de composition XB = 0.20 sous 1 atm ? Réponse: XA L =1 X A =1 AL+ V(v=1)
- 14. Question14: Tracer la courbe d’analyse thermique au point M1 BL+V (v=1) V (v=2) AL+BL V (v=0) AL+BL (v=1) Apparition des 1ieres gouttes liquides B Apparition des 1ieres gouttes liquides A Disparition de la phase vapeur AL + BL (v=1) BL+ V(v=1) AL+V (v=1) V(v=2)
- 15. Question15: Tracer la courbe d’analyse thermique au point M2 V (v=2) AL+BL V(v=0) AL+BL (v=1) Apparition des 1ieres gouttes liquides A et B Disparition de la phase vapeur AL + BL (v=1) BL+ V(v=1) AL+V (v=1) V(v=2)
- 16. Question 16: Un mélange de fraction molaire XA = 0.2 est porté à la température de 80°C, sous 1 atm . Sachant que ce mélange contient 100 moles , combien de moles de A sont transformées en vapeur à 80°C? Réponse: ML x nL = MV x nV 0.2 x nL = 0.3 x nV nL + nV = 100 d’ou: nL = 60 et nV = 40 D’autre part: XA V= nA V/nV = 0.5 D’où: nA V = 20 mol X A =0.2 L M V X A =0.5 X A =0