Exercice physique-chimie adrien thinnes
•
1 j'aime•219 vues
bien ou bien
Signaler
Partager
Signaler
Partager
Télécharger pour lire hors ligne
Recommandé
Recommandé
Procéder avec une orientation axée vers les résultats prioritaires.
On dit souvent que le « cœur » d’un département TI est son personnel… mais nous pouvons également dire qu’une partie de son « cerveau » se retrouve dans la CMDB.
Dans ce webinaire, Jean-Claude Beaudry, ITIL® Master, DevOps/DevSecOps/SRE Practitioner, PRINCE2®/PRINCE2® Agile Practitioner vous guidera à travers les étapes clés pour concevoir, implémenter et maintenir une CMDB (base de données de gestion des configurations) efficace, permettant à votre département TI de prendre des décisions éclairées, d'agir efficacement et d'automatiser les processus essentiels.
Pour voir le webinaire : https://www.technologia.com/webinaires/concevoir-et-mettre-en-place-une-cmdb-comment-reussirPrésentation Webinaire Cohésion - Concevoir et mettre en place une CMDB, comm...

Présentation Webinaire Cohésion - Concevoir et mettre en place une CMDB, comm...Technologia Formation
Contenu connexe
Dernier
Procéder avec une orientation axée vers les résultats prioritaires.
On dit souvent que le « cœur » d’un département TI est son personnel… mais nous pouvons également dire qu’une partie de son « cerveau » se retrouve dans la CMDB.
Dans ce webinaire, Jean-Claude Beaudry, ITIL® Master, DevOps/DevSecOps/SRE Practitioner, PRINCE2®/PRINCE2® Agile Practitioner vous guidera à travers les étapes clés pour concevoir, implémenter et maintenir une CMDB (base de données de gestion des configurations) efficace, permettant à votre département TI de prendre des décisions éclairées, d'agir efficacement et d'automatiser les processus essentiels.
Pour voir le webinaire : https://www.technologia.com/webinaires/concevoir-et-mettre-en-place-une-cmdb-comment-reussirPrésentation Webinaire Cohésion - Concevoir et mettre en place une CMDB, comm...

Présentation Webinaire Cohésion - Concevoir et mettre en place une CMDB, comm...Technologia Formation
Dernier (12)
Fiche - Accompagnement du travail coopératif au sein d’une équipe d’enseignan...

Fiche - Accompagnement du travail coopératif au sein d’une équipe d’enseignan...
MARTYRS DE TURQUIE – une histoire de persécution chrétienne en Anatolie.pptx

MARTYRS DE TURQUIE – une histoire de persécution chrétienne en Anatolie.pptx
EL KATRY Reem: Proposition de Programme Artistique et Exposition pour les Écoles

EL KATRY Reem: Proposition de Programme Artistique et Exposition pour les Écoles
Decret-n°19-10-du-23-janvier-2019-reglementant-lexportation-des-déchets-spéci...

Decret-n°19-10-du-23-janvier-2019-reglementant-lexportation-des-déchets-spéci...
Gestion des flux de trésorerie dans les entreprises

Gestion des flux de trésorerie dans les entreprises
Comment enseigner la langue française en Colombie?

Comment enseigner la langue française en Colombie?
Présentation sur les Risques Électriques et Leur Prévention en Algérie

Présentation sur les Risques Électriques et Leur Prévention en Algérie
Présentation Webinaire Cohésion - Concevoir et mettre en place une CMDB, comm...

Présentation Webinaire Cohésion - Concevoir et mettre en place une CMDB, comm...
En vedette
More than Just Lines on a Map: Best Practices for U.S Bike Routes
This session highlights best practices and lessons learned for U.S. Bike Route System designation, as well as how and why these routes should be integrated into bicycle planning at the local and regional level.
Presenters:
Presenter: Kevin Luecke Toole Design Group
Co-Presenter: Virginia Sullivan Adventure Cycling AssociationMore than Just Lines on a Map: Best Practices for U.S Bike Routes

More than Just Lines on a Map: Best Practices for U.S Bike RoutesProject for Public Spaces & National Center for Biking and Walking
En vedette (20)
Content Methodology: A Best Practices Report (Webinar)

Content Methodology: A Best Practices Report (Webinar)
How to Prepare For a Successful Job Search for 2024

How to Prepare For a Successful Job Search for 2024
Social Media Marketing Trends 2024 // The Global Indie Insights

Social Media Marketing Trends 2024 // The Global Indie Insights
Trends In Paid Search: Navigating The Digital Landscape In 2024

Trends In Paid Search: Navigating The Digital Landscape In 2024
5 Public speaking tips from TED - Visualized summary

5 Public speaking tips from TED - Visualized summary
Google's Just Not That Into You: Understanding Core Updates & Search Intent

Google's Just Not That Into You: Understanding Core Updates & Search Intent
The six step guide to practical project management

The six step guide to practical project management
Beginners Guide to TikTok for Search - Rachel Pearson - We are Tilt __ Bright...

Beginners Guide to TikTok for Search - Rachel Pearson - We are Tilt __ Bright...
Unlocking the Power of ChatGPT and AI in Testing - A Real-World Look, present...

Unlocking the Power of ChatGPT and AI in Testing - A Real-World Look, present...
More than Just Lines on a Map: Best Practices for U.S Bike Routes

More than Just Lines on a Map: Best Practices for U.S Bike Routes
Ride the Storm: Navigating Through Unstable Periods / Katerina Rudko (Belka G...

Ride the Storm: Navigating Through Unstable Periods / Katerina Rudko (Belka G...
Exercice physique-chimie adrien thinnes
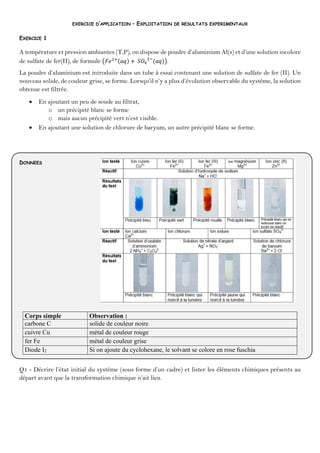
- 1. EXERCICE D’APPLICATION – EXPLOITATION DE RESULTATS EXPERIMENTAUX EXERCICE 1 A température et pression ambiantes (T,P), on dispose de poudre d’aluminium Al(s) et d’une solution incolore de sulfate de fer(II), de formule 𝐹𝑒 (𝑎𝑞) + 𝑆𝑂 (𝑎𝑞) . La poudre d’aluminium est introduite dans un tube à essai contenant une solution de sulfate de fer (II). Un nouveau solide, de couleur grise, se forme. Lorsqu’il n’y a plus d’évolution observable du système, la solution obtenue est filtrée. En ajoutant un peu de soude au filtrat, o un précipité blanc se forme o mais aucun précipité vert n’est visible. En ajoutant une solution de chlorure de baryum, un autre précipité blanc se forme. DONNEES Corps simple Observation : carbone C solide de couleur noire cuivre Cu métal de couleur rouge fer Fe métal de couleur grise Diode I2 Si on ajoute du cyclohexane, le solvant se colore en rose fuschia Q1 - Décrire l’état initial du système (sous forme d’un cadre) et lister les éléments chimiques présents au départ avant que la transformation chimique n’ait lieu.
- 2. Q2 - Parmi la liste suivante des produits suivants, quels sont ceux qui peuvent éventuellement se former. ? Pourquoi ? Cu, Cu(OH)2, Al(OH)3, Al3+, Al2O3, Fe2+, Fe3+, Fe, HO-, S, 𝑆𝑂 , H2O ………………………………………………………………………………………………………………… ……………………………………………………………………………………………………………….. ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ……………………………………………………………………………………………………………….. Q3 - A l’aide des données recensant les tests d’identification de quelques ions et corps purs, interpréter les observations faites à l’issue de la transformation chimique ainsi que les résultats des tests de caractérisation effectuée. ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ETAT INITIALEléments chimiques présents S O Fe Al Fe²+(acqueux) SO2– (acqueux) Al(solide) Les ions qui peuvent éventuellement se former sont : -Le ions Fe car si le ion Fe²+ donne tous ses électrons de valence à un autre ion alors il devient un ion Fe. -Le ion Al3+ car si le ion Al reçoit 3 électrons de valence alors il devient un ion Al3+ -Les ions Fe²+ et SO²- peuvent se former car si ils sont des ions spectateurs alors il resteront dans leurs états initiales. -Le ions S peut se former si le ion O n'existe plus. On remarque qu'en ajoutant de la soude au filtrat on obtient un précipité blanc qui signalise le fait que des ions Al3+ sont présents mais aucuns précipité vert ce qui signifie le fait qu'il n'y'a plus de ions Fe²+, en ajoutant la solution de chlorure de baryum on observe l’apparition d'un précipité blanc se qui signifie la présence de ions SO²- et qui prouve de ce fait que ce ion est un ion spectateur.
- 3. Q4 – Décrire l’état final de la transformation chimique Q5 – Identifier les produits formés et les éléments chimiques qu’ils contiennent. ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… Q6 – Identifier, parmi les espèces présentes à l’état initial, les réactifs et les espèces spectatrices en justifiant votre réponse. ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ETAT FINAL SO²-(acqueux) Al3+ (acqueux) Fe (acqueux) Les produits formés sont les ions Al3+ qui s'est formé grâce au ion Fe²+ et au ion Al ainsi que le ion SO²- qui est un ion spectateur . Les espèces présentent à l'état initial sont les ions Fe²+,Al et le ion SO²- les réactifs sont Fe²+ et le ion Al car le ion Fe²+ a donné ses 2 électrons de valence au ion Al afin qu'il devienne un ion Al3+ et le ion SO²- est un ion spectateur car il n'a pas participé à la transformation chimique.
- 4. Q7 – En déduire l’équation de la transformation chimique Q8 – Identifier le réactif limitant. Justifier votre réponse. ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… ………………………………………………………………………………………………………………… EXERCICE 2 EXERCICE 2 – N° 4 P. 122 DU LIVRE Al + So²- + Fe²+ ---------------------------------------> So²- + Fe + Al3+ 4 4 Le réactif limitant est Fe²+ car une fois qu'il a donné ses 2 électrons de valence alors il n'a plus d'électrons de valence à donné au ion Al donc la transformation chimique s’arrête elle est ,donc limiter par l'ion Fe²+.
- 5. Exercice 2: -Pour le système A le diazote est l'espèce spectatrice et le réactif limitant est le dioxygène car il donne des électrons de valence au carbone afin de crée du dioxyde de carbone . -Pour le système B l'H2O et le ion sulfates sont les espèces spectatrice et le ion cuivre (III) et le Zinc métal sont les réactifs. Exercice 4: 1) Les 2 produits formés sont ceux qui ne sont pas présent dans l'état initial donc c'est H₂ et Zn²+. 2)Le réactif pour Zn²+ est est H+ et le réactif pour H₂ est Zn. 3)a. Le réactif totalement consommé est Zn. b.C'est un réactif limitant. Les 2 espèces spectatrices sont Cl et H2O.