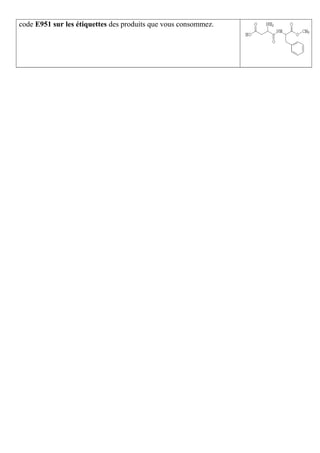
Le document décrit un protocole expérimental pour synthétiser l'éthanoate d'isoamyle, une molécule d'arôme de banane, à travers plusieurs étapes de manipulation et d'observation. Il inclut également des questions de sécurité et des considérations sur les arômes synthétiques par rapport aux arômes naturels, ainsi que des informations sur le saccharose, le xylitol, et l'aspartame. Enfin, il aborde les implications de la consommation de sucre et des édulcorants sur la santé.