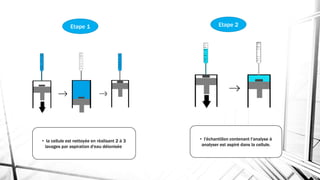
La microextraction en phase liquide (LPEM) est une technique d'extraction nécessitant de très petites quantités de solvant, permettant d'analyser divers échantillons de manière efficace et respectueuse de l'environnement. Elle est compatible avec des méthodes d'analyse comme la GC et la HPLC, et inclut des techniques spécifiques telles que la microextraction à simple goutte (SDME) pour extraire des analytes à partir de matrices liquides et gazeuses. Les avantages incluent une réduction des solvants toxiques et une analyse rapide, bien que des défis tels que l'instabilité des gouttes demeurent.