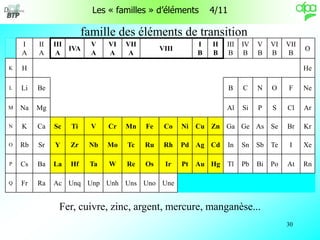
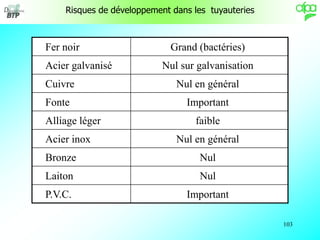
Le document discute de la chimie de l'eau, en mettant l'accent sur sa composition, ses propriétés et sa répartition sur Terre. Il explique le cycle de l'eau, la présence de diverses matières dans l'eau, ainsi que les défis associés à son traitement, tels que l'entartrage et la corrosion. Des rappels de chimie sur les familles d'éléments et leur impact sur la composition de l'eau sont également fournis.