Intégrer la présentation
Télécharger pour lire hors ligne



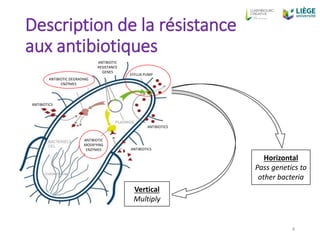
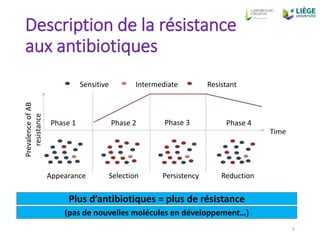



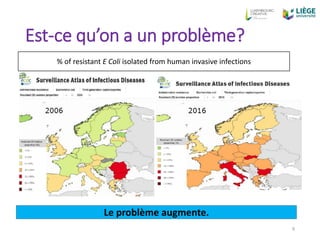

































































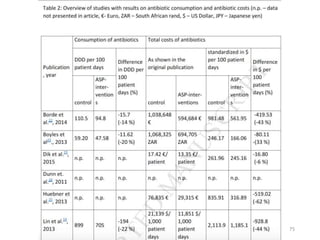




























Le document aborde la problématique croissante de la résistance aux antibiotiques dans le cadre de la santé unique 'One Health', en mettant en lumière les causes de la résistance et les efforts pour y remédier dans le domaine vétérinaire. Il souligne la contribution de l'utilisation inadéquate des antibiotiques, tant chez l'humain que chez les animaux, et discute des stratégies de réduction de leur usage. Enfin, il propose des mesures pour améliorer la prescription d'antibiotiques et encourage une approche plus préventive dans le traitement vétérinaire.







































































































