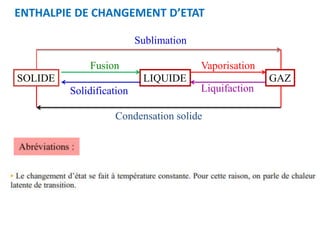
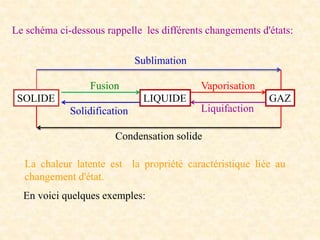
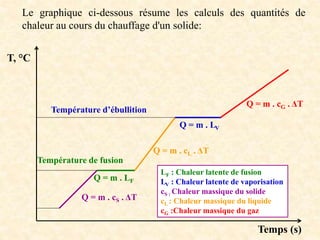
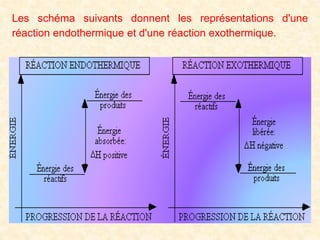
Ce document traite des principes fondamentaux de la thermochimie, en se concentrant sur les échanges de chaleur lors des transformations de l'état de la matière, la mesure des chaleurs latentes, et l'effet de ces transformations sur l'énergie interne et l'enthalpie des substances. Il explique également les concepts de réactions exothermiques et endothermiques, ainsi que les calculs associés à la chaleur nécessaire pour changer l'état d'une substance. Enfin, il présente des grandeurs thermochimiques importantes telles que les chaleurs massiques et de formation, ainsi que les chaleurs de combustion et de dissolution.