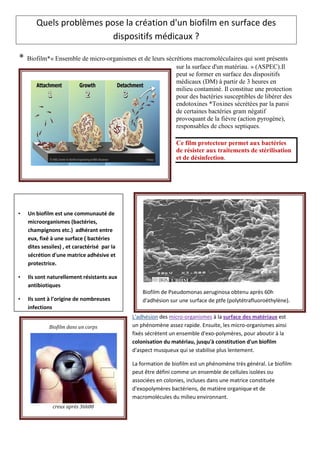
La création de biofilms sur les dispositifs médicaux pose des problèmes majeurs en raison de leur capacité à protéger les bactéries, augmentant ainsi le risque d'infections et de libération d'endotoxines. Bien que différents procédés de stérilisation aient été testés, peu d'entre eux réduisent efficacement la charge endotoxinique des biofilms. Le pré-traitement rapide et le nettoyage rigoureux sont essentiels pour prévenir la formation de biofilms sur ces dispositifs.