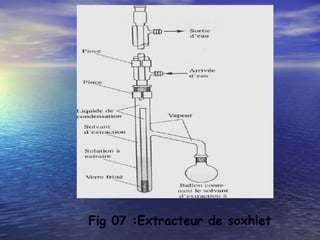
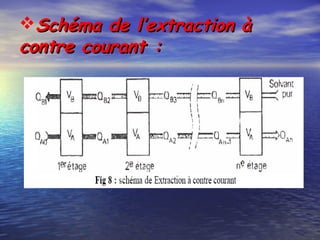
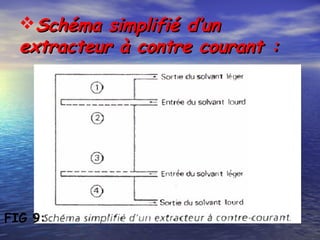
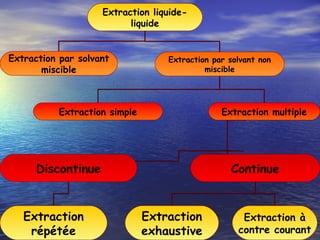
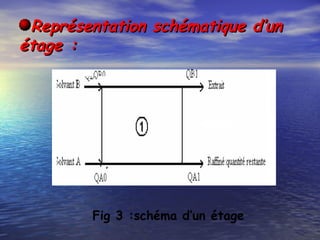
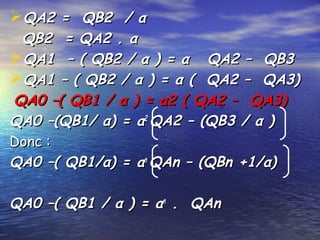Le document traite des méthodes d'extraction liquide-liquide, expliquant les principes de transfert de solutés entre deux phases à l'aide de solvants miscibles ou non miscibles. Il détaille les différentes techniques d'extraction, les critères de choix des solvants, ainsi que les calculs et notions fondamentales tels que le coefficient de partage et le rendement d'extraction. Enfin, il aborde la mise en œuvre pratique de ces méthodes tant en laboratoire qu'en milieu industriel.
















































![• Le rapport de quantité α peut êtreLe rapport de quantité α peut être
remplacé par sa valeur et leremplacé par sa valeur et le
rendement est alors exprimé enrendement est alors exprimé en
fonction de VB / VA et du coefficientfonction de VB / VA et du coefficient
de partage ou du taux dede partage ou du taux de
distribution :distribution :
11
ζ =ζ = 1 -1 -
[1 + λ (VB / VA)][1 + λ (VB / VA)]](https://image.slidesharecdn.com/extractionliquide-liquide-170616171105/85/Extraction-liquide-liquide-56-320.jpg)