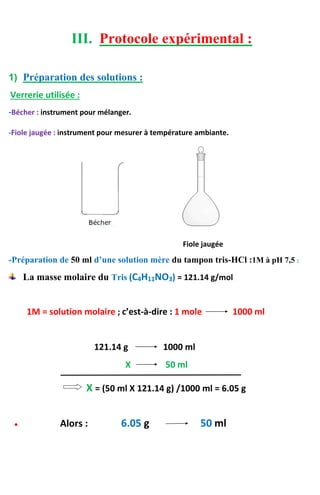
Ce document présente un rapport technique sur les techniques d'analyses biochimiques, incluant des travaux pratiques sur l'extraction et le dosage de pigments chlorophylliens des végétaux par spectrophotométrie et sur les méthodes de chromatographie. Les résultats expérimentaux montrent la quantification des pigments tels que la chlorophylle a et b, ainsi que les caroténoïdes, en utilisant des techniques analytiques variées. Il conclut que les méthodes analytiques biochimiques sont essentielles pour caractériser et quantifier les espèces chimiques dans divers mélanges.














![5) Calcul des quantités de chaque pigment :
-On utilise les équations de Lichtenthaler qui donnent la concentration de chaque
pigment en μg /ml dans la cuve :
Chl a = 12,25 (A663) – 2,79 (A647)
Chl b = 21,50 (A647) – 5,10 (A663)
Chl a+b = 7,15 (A663) + 18,71 (A647)
Car = 5,05 (A470) – (1,82 [Chl a] + 85,02 [Chl b])
198
Pour la chlorophylle a, on a :
Chl a = 12,25 (A663) – 2,79 (A647) = 12,25 x 0,57 – 2,79 x 0,23 = 6,30 μg [Chl a] /ml
-En tenant compte le facteur de dilution lors du dosage au spectrophotomètre :
On a : Facteur de la dilution = Vf/Vi = 1200μl solution / 200μl d’échantillon = 6
Alors, on doit multiplier 6,30 μg [Chl a] /ml par 6, on aura : 37,8 μg [Chl a] /ml
-Et dans un deuxième temps, par le facteur de dilution dans l’acétone (broyat dilué 5
fois par l’acétone) :
Fd = Vf/Vi = 2.5 ml / 0.5 ml = 5
Alors, on doit multiplier 37,8 μg [Chl a] /ml par 5, on aura : 189 μg [Chl a] /ml
-Puis par le volume total du broyat (4 ml) :
C’est-à-dire : 189 μg [Chl a] 0,5 ml
X μg [Chl a] 4 ml
Et sachant que : 10-6 g = 10-3 mg = 1μg
Alors : X = 4ml x 189 μg [Chl a] x 10-3 / 0,5 ml = 1,512 mg [Chl a]
-Revenons à la masse initiale de la matière sèche utilisée :
- On a : 0,4 g = 1,512mg [Chl a ] 1 g = X mg [Chl a]
-Pour 1g de matière sèche, on aura : 3,78 mg [Chl a].
-Donc on a : 3,78 mg [Chl a] / g de matière sèche.](https://image.slidesharecdn.com/rapportdutptqpagroupe2-2-180602005838/85/Rapport-du-tp-tqpa-groupe-2-2-18-320.jpg)
![- De la même façon, on calcul la quantité des autres pigments en mg par g de
matière sèche :
Pour la Chlorophylle b :
Chl b = 21,50 (A647) – 5,10 (A663) =21,5 x 0,2378 – 5,1 x 0,5685 = 2,21 μg [Chl b] /ml
-Donc on a : 1,32 mg [Chl b] / g de matière sèche
Et pour les caroténoïdes (carotène, lycopène, xanthophylle …) :
Car = 5,05 (A470) – (1,82 [Chl a] + 85,02 [Chl b])
198
= 5,05 x 0,5673 - (1,82 x 6,30 + 85,02 x 2,21) = 1,55 μg [Car] /ml
198
-Donc on a : 0,93 mg [Car] / g de matière sèche
IV. Interprétation des résultats :
Puisqu’il s’agit des feuilles vertes (siège de la photosynthèse),
c’est normal qu’on a trouvé tous les pigments. Surtout de la
chlorophylle a et de la chlorophylle b responsables de la couleur
verte.
Conclusion
La propriété de l’absorbance à une longueur d’onde
donnée confère aux pigments une couleur déterminée
lorsqu'ils sont éclairés par de la lumière blanche.](https://image.slidesharecdn.com/rapportdutptqpagroupe2-2-180602005838/85/Rapport-du-tp-tqpa-groupe-2-2-19-320.jpg)








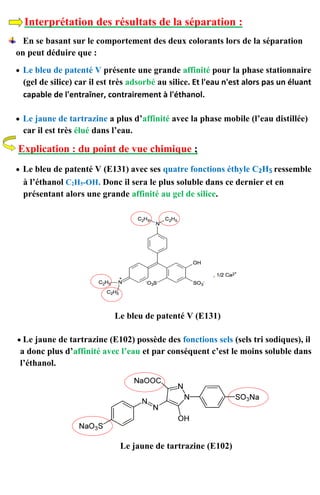


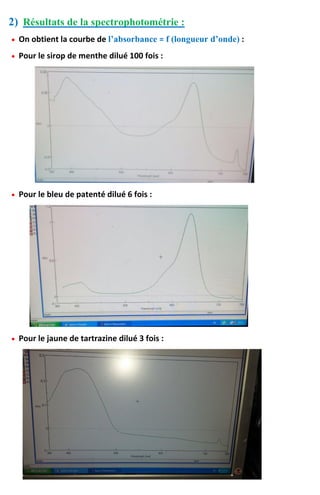
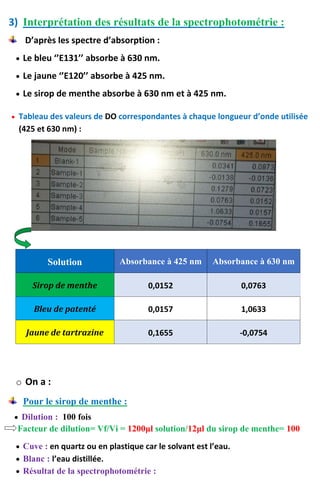

![4) Détermination de la concentration des trois préparations par
spectrophotométrie :
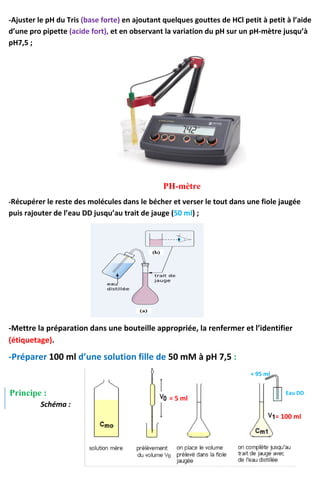
On utilise la courbe d’étalonnage donnée pour le bleu de patenté V et pour la
tartrazine à partir d’une gamme, pour déterminer les différentes concentrations
correspondantes aux valeurs de DO (absorbance) :
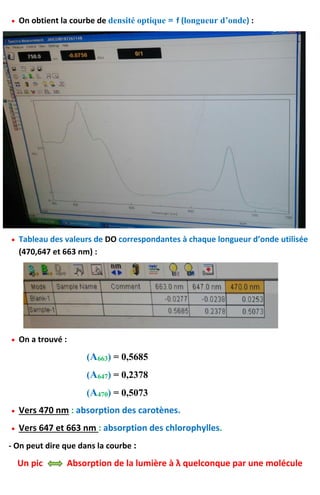
-On a trouvé que :
Pour le sirop de menthe dilué 100 fois :
o A630 = 0,08 ≈ 0,1 [Bleu de patenté V] = 1 mg/l
-En tenant compte le facteur de dilution lors du dosage au spectrophotomètre ;
- On a : Facteur de la dilution = Vf/Vi = 100
-C’est-à-dire on doit multiplier 1 mg/l par 100, on aura : 100 mg/l
Donc on a : 100 mg de Bleu de patenté V / L de sirop de menthe.
o A425 = 0,02 [Jaune de tartrazine] = 0,5 mg/l
-En tenant compte le facteur de dilution lors du dosage au spectrophotomètre ;
- On a : Facteur de la dilution = Vf/Vi = 100
-C’est-à-dire on doit multiplier 0,5 mg/l par 100, on aura : 50 mg/l
Donc on a : 50 mg de jaune de tartrazine / L de sirop de menthe.
A Bleu = 1
A Jaune =0,2
A 630 de Sirop de menthe =0,1
A 425 de sirop de menthe = 0,02](https://image.slidesharecdn.com/rapportdutptqpagroupe2-2-180602005838/85/Rapport-du-tp-tqpa-groupe-2-2-35-320.jpg)
![Pour le bleu de patenté V dilué 6 fois :
o A630 = 1 [Bleu de patenté V] = 6 mg/l
-En tenant compte le facteur de dilution lors du dosage au spectrophotomètre ;
- On a : Facteur de la dilution = Vf/Vi = 6
-C’est-à-dire on doit multiplier 6 mg/l par 6, on aura : 36 mg/l
Donc on a : [Bleu de patenté V] = 36 mg / L
Pour le jaune de tartrazine dilué 3 fois :
o A425 = 0,2 [jaune de tartrazine] = 5 mg/l
-En tenant compte le facteur de dilution lors du dosage au spectrophotomètre ;
- On a : Facteur de la dilution = Vf/Vi = 3
-C’est-à-dire on doit multiplier 5 mg/l par 3, on aura : 15 mg/l
Donc on a : [jaune de tartrazine] = 15 mg / L
5) Les facteurs de dilution des deux colorants après chromatographie :
On a : Ci. Vi = Cf. Vf Ci/Cf = Vi/Vf
Pour le bleu de patenté :
Facteur de la dilution =Ci/Cf =100/36= 2,77
Pour le jaune de tartrazine :
Facteur de la dilution =Ci/Cf =50/15= 3,33
6) Détermination du volume des éluants utilisés pendant les élutions :
On utilise : Vi = 100 µl :
Pour le bleu de patenté : l’éluant est l’éthanol ;
On a : Fd = Vf/Vi =Ci/Cf = 2,77 Vf = Vi x Fd = 100 x 2,77 = 277 µl
Pour le jaune de tartrazine : l’éluant est l’eau distillée ;
On a : Fd = Vf/Vi =Ci/Cf = 3,33 Vf = Vi x Fd = 100 x 3,33 = 333 µl](https://image.slidesharecdn.com/rapportdutptqpagroupe2-2-180602005838/85/Rapport-du-tp-tqpa-groupe-2-2-36-320.jpg)


