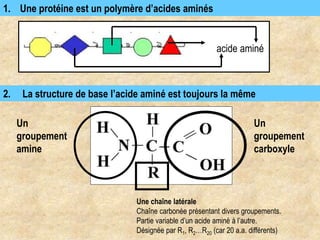
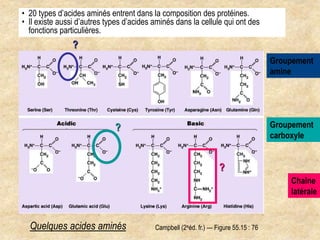
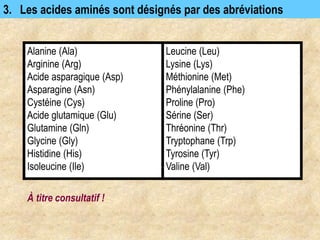
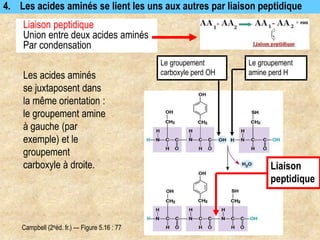
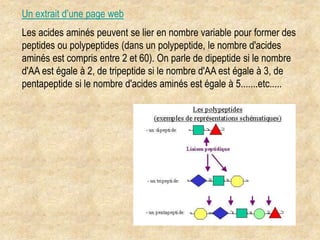
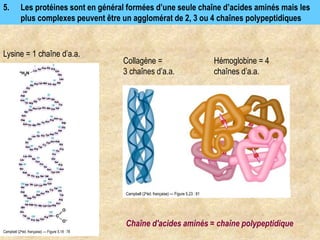
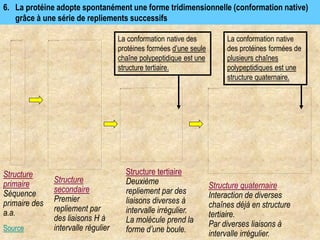
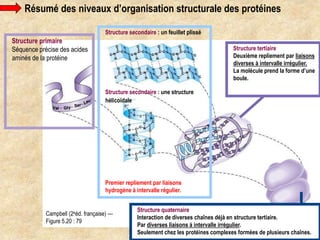
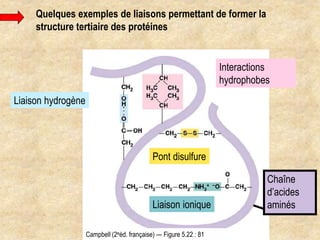
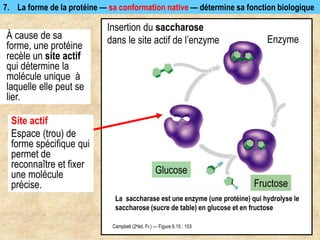
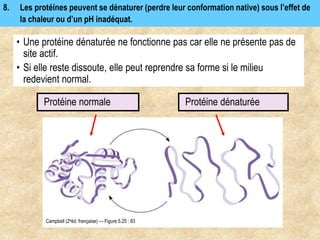
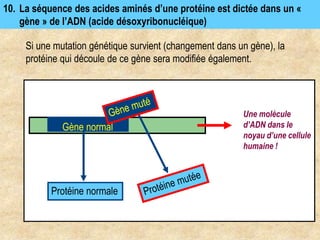
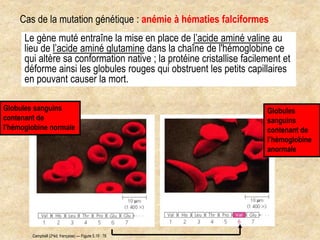
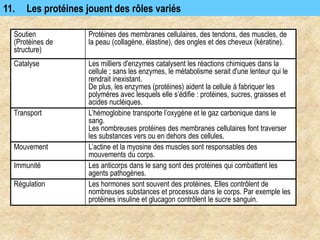
Les protéines sont des polymères d'acides aminés déterminant leur structure et fonction, avec la séquence d'acides aminés dictée par les gènes de l'ADN. Elles adoptent une conformation tridimensionnelle essentielle à leur activité biologique, mais peuvent se dénaturer sous certaines conditions, perdant ainsi leur fonction. Les protéines jouent des rôles variés tels que le soutien, la catalyse des réactions chimiques, le transport, le mouvement et la régulation des processus corporels.