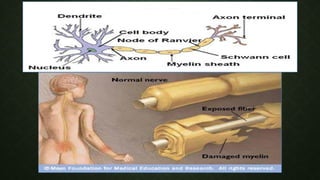
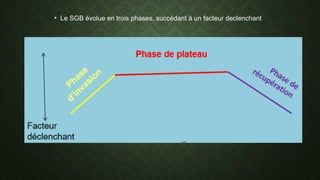
Le syndrome de Guillain-Barré est une polyradiculonévrite aiguë caractérisée par une démyélinisation des nerfs périphériques, entraînant des déficits moteurs et sensitifs progressifs. Il se développe généralement après une infection et évolue en trois phases : extension, plateau et récupération, avec une prise en charge incluant des traitements symptomatiques, plasmaphérèse et immunoglobulines intraveineuses. La neurologie préopératoire et la gestion anesthésique doivent être adaptées en raison de la dysautonomie fréquente chez ces patients.