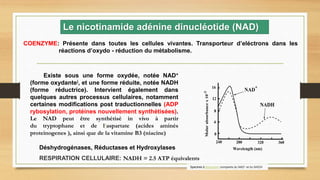
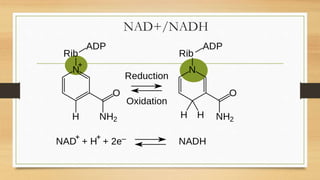
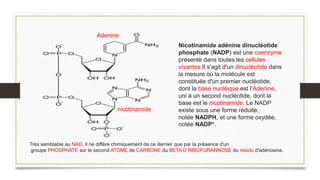
Le document aborde la biochimie microbienne en se concentrant sur le métabolisme énergétique des microorganismes, y compris le catabolisme des glucides et d'autres composés organiques. Il présente les différentes voies métaboliques, les réactions enzymatiques, et leur rôle dans la production d'énergie et de biomasse. Enfin, il souligne l'importance des coenzymes comme le NADH et le NADPH dans les processus biochimiques cellulaires.