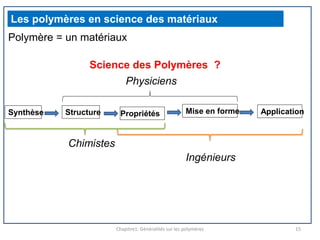
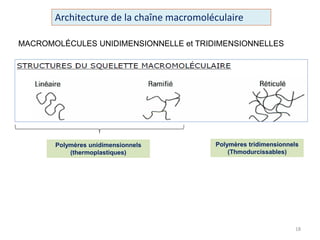
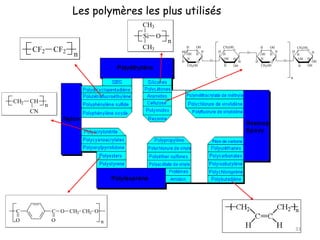
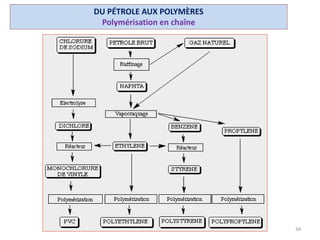
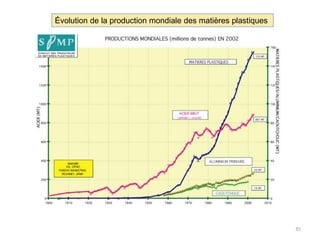
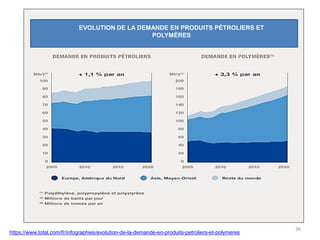
Le document retrace l'histoire et les développements des polymères en chimie, en mettant en lumière des figures clés comme Hermann Staudinger, qui a introduit le concept de macromolécule en 1922, et les découvertes majeures dans les années 50 par Karl Ziegler et Giulio Natta. Il décrit également les différentes classes de polymères, leur synthèse, ainsi que les aspects physiques et chimiques qui déterminent leur utilisation industrielle. Enfin, il souligne l'importance croissante des polymères dans diverses applications modernes grâce à leurs propriétés uniques et variées.