Le document présente un cours sur les matériaux et leur structure, abordant des concepts tels que les classes de matériaux, leurs propriétés, et leur utilisation dans diverses applications. Il décrit également la structure atomique, les types de liaisons chimiques, et la construction de structures cristallines. Enfin, il traite des aspects économiques et de la disponibilité des matériaux dans l'industrie.















































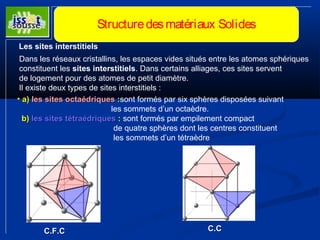
![Structure des matériaux Solides
Directions cristallographiques
Si l'un des noeuds correspond à l'origine
du réseau, on peut désigner la rangée par
les coordonnées u, v et w du noeud le plus
proche de l'origine appartenant à la droite.
Ces rangées sont notées [u,v,w] et l'ensemble
des rangées se déduisant les unes des autres
par des opérations de symétrie constitue une
famille de rangée et se note <u,v,w>.
http://nte.enstimac.fr/SciMat/co/SM_uc1-4-2.html](https://image.slidesharecdn.com/coursmatriaux2010-2011chapitre1-140831112158-phpapp01/85/Cours-Sciences-des-Materiaux-2010-2011-50-320.jpg)