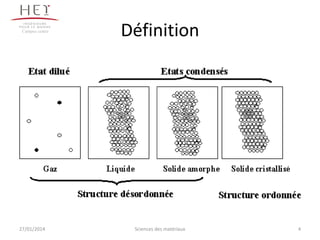
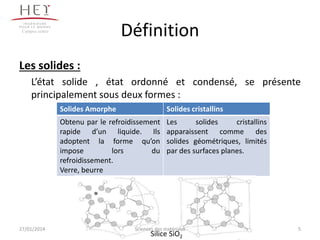
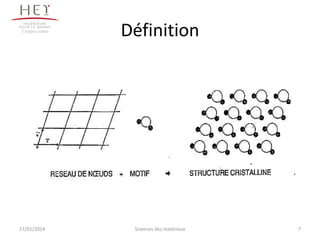
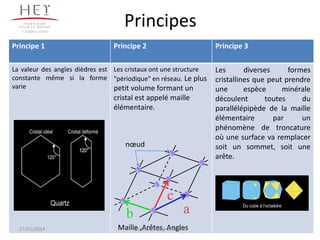
Le document présente une étude approfondie sur les solides cristallisés, incluant leur structure, les défauts cristallins, et les systèmes cristallins. Il décrit des concepts clés tels que la cristallographie, les mailles élémentaires, et la déformation plastique des cristaux. Les différents systèmes cristallins et leurs caractéristiques sont également abordés, ainsi que les impacts des défauts sur les propriétés des matériaux.