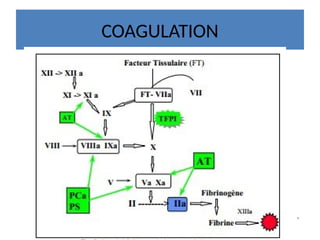
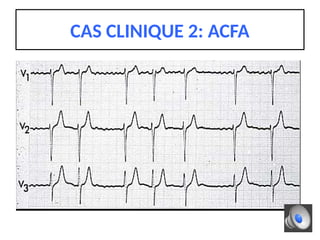
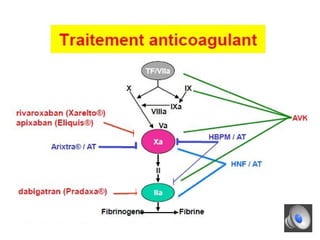
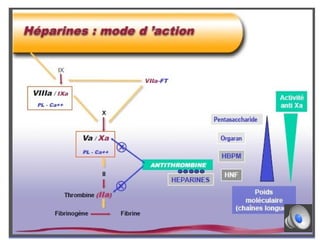
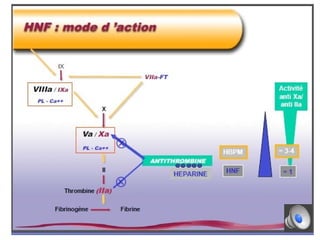
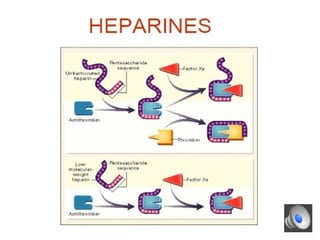
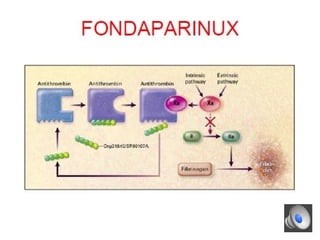
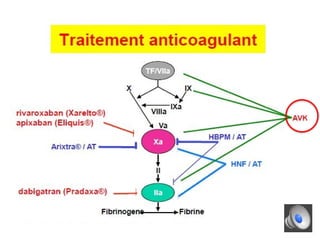
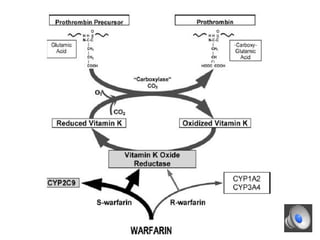
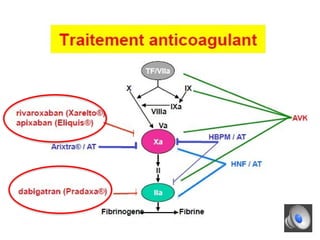
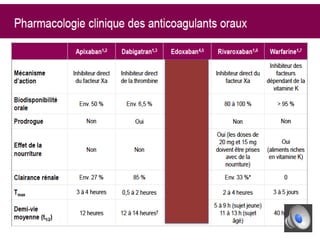
Le document aborde la gestion des anticoagulants, notamment pour un patient de 50 ans avec fibrillation atriale sous traitement antituberculeux, qui a présenté un sous-dosage des anticoagulants. L'héparine et les antivitamines K (AVK) sont expliquées, ainsi que les interactions médicamenteuses, la surveillance biologique, et les ajustements nécessaires. Une attention particulière est portée sur les anticoagulants oraux directs et leur efficacité par rapport aux AVK dans le contexte de la cardiologie.