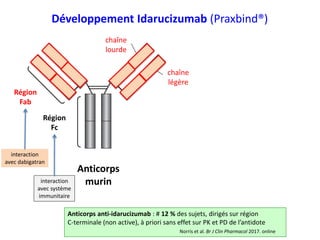
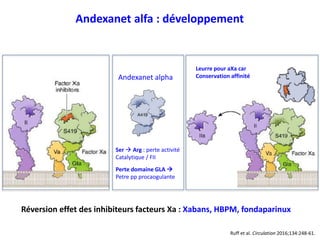
Le document traite du développement clinique des antidotes pour les anticoagulants oraux directs (AOD) comme le dabigatran. Il présente des données sur l'efficacité des antidotes, en particulier l'idarucizumab, et discute des implications des surdosages et des situations cliniques critiques. Les résultats montrent que l'idarucizumab est efficace pour inverser les effets du dabigatran, mais que des considérations de dose et de pharmacocinétique sont cruciales dans des contextes particuliers.










![Albaladejo et al. Anesthesiology 2017;online.
Expérience clinique / réversion non spécifique : GIHP-NACO
DABIGATRAN
n=207
RIVAROXABAN
n=472
APIXABAN
n=53
81 77 78âge
Juin 2013 – nov 2015:
AOD / FA > 90 %
22 % 10 % 19 %ClCr < 30 ml/mn
17 % 17 % 21 %antiplaquettaire
162 [3-3500] 124 [0-1250] 111 [18-527]C(t) ng/ml (60 % pts)
7.4 %MACE
14 %Décès tte cause
12 %• décès sur GIB
28 %• décès sur HIC
28 % / 10 %CCP (> 40 U/kg) / CCPa
0 % / 0 % / 5 %Idarucizumab / rFVIIa / ac. Tranex.
44 % / 37 %Efficacité totale / partielle sur Hgie
24 %Geste hémostatique mécanique](https://image.slidesharecdn.com/smmvantidote2017mismitidef1-170721075803/85/SMMV-Marrakech-2017-15-320.jpg)





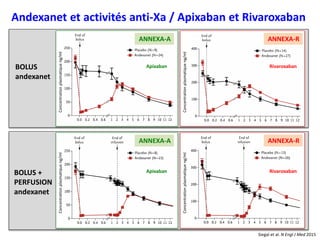
![Rivaroxaban : n = 26 Apixaban : n = 20
> 7 h post-dose AOD : bolus 400 mg + perf /2H 480 mg
< 7 h post-dose AOD : bolus 800 mg + perf /2H 960 mgDose d’Andexanet
fin de
bolus
fin de
perf H2
H4 H8 H12basal fin de
bolus
fin de
perf H2
H4 H8 H12basal
277 17 31 178 127 98 150 10 13 103 107 100
Efficacité de l’Andexanet-α : étude ANNEXA-4
Connolly et al. N Engl J Med 2016;375:1131-41.
Efficacité clinique bonne/excellente
81 % [IC95% 61-93]
Efficacité clinique bonne/excellente
75 % [IC95% 51-91]
N = 67 - 77 ans GIB = 49% - HIC = 42% - autres = 9% andexanet à 5h ± 2 / admission](https://image.slidesharecdn.com/smmvantidote2017mismitidef1-170721075803/85/SMMV-Marrakech-2017-23-320.jpg)


![[Dabigatran initiale]
< 500 ng / ml
[Dabigatran initale]
> 500 ng / ml
Dabigatran libre post-bolus # 0 pour 24 heures
contrôle c(t) précoce (H12) si insuf. rénale sévère
• si Hgie non contrôlée ou CNS Hgique /geste invasif
mesures habituelles / Hgie ± réversion si c(t) > 0
Dabigatran libre post-bolus # 0 temporairement (< H4 - H8)
• Si insuf. rénale aigue ou IRC sévère selon risque hgique
suivi précoce c(t) et envisager 2ème bolus et EER
• Si Hgie non contrôlée ou CNS Hgique / geste invasif
dosage c(t) et 2ème bolus ± EER
réversion non spécifique (CCP >> aCCP >> rFVIIA)
mesures habituelles / Hgie
Considérations PK et interprétations personnelles
/ stratégies thérapeutiques potentielles](https://image.slidesharecdn.com/smmvantidote2017mismitidef1-170721075803/85/SMMV-Marrakech-2017-26-320.jpg)