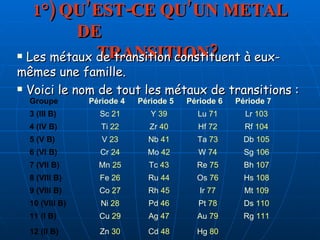
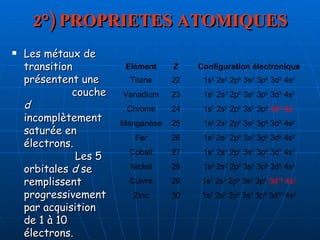
Les métaux de transition sont des éléments qui se situent entre les métaux très métalliques et les non-métaux, caractérisés par des propriétés atomiques et chimiques uniques. Ils sont utilisés dans divers domaines tels que la médecine, l'industrie et la chimie en raison de leur capacité à former des complexes colorés et à agir comme des catalyseurs. Des expériences démontrent la nature réactive de ces métaux et la formation de différents composés lors de réactions chimiques.






















![5°) EXPERIENCES Une fois la solution filtrée, ajouter de l’acide sulfurique [ 2H 3 O( +) + SO 4 ( 2-) ] concentré à Deuxième Partie :](https://image.slidesharecdn.com/lesmetauxdetransitions-12834422003379-phpapp01/85/TRANSITION-METALS-25-320.jpg)

![5°) EXPERIENCES Couples : MnO 4 ( - ) / MnO 2 ; MnO 4 (-) / MnO 4 ( 2- ) Ecrivons les demi-équations : - [ MnO 4 ( - ) + e ( - ) MnO 4 ( 2- ) ] x3 - [ MnO 4 ( - ) + 3e ( - ) + 4H( + ) MnO 4 ( 2- ) + H 2 O ] x1 D’où l’équation bilan : 3MnO 4 (-) + MnO 2 + H 2 O 3MnO 4 ( 2- ) + MnO 4 ( - ) + H ( + ) RESULTATS :](https://image.slidesharecdn.com/lesmetauxdetransitions-12834422003379-phpapp01/85/TRANSITION-METALS-27-320.jpg)







