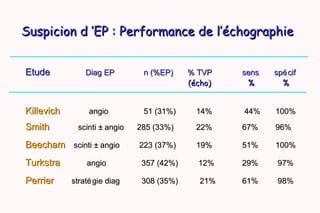
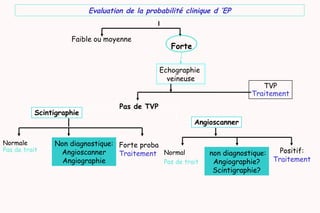
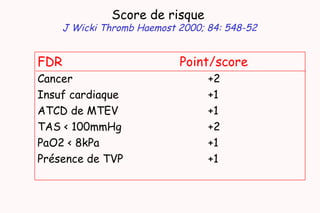
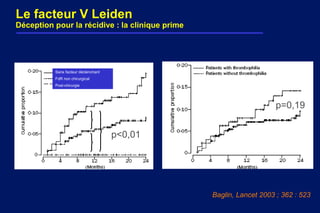
Le document traite de l'embolie pulmonaire, en détaillant les examens diagnostiques, les scores cliniques d'évaluation de la probabilité et les stratégies de traitement. Il souligne l'importance de la probabilité clinique, du dosage des D-dimères et de l'échographie veineuse dans le diagnostic et la prise en charge des cas non graves. De plus, il aborde le traitement anticoagulant, les recommandations pour la gestion des patients à domicile, ainsi que les facteurs de risque de récidive et la durée du traitement.






































![INTENSITÉ de TRAITEMENT PROLONGÉINTENSITÉ de TRAITEMENT PROLONGÉ
MVTE IDIOPATHIQUE
Evênements
annuels
Randomisation
Ridker, 2003 placebo INR 1,5 - 2
Récidive TEV
hémorragie
7,2 %
0,4 %
2,6 %
0,9%
Kearon, 2003 INR 1,5 – 1,9 INR 2 – 3
Récidive TEV
hémorragie
1,9 %
1,1 %
0,7 %
0,9 %
Crowther, 2004* INR 2 - 3 INR 3,1 - 4
Récidive TEV
hémorragie
3,4 %
6,9 %
10,7 %
5,4 %
* : étude sur le syndrome des antiphospholipides
OBJECTIFOBJECTIF
INR = 2,5 [2 - 3 ]INR = 2,5 [2 - 3 ]
Grade AGrade A
p < 0,001
P = 0,03
P = NS](https://image.slidesharecdn.com/ep-160207145039/85/Ep-42-320.jpg)















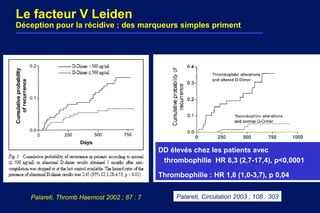

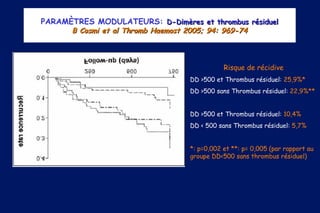
![RISQUE HÉMORRAGIQUE
Incidence annuelle d ’un saignement grave induit par AVK
- 3%/an (pour INR [2 - 3]) mortel dans 10 à 20% des cas
Influence majeure de facteurs:
- Âge > 65 ans
- Antécédent d ’hémorragie digestive
- AVC
- Alcoolisme chronique
- Diabète
- Prise concomitante d ’antiagrégants
- AVK mal équilibré
- polymorphismes sur le cytochrome P450
(Schulman, 1995, Kearon, 1999, Palareti, 1996, Landefeld 1993)
Beyth, 1998, Palareti, 1996, Landefeld, 1993, Kuijer 1999, White 1999, Margaglione 2000
De 3% à 50% par an
si plusieurs facteurs](https://image.slidesharecdn.com/ep-160207145039/85/Ep-62-320.jpg)





