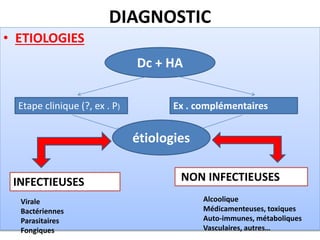
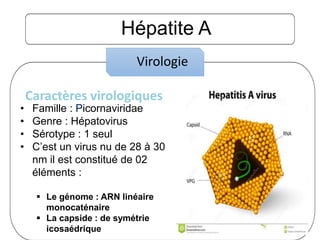
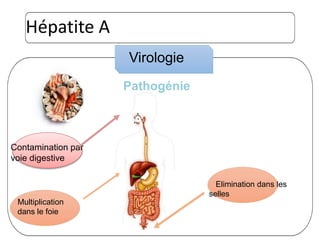
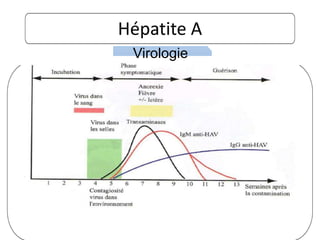
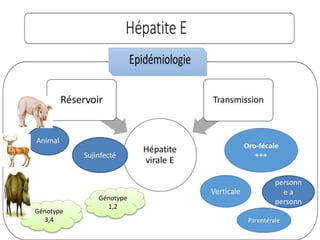
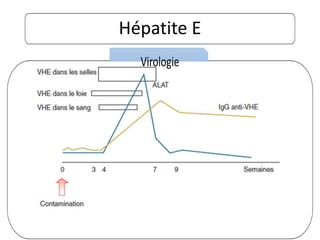
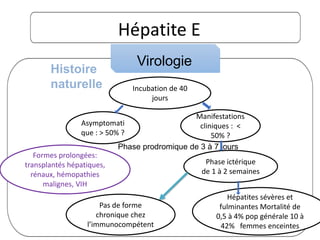
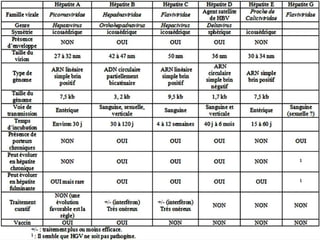
Le document traite des hépatites aiguës, abordant les aspects cliniques, biologiques et diagnostiques. Il décrit plusieurs étiologies, notamment virales, bactériennes et parasitaires, ainsi que les méthodes de diagnostic et de traitement. Il souligne également l'importance de la prise en charge rapide, en particulier pour les formes sévères et fulminantes.