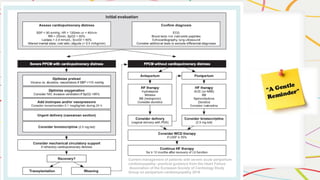
Le document discute de la cardiomyopathie du péripartum, caractérisée par une insuffisance cardiaque et une réduction de la fraction d'éjection ventriculaire gauche, survenant souvent vers la fin de la grossesse ou dans les mois suivant l'accouchement. Divers cas cliniques illustrent les complications, le traitement et l'importance d'un suivi cardiaque post-partum. Il souligne également l'absence d'un consensus sur les méthodes de gestion et les précautions durant le travail et l'accouchement pour des femmes atteintes de cette condition.