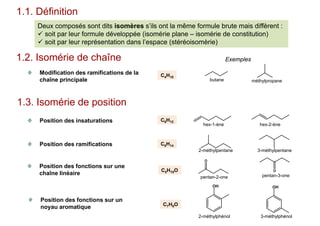
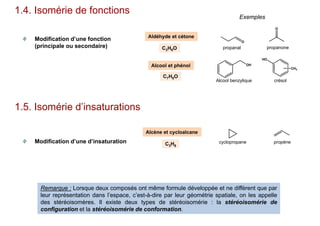
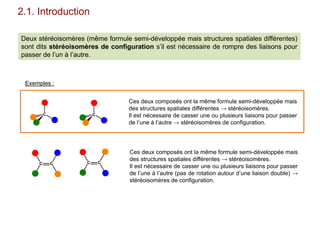
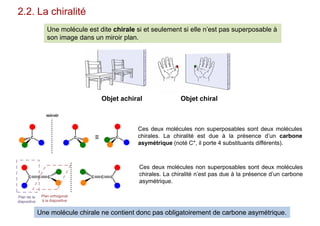
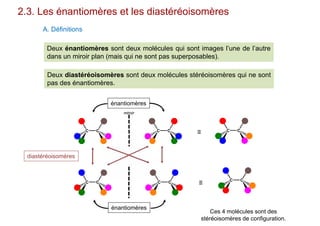
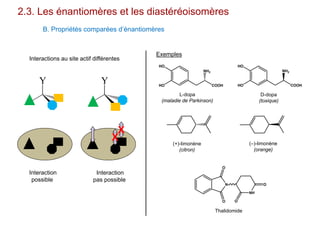
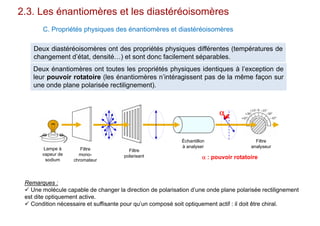
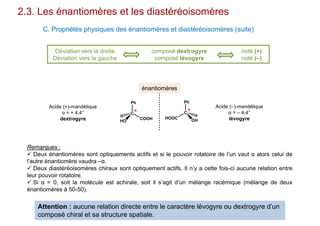
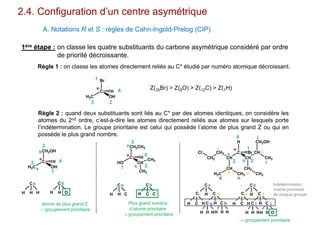
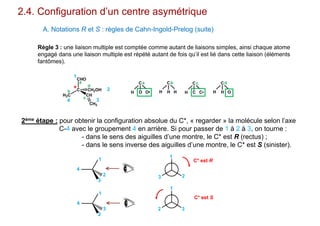
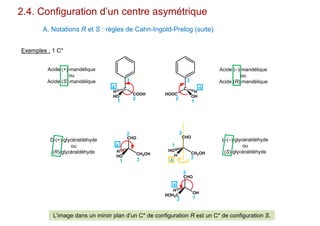
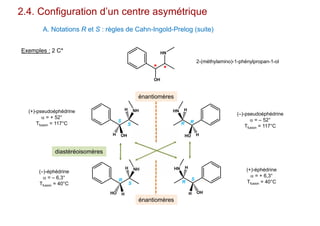
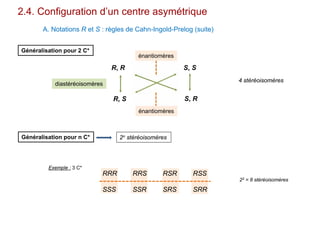
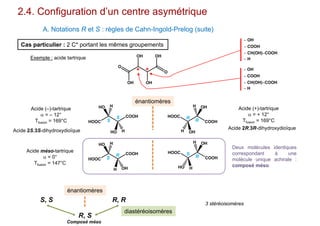
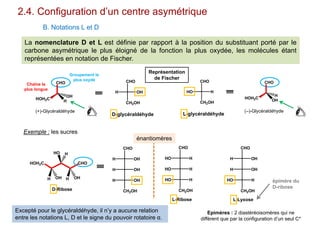
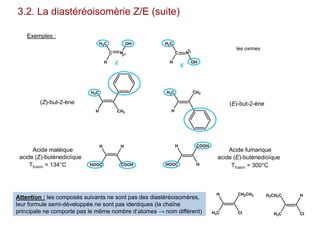
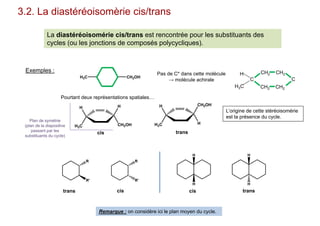
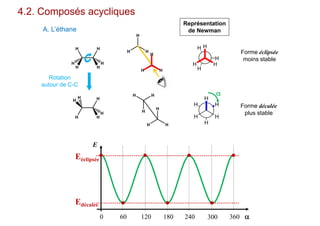
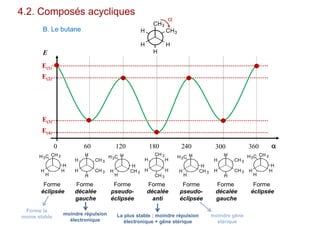
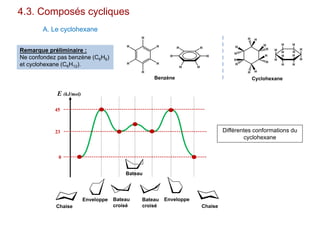
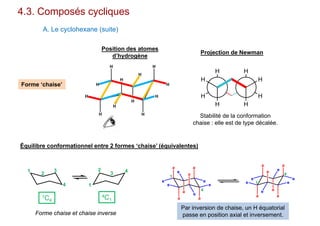
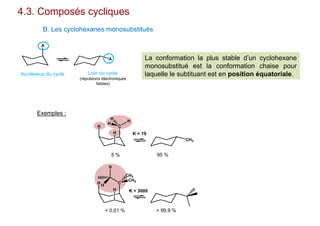
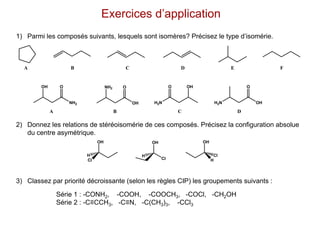
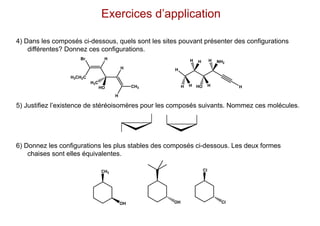
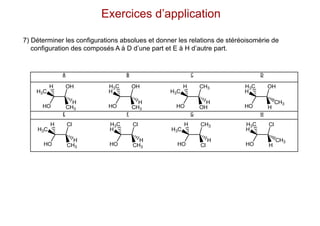
Le document traite de l'isomérie en chimie, en se concentrant sur les types d'isomérie, y compris l'isomérie plane et la stéréoisomérie de configuration et de conformation. Il explique les concepts de chiralité, d'énantiomères et de diastéréoisomères, ainsi que les règles de classification des stéréoisomères. De plus, il aborde les notations R/S, la diastéréoisomérie Z/E et cis/trans, en précisant les propriétés physiques des différents types de stéréoisomères.