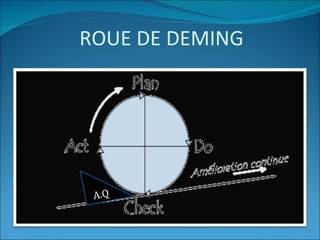
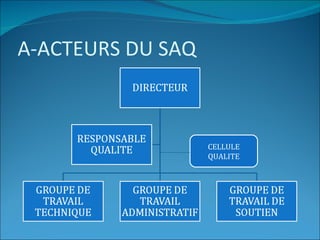
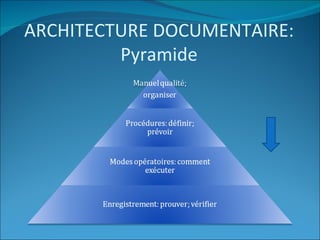
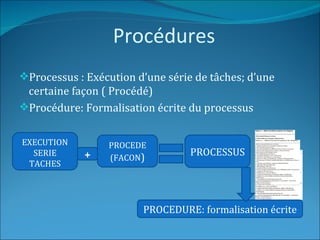
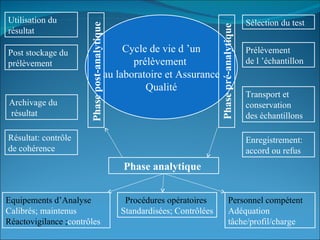
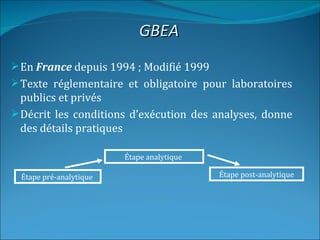
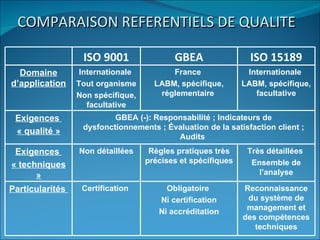
Le document traite de l'assurance qualité dans les laboratoires de biologie médicale, définissant des normes, des processus et des acteurs impliqués dans la mise en place d'un système de management de la qualité. Il souligne l'importance de garantir la qualité des prestations à travers des méthodes d'évaluation et d'audit, ainsi que la conformité aux référentiels tels que le GBEA et les normes ISO. En conclusion, la pérennisation de la qualité est présentée comme essentielle pour satisfaire aux exigences des patients et des clients.