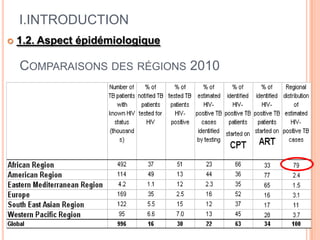
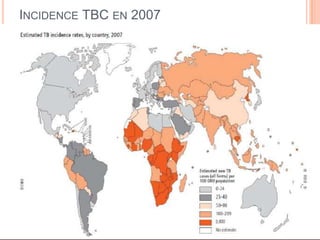
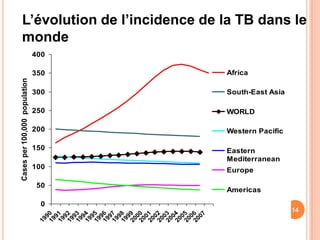
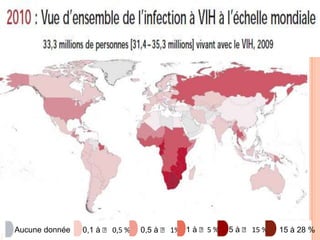
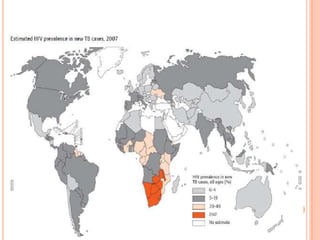
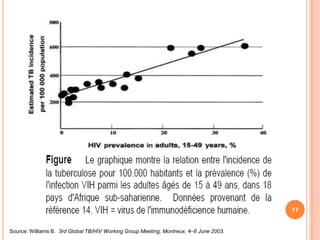
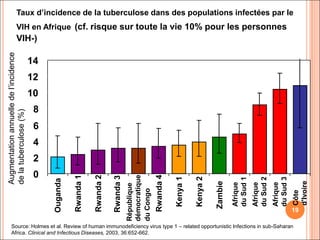
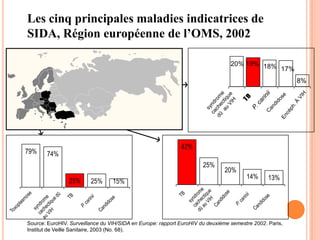
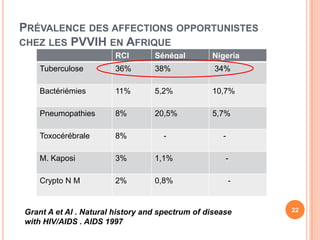
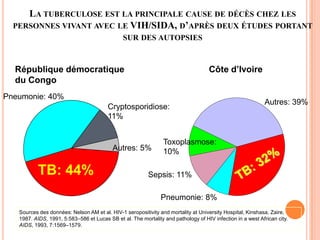
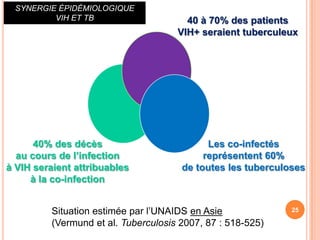
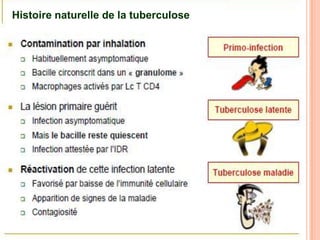
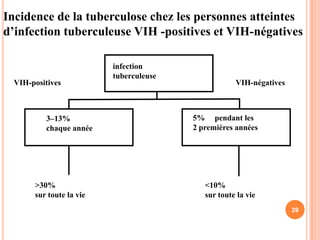
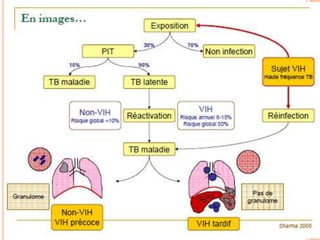
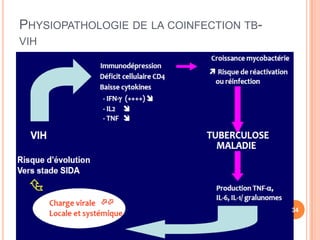
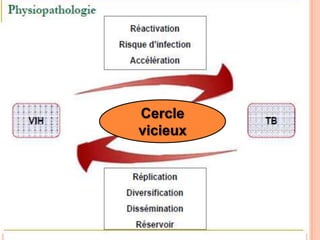
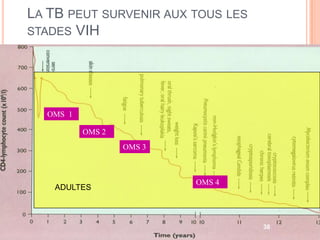
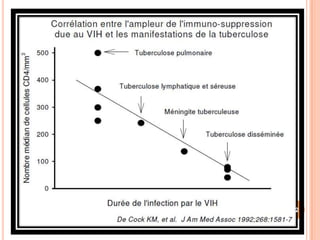
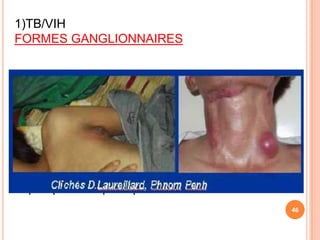
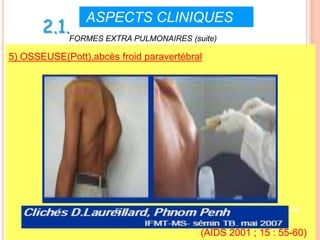
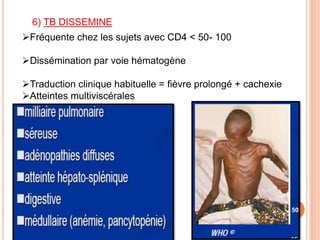
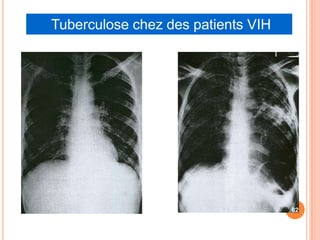
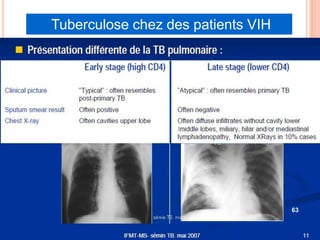
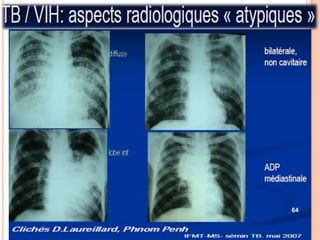
Ce document aborde la co-infection tuberculose (TB) et VIH, soulignant son importance en tant que défi de santé publique, particulièrement en Afrique subsaharienne, où 70% des cas de TB sont associés au VIH. Il décrit les particularités de diagnostic, la complexité des interactions entre les deux maladies, notamment en matière de physiopathologie, ainsi que les implications épidémiologiques et les enjeux thérapeutiques. Enfin, il souligne les taux de morbidité et mortalité alarmants liés à cette co-infection, ainsi que la nécessité de stratégies de prise en charge adaptées.