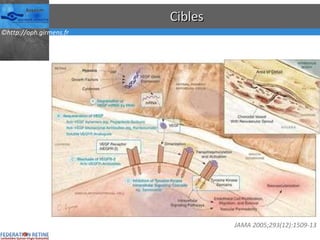
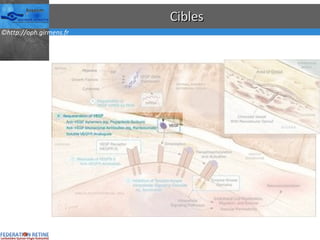
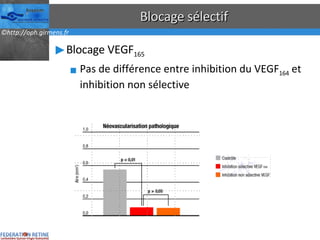
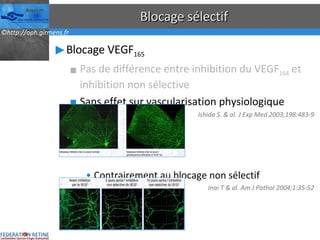
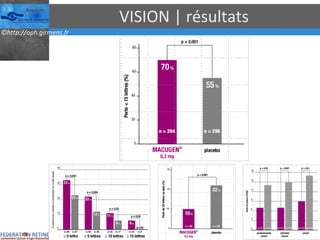
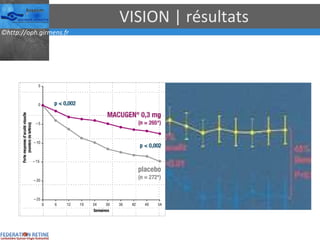
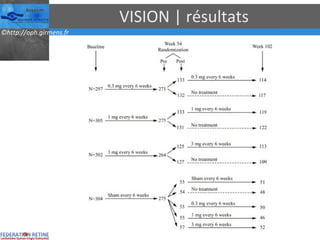
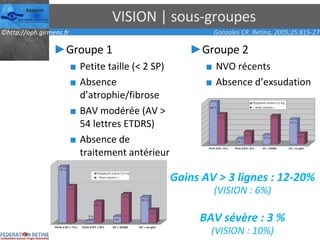
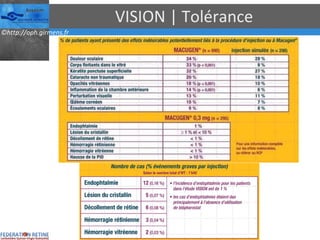
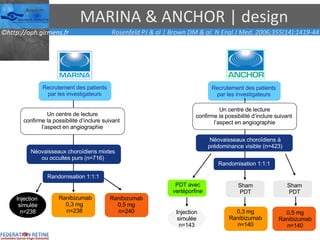
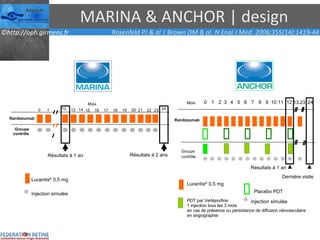
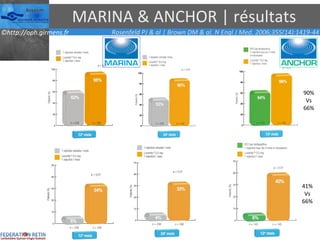
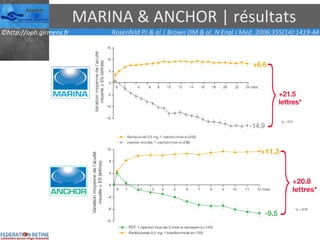
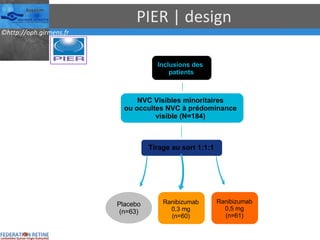
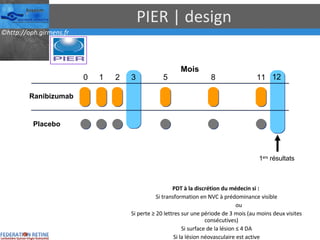
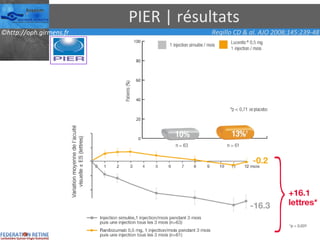
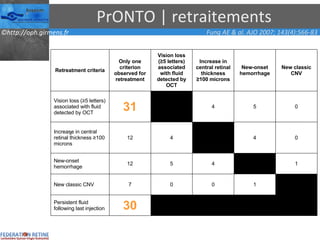
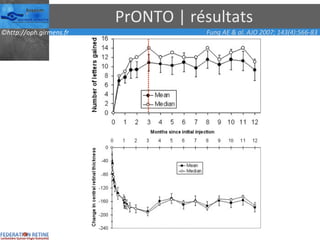
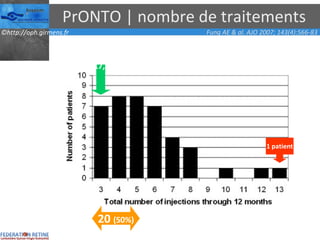
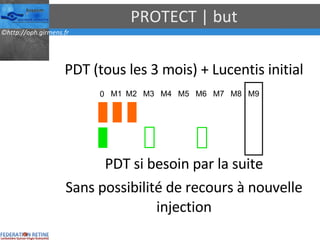
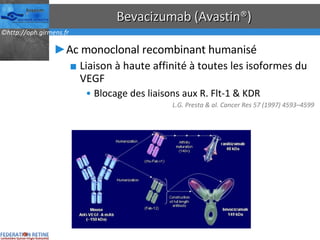
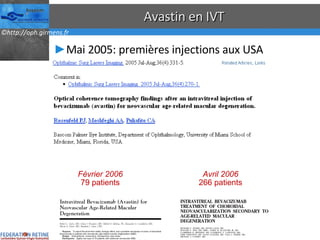
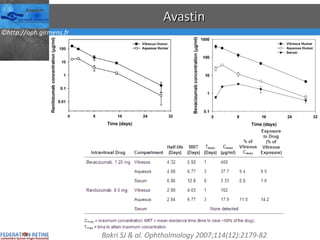
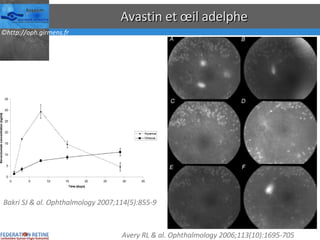
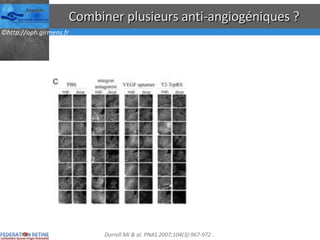
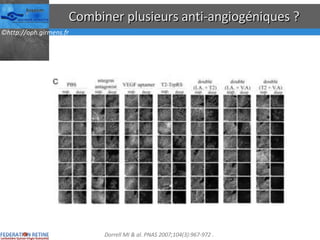
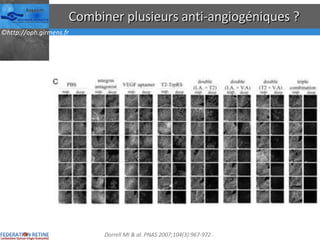
Le document traite des anti-VEGF et de leur efficacité dans le traitement des maculopathies liées à l'âge, en soulignant leur rôle dans l'angiogenèse et en fournissant des résultats d'études cliniques sur différents traitements. Il met en évidence les récepteurs VEGF, leur physiologie, et des antidotes comme le pegaptanib et le ranibizumab, ainsi que leurs effets secondaires et leur administration. Des résultats de traitements combinés et la possibilité de réduire les injections à l'aide d'outils comme l OCT sont également discutés.