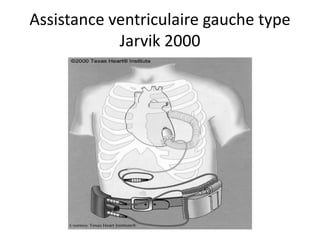
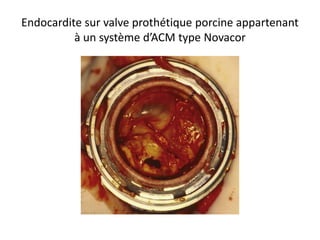
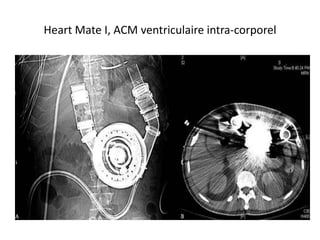
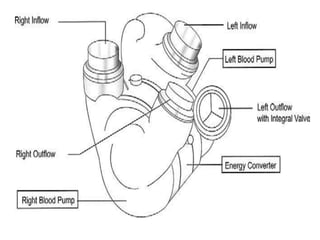
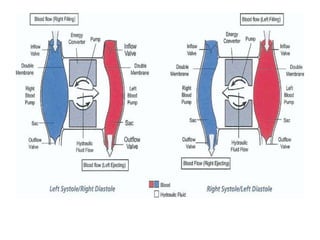
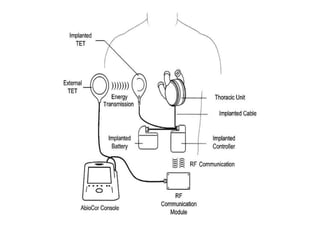
L'insuffisance cardiaque représente une épidémie mondiale croissante, avec des décès annuels et une augmentation continue de son incidence. Les dispositifs d'assistance circulatoire, y compris les cœurs artificiels partiels et totaux, offrent des options thérapeutiques prometteuses pour les patients non éligibles à la transplantation cardiaque. La recherche et le développement de ces dispositifs visent à améliorer la qualité de vie et à fournir des solutions aux patients atteints d'insuffisance cardiaque avancée.