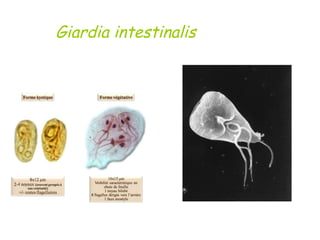
Le document traite des techniques de récolte et d'identification des protozoaires intestinaux dans les selles, précisant les méthodes de coloration et de concentration utilisées en parasitologie. Il souligne l'importance des protozoaires en tant que parasites responsables de maladies chez l'homme et les animaux, en détaillant les techniques de laboratoire pour les détecter. La conclusion insiste sur l'essor des techniques de biologie moléculaire, comme la PCR, pour une détection plus précise des espèces et génotypes de protozoaires.