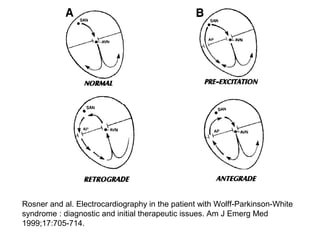
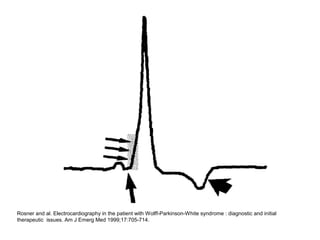
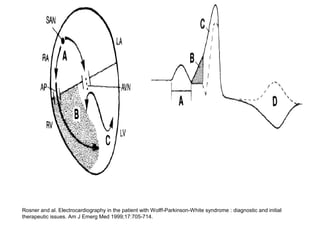
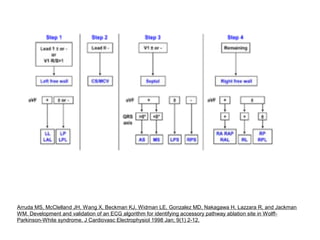
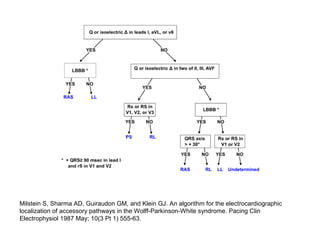
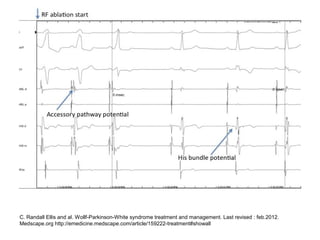
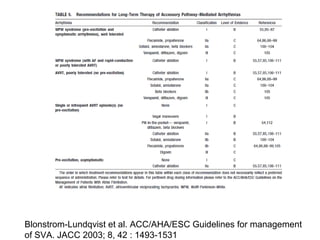
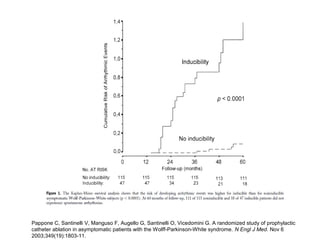
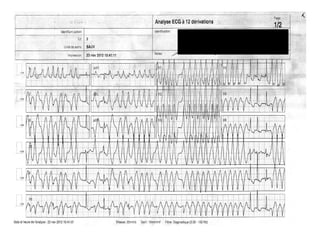
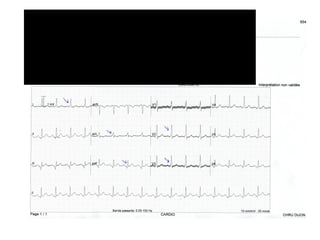
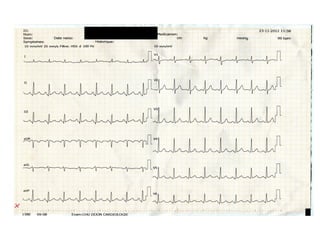
Le syndrome de Wolff-Parkinson-White est une condition cardiaque liée à la présence d'un faisceau accessoire, le faisceau de Kent, qui altère la conduction électrique et peut entraîner des tachycardies. La prévalence est faible dans la population générale mais augmente avec des antécédents familiaux; des complications comme des tachycardies et des morts subites sont possibles même chez les patients asymptomatiques. La gestion inclut un suivi régulier, des études électrophysiologiques, et potentiellement des interventions comme l'ablation du faisceau accessoire.