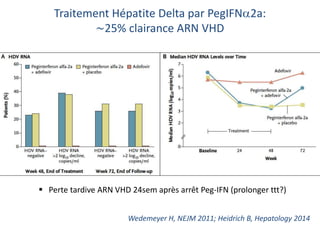
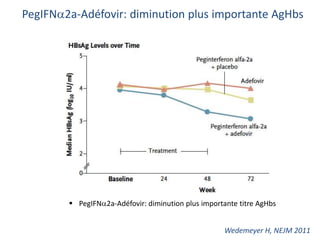
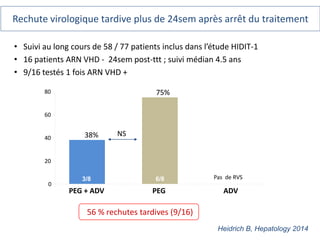
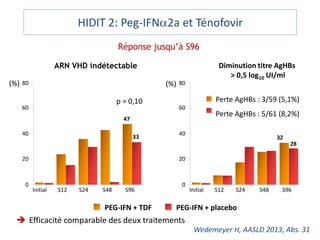
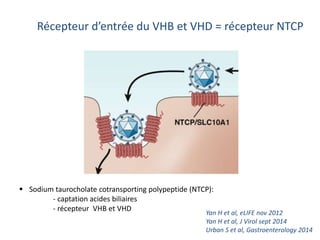
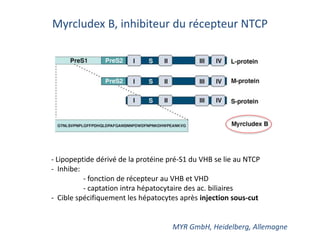
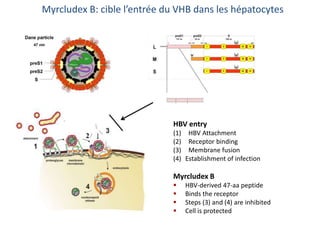
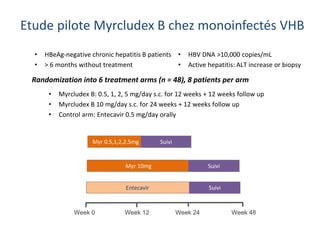
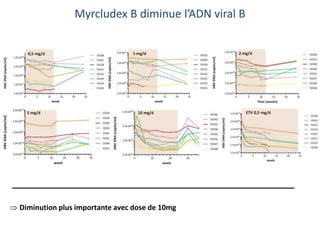
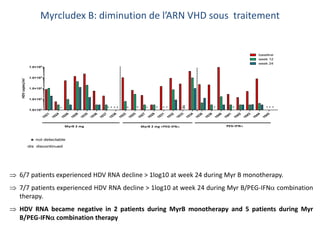
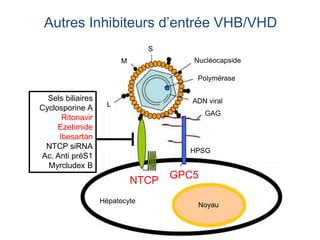
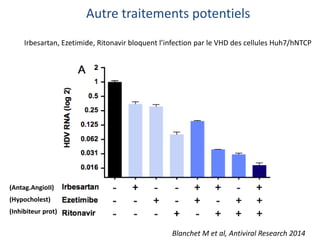
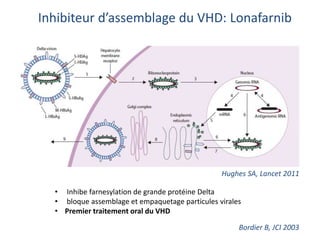
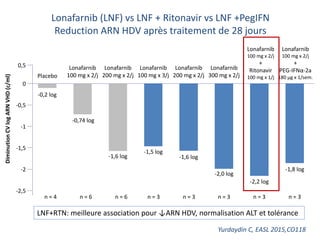
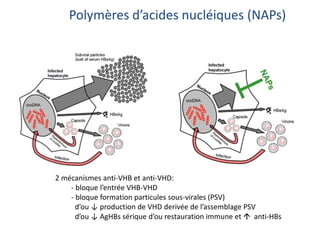
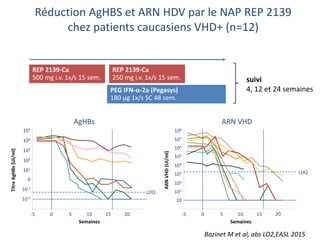
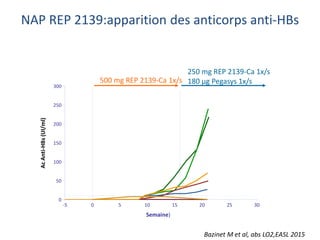
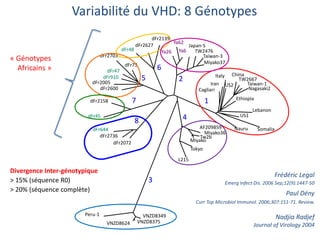
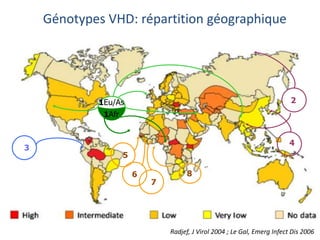
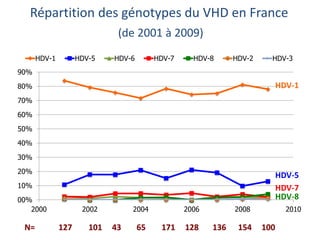
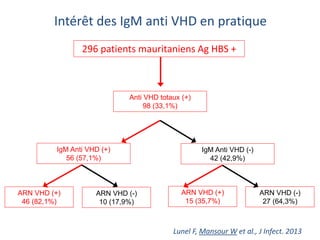
Le document analyse l'hépatite delta, en décrivant ses caractéristiques virales, son épidémiologie et son traitement actuel et futur. Il souligne l'importance de la co-infection avec le virus de l'hépatite B et la gravité des conséquences associées à l'infection par le virus delta. Enfin, il évoque les approches diagnostiques et thérapeutiques en développement pour gérer cette infection virale complexe.












![Status clinique Initial Fin de suivi
Cirrhose 28.3% 48.8%
Décompens. hépatique 14.8% 24.2%
CHC 2.7% 9.2%
Décès ou TH* - 19.1%
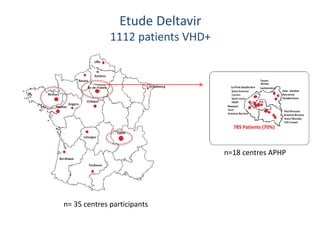
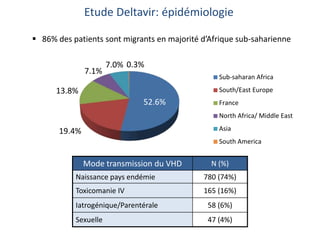
Deltavir: sévérité de l’hépatopathie
En fin de suivi:
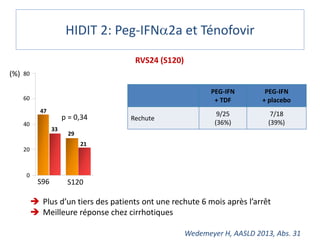
- 584 pts traités par IFN ou PegIFN
- 33% d’entre eux ARN VHD négatifs
Suivi médian : 4.4 ans [0,8-8,9]
* TH: transplantation hépatique](https://image.slidesharecdn.com/ssaokpsb6fnurlrsulrg-signature-6f006525617f2b92773dab668ca306346a0a29494921fcc7056e51c49b86a339-poli-160122161407/85/Roulo-tbis-vhd-du16-28-320.jpg)