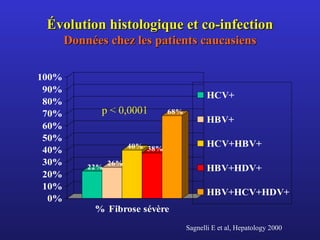
Le document examine l'impact de la co-infection par les virus de l'hépatite B et C sur la réplication virale et l'évolution clinique chez les patients. Il souligne que la co-infection influence négativement la réponse immunitaire et augmente le risque de cirrhose et de mortalité hépatique. Des données indiquent également que le choix thérapeutique doit être basé sur l'identification du virus dominant en raison de variations dans la réponse au traitement.