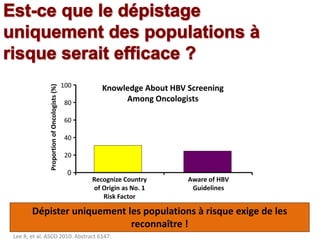
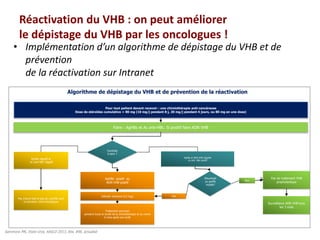
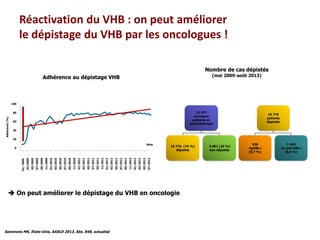
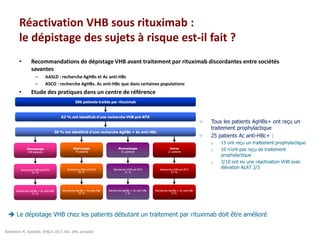
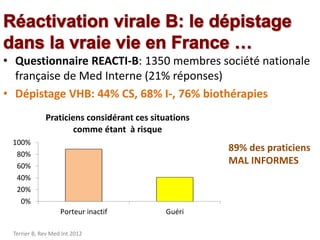
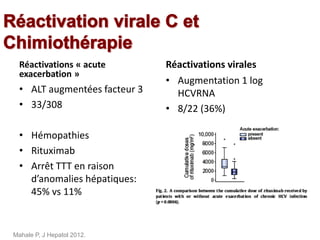
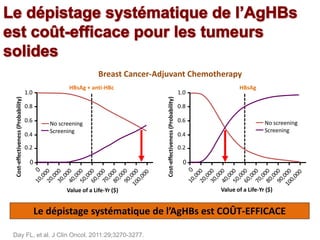
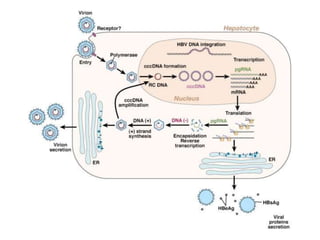
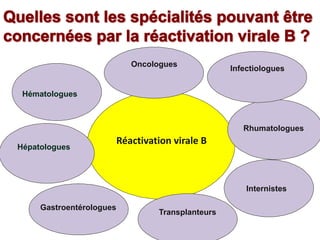
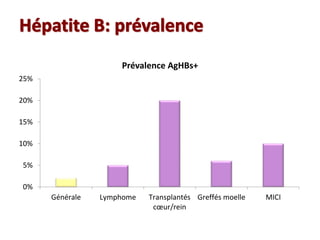
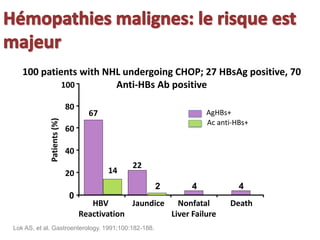
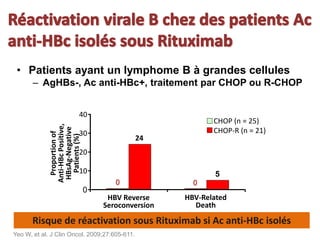
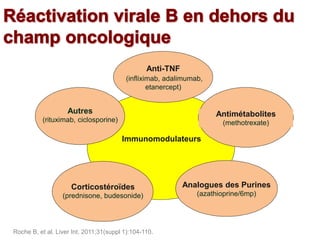
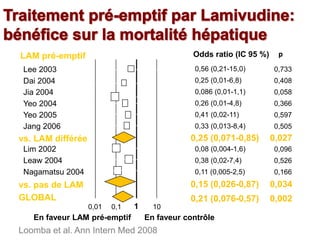
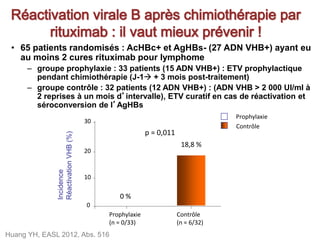
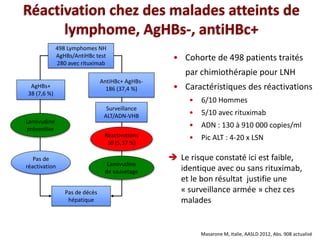
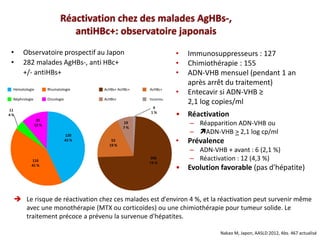
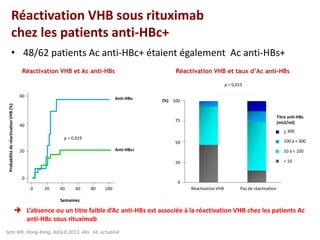
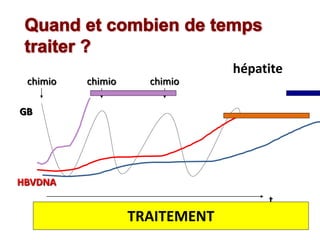
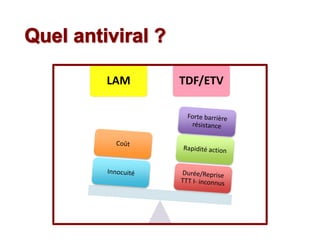
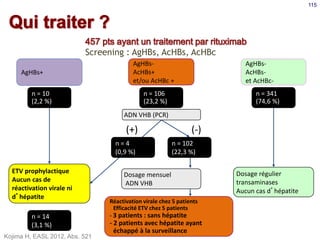
Le document traite de la réactivation du virus de l'hépatite B (VHB) chez les patients sous immunosuppresseurs, notamment durant des traitements de chimiothérapie. Il présente des données épidémiologiques, les risques associés selon le type de chimiothérapie, et les recommandations pour un traitement préventif versus curatif. Les analyses soulignent l'importance de surveiller la charge virale et d'adapter la gestion des patients porteurs du VHB en fonction de leur statut sérologique.














![Patientes AgHBs+ ayant une chimiothérapie
pour K du sein
Hépatite aiguë VHB: 21%[1]
Dosages réguliers HBVDNA, réactivation VHB:
41%[2]
Of those who flare[2]:
35% chemotherapy interruption
35% premature termination of chemotherapy
1. Kim MK, et al. Korean J Intern Med. 2007;22:237-243.
2. Yeo W, et al. J Med Virol. 2003;70:553-561.](https://image.slidesharecdn.com/lnveouaoqcw91mmoa5kg-signature-b31548432632dfa5bf97ce087c5d9eee79039615d4c2b7a1bb1d9436e5825e3f-poli-150122100817-conversion-gate02/85/Thabut-reinfection-du2015-17-320.jpg)

















![1. Khokhar OS, et al. Chemotherapy. 2009;55:69-75. 2. Lee R, et al. Curr Oncol. 2010;17:32-38.
Self-Reported HBV Screening
Practices of 131 US Oncologists[1]
Chart Review
of Actual Screening
(208 Pts at Single
Institution)[2]
Dépistage systématique TRES RARE
HBVScreening(%)
60
40
20
0
None High Risk All Actual
Screening
Rate
62
24
14 14
80
100](https://image.slidesharecdn.com/lnveouaoqcw91mmoa5kg-signature-b31548432632dfa5bf97ce087c5d9eee79039615d4c2b7a1bb1d9436e5825e3f-poli-150122100817-conversion-gate02/85/Thabut-reinfection-du2015-50-320.jpg)