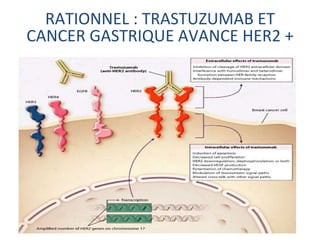
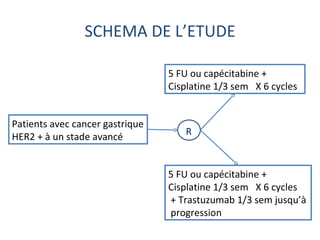
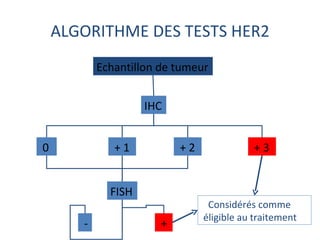
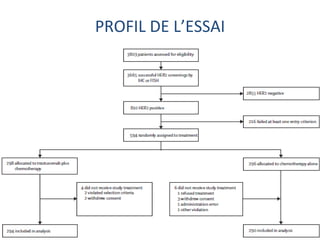
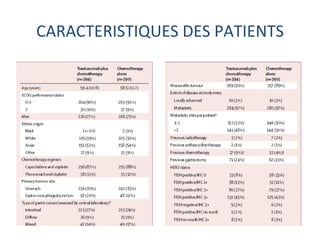
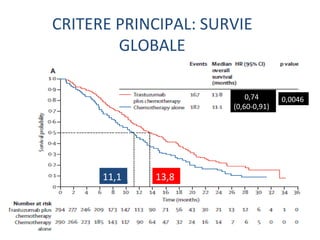
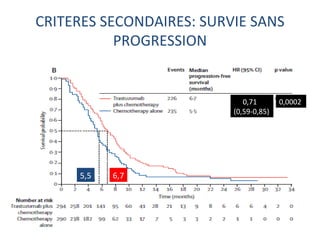
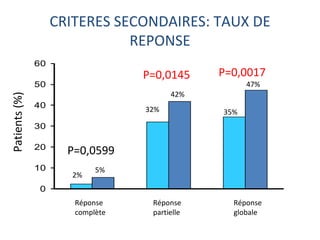
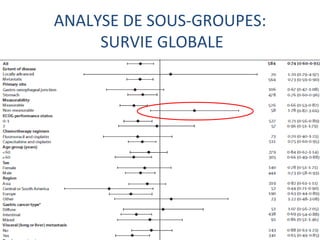
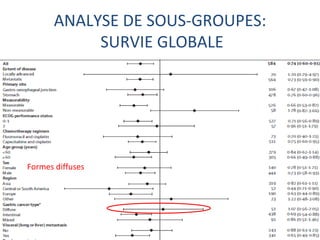
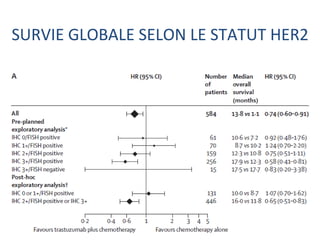
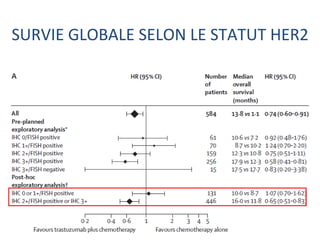
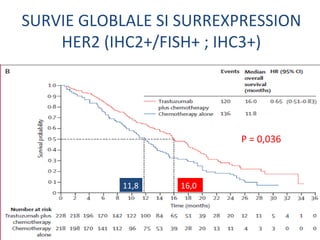
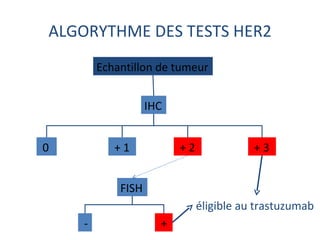
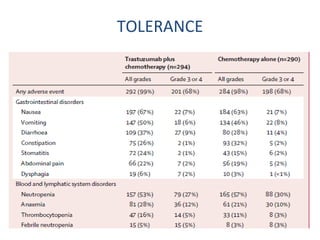
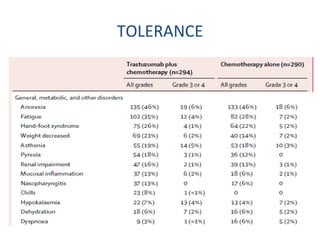
L'étude Toga a exploré l'efficacité du trastuzumab en association avec une chimiothérapie standard pour les patients atteints de cancer gastrique avancé HER2+. Les résultats montrent une amélioration de la survie globale et un bénéfice clinique, bien que les bénéfices soient jugés minimes. La nécessité d'autres essais pour optimiser les traitements et évaluer d'autres options thérapeutiques est également soulignée.