Le syndrome médiastinal est caractérisé par un ensemble de signes révélant la présence d'air, de liquide ou de tissus anormaux dans le médiastin. Plusieurs techniques d'imagerie comme la radiographie, la tomodensitométrie et l'échographie sont utilisées pour identifier ces anomalies et leur localisation. Ce document fournit également un aperçu de l'anatomie radiologique et des techniques d'exploration du médiastin.

![32-360-P-10 Syndrome médiastinal Radiodiagnostic
– le tronc veineux brachiocéphalique concave en dehors et en
bas ; il est parfois visible jusqu’en arrière de la clavicule ;
– la veine cave supérieure : elle est souvent invisible, soit parce
que confondue avec le bord droit du rachis, soit parfois masquée
par une aorte ascendante déroulée ;
– l’oreillette droite, convexe vers la droite ; elle réalise le bord
droit de la silhouette cardiaque ;
– la veine cave inférieure, oblique en haut et en dedans.
– Le bord gauche se compose de haut en bas de structures artérielles
qui sont :
– l’artère sous-clavière gauche, concave vers le bas, oblique en
haut et en dehors ;
– le bouton aortique qui correspond à la portion postérieure et
supérieure de la crosse ; c’est l’arc supérieur gauche de la
silhouette cardiomédiastinale ;
– le bord gauche du tronc de l’artère pulmonaire et l’auricule
gauche forment l’arc moyen ;
– le bord gauche du ventricule gauche constitue l’arc inférieur.
· Lignes du médiastin [10, 50, 51]
Elles représentent les contours externes du médiastin qui sont
moulés par la clarté pulmonaire. Elles ne sont visibles que
lorsqu’elles sont tangentes au rayonnement incident. Leur analyse
nécessite des clichés en haute tension, suffisamment pénétrés. Leur
non-visualisation peut être liée à une conformation particulière du
sujet ou à une incidence non tangentielle à l’interface
médiastinopulmonaire. En revanche, leur refoulement ou leur
déformation sont pathologiques et permettent de déceler et de
localiser un processus pathologique.
Les principales lignes du médiastin sont [51] :
– les lignes médiastinales antérieure et postérieure : elles sont
constituées par le contact entre les deux poumons qui peut être
réalisé en deux endroits :
– en arrière, le contact s’établit entre le rachis et l’oesophage ; il
définit la ligne médiastinale postérieure ; sa projection dessine un
« V » : la pointe est située au-dessus d’un plan passant par le bord
supérieur de la veine azygos ; les branches, concaves en dehors,
se prolongent au-dessus du manubrium sternal, signant sa
topographie postérieure ; les feuillets de la plèvre s’écartent en
haut, en continuité avec les apex ; en bas, ils se prolongent à
gauche vers la crosse aortique et à droite vers le bouton azygos ;
cette ligne est visible dans environ 60 % des cas chez l’adulte, un
peu moins fréquemment chez l’enfant ;
– en avant, le contact entre les deux poumons s’effectue en région
rétrosternale ; sa projection définit la ligne médiastinale
antérieure, qui dessine également un « V » et dont les branches,
en haut, ne dépassent jamais le bord supérieur du manubrium
sternal ; la pointe du « V » se projette du deuxième au quatrième
cartilage costal, le plus souvent en situation paramédiane gauche.
Cette ligne est présente dans environ 25 % des cas chez l’adulte et
n’est pas visible chez le nourrisson, en raison de la présence du
thymus ;
– la ligne paratrachéale droite, visible dans 65 % des cas chez
l’adulte : construite par la réflexion de la plèvre médiastinale sur le
bord droit de la trachée, elle dessine une bande de tonalité hydrique,
délimitée par la clarté de la lumière trachéale et celle du poumon
droit ; elle est constituée par la paroi trachéale droite et par du tissu
adipeux médiastinal ; son épaisseur normale ne dépasse pas 4 mm ;
au-delà de 5 mm, elle est toujours pathologique ;
– la ligne paravertébrale droite visible dans 35 % des cas : elle est
formée par la réflexion de la plèvre sur les tissus mous
paravertébraux ; elle dessine une ligne distante d’environ 2 à 4mm
du bord du rachis et peut être refoulée par une grosse veine azygos ;
– la ligne paravertébrale gauche : elle correspond à la réflexion du
poumon gauche et de la plèvre sur les tissus mous paravertébraux ;
2 Médiastin de profil.
1. Médiastin antérieur ;
2. médiastin moyen ; 3. mé-diastin
postérieur ; 4. tra-chée
; 5. aorte ; 6. artère pul-monaire
; 7. veine cave
inférieure ; 8. tronc artériel
brachiocéphalique ; 9. ven-tricule
droit ; 10. ventricule
gauche.
elle est habituellement visible du bouton aortique à T10-T11 où elle
rejoint la ligne para-aortique ; elle reste solidaire de l’aorte et la suit
dans ses sinuosités ; cette ligne se situe toujours un peu en dehors
du milieu de la distance qui sépare le bord gauche de l’aorte
descendante des corps vertébraux ;
– la ligne para-aortique gauche, toujours visible : elle est déterminée
par la tangence entre le bord externe de l’aorte thoracique et le
poumon gauche ; elle est rectiligne, oblique en bas et en dedans ;
elle rejoint la ligne paravertébrale gauche à la hauteur de T10 ; chez
les sujets âgés, elle devient convexe en dehors avec le déroulement
de l’aorte thoracique ; le bord droit de l’aorte n’est habituellement
pas visible, mais une aorte déroulée peut faire hernie dans le cul-de-sac
interazygooesophagien, surtout si celui-ci est profond, et
détermine ainsi une ligne para-aortique droite ;
– la ligne para-azygo-oesophagienne, visible dans 88 % des cas : elle
représente la limite gauche du récessus interazygo-oesophagien, qui
correspond à du parenchyme du lobe inférieur droit venant
s’insinuer entre la grande veine azygos en arrière et l’oesophage en
avant ; elle décrit une ligne se projetant sur le rachis, en forme de
« S » allongé, dont le tiers supérieur est concave et les deux tiers
inférieurs convexes à droite ; en haut, elle est en continuité avec le
bouton azygos et se prolonge avec la ligne médiastinale postérieure ;
en bas, la ligne para-aortique droite peut lui faire suite, lorsque le
récessus interazygo-oesophagien vient mouler le bord droit de
l’aorte ;
– la ligne aorticopulmonaire : elle ferme la fenêtre aorticopulmonaire
sous forme d’une ligne oblique en bas et en dehors, et concave en
haut ; elle relie le bord externe du bouton aortique et le bord
supérieur de l’artère pulmonaire [35] ;
– la ligne aorticoveineuse : elle relie le bouton aortique au bord
supérieur de la veine pulmonaire supérieure gauche ; moins
fréquente que la précédente, elle a la même forme et se situe un peu
au-dessous d’elle [35].
Médiastin sur une radiographie de profil (fig 2)
Cette incidence permet d’individualiser :
– la silhouette cardiaque dont le bord antérieur est constitué par le
ventricule droit, le bord postérieur par l’oreillette gauche et le
ventricule gauche ; la présence de franges épicardiques peut se
traduire par une opacité triangulaire comblant l’angle
cardiophrénique, avec un sommet diaphragmatique antérieur ;
– l’aorte est habituellement visible au niveau de la partie inférieure
de la crosse ; lorsqu’elle est déroulée, elle peut être entièrement
visible, silhouettée par la clarté pulmonaire ;
2](https://image.slidesharecdn.com/syndromemdiastinal-141209093856-conversion-gate02/85/Syndrome-mediastinal-2-320.jpg)
![Radiodiagnostic Syndrome médiastinal 32-360-P-10
– la trachée est oblique en bas et en arrière ; sa paroi postérieure,
comprise entre l’air de la trachée et celui du poumon droit qui vient
s’insinuer en arrière d’elle, mesure 3 mm.
Division du médiastin [13]
Selon Felson, sur le cliché thoracique (fig 2), le médiastin est divisé
en :
– médiastin antérieur : c’est l’espace compris entre le sternum en
avant, le bord antérieur de la trachée et le bord postérieur du coeur
en arrière ;
– médiastin moyen : en arrière du précédent, il est limité en arrière
par une ligne virtuelle passant 1 cm en arrière du bord antérieur des
corps vertébraux ;
– médiastin postérieur : en arrière du médiastin moyen, il va jusqu’à
la paroi thoracique postérieure.
¦ Tomodensitométrie [19, 27]
Elle fournit une analyse topographique beaucoup plus précise selon
Heitzman [28], qui permet une classification des masses médiastinales
proposée par Hammon-Kerautret [27] inspirée par Heitzman. Elle
distingue neuf territoires et permet une approche topographique des
processus expansifs qui se développent dans le médiastin. Ceux-ci
proviennent soit des limites, soit du contenu de la région dans
laquelle ils se développent, mais ils peuvent aussi venir d’ailleurs et
s’étendre secondairement dans cette région.
Orifice cervicomédiastinal (fig 3)
Il est oblique en bas et en avant, limité par :
– en avant, le manubrium sternal et les articulations
sternoclaviculaires ;
– en arrière, le corps vertébral de T1 ;
– latéralement, les apex pulmonaires.
C’est un carrefour qui fait communiquer la base du cou, le
médiastin, les apex pulmonaires et les régions axillaires. Il contient,
au sein d’un tissu cellulograisseux :
– l’axe aérodigestif représenté par la trachée et l’oesophage, en avant
duquel se trouve le pôle inférieur des lobes thyroïdiens et parfois la
partie supérieure du thymus ;
– les axes vasculaires jugulocarotidiens ;
– les structures nerveuses (nerfs phréniques, récurrents,
pneumogastriques, chaînes sympathiques) ;
– le canal thoracique.
Espace rétrosternal préaorticocave (fig 4)
Ses limites sont représentées par :
– en avant, la paroi sternocostale ;
– latéralement, la plèvre médiastinale ;
– en arrière, les troncs veineux brachiocéphaliques, la veine cave
supérieure, l’auricule droite, l’oreillette droite, le ventricule droit, le
bord antérieur de l’aorte et le péricarde qui entoure l’origine de
l’aorte et le tronc de l’artère pulmonaire ;
– en haut, l’orifice cervicomédiastinal ;
– en bas, les angles cardiophréniques antérieurs.
Cet espace correspond à l’ancien médiastin antérieur et supérieur. Il
contient le thymus, les pédicules vasculaires mammaires internes,
les nerfs phréniques, le pédicule vasculaire médiastino-péricardo-diaphragmatique,
les chaînes ganglionnaires médiastinales
antérieures droite, gauche et transverse.
Angles cardiophréniques antérieurs (fig 5)
Ils sont délimités par :
– en avant, la paroi sternochondrocostale ;
– en arrière et en dedans, le péricarde recouvrant l’oreillette droite
et la pointe du coeur ;
– en bas, la portion antérieure horizontale du diaphragme.
Ils contiennent :
– les pédicules vasculaires et lymphatiques mammaires internes ;
– les ganglions lymphatiques des groupes diaphragmatiques
antérieurs (prépéricardiques) et moyen (latéropéricardiques) ;
– les nerfs phréniques droit et gauche.
Angle cardiophrénique postérieur (fig 6)
Il est limité par :
– en avant, le bord postérieur du coeur et de la veine cave
inférieure ;
– en arrière, la veine grande azygos, l’aorte, le canal thoracique ;
– latéralement, la plèvre médiastinale et les ligaments triangulaires ;
– en haut, il est en relation avec l’oreillette gauche et les veines
pulmonaires inférieures, et se poursuit avec la région sous- et
rétrocarinaire ;
3 Orifice cervicomédias-tinal.
1. Corps de T1 ;
2. apex pulmonaire ; 3. tra-chée
; 4. oesophage ; 5. thy-roïde
; 6. carotide primi-tive
; 7. artère sous-clavière
; 8. veine jugulaire
interne ; 9. chaîne sympa-thique
; 10. nerf récurrent ;
11. nerf pneumogastrique ;
12. canal thoracique.
4 Espace rétrosternal
préaorticocave. 1. Sternum ;
2. veine cave supérieure ;
3. aorte ; 4. trachée ; 5. thy-mus
; 6. nerf phrénique ;
7. pédicule mammaire in-terne
; 8. chaîne ganglion-naire
médiastinale anté-rieure
droite ; 9. chaîne
ganglionnaire médiastinale
antérieure gauche ; 10. nerf
pneumogastrique ; 11. nerf
récurrent gauche.
5 Angle cardiophrénique
antérieur droit. 1. Appen-dice
xiphoïde ; 2. oreillette
droite ; 3. ventricule droit ;
4. artère mammaire inter-ne
; 5. veine cave inférieu-re
; 6. nerf phrénique droit ;
7. ganglion du groupe
diaphragmatique latéropé-ricardique
; 8. ganglion du
groupe diaphragmatique
antérieur ; 9. muscle trian-gulaire
du sternum.
3](https://image.slidesharecdn.com/syndromemdiastinal-141209093856-conversion-gate02/85/Syndrome-mediastinal-3-320.jpg)

![Radiodiagnostic Syndrome médiastinal 32-360-P-10
Si les descriptions princeps reposent sur la radiologie
conventionnelle, il est aujourd’hui nécessaire d’inclure la sémiologie
scanographique, IRM et échographique.
RADIOLOGIE CONVENTIONNELLE
¦ Opacités
Elles représentent l’essentiel de la pathologie médiastinale.
Indépendamment de leurs étiologies, elles ont des caractères
sémiologiques communs sur la radiographie thoracique de face qui
présente l’avantage de ne pas superposer le médiastin et le poumon.
Caractères généraux des opacités médiastinales [8]
Ce sont des opacités :
– de densité hydrique, le plus souvent homogène ;
– à limite externe nette et continue, convexe vers le poumon, se
raccordant en pente douce avec les bords du médiastin ;
– à limite interne invisible noyée dans le médiastin où se situe
approximativement leur centre.
Leur topographie médiastinale se traduit :
– soit par un déplacement ou une anomalie du contour externe du
médiastin ;
– soit par un déplacement d’une ligne médiastinale ;
– soit par l’apparition d’une ligne médiastinale anormale.
Localisation de l’opacité
Il importe de situer la lésion dans un des compartiments antérieur,
moyen, postérieur – classification de Felson –, dans la mesure où les
orientations diagnostiques sont étroitement liées à cette topographie.
Cette localisation repose sur :
10 Tératome médiastinal bénin avec adhérence péricardique
à l’intervention.
A. Thorax de face : opacité à limite externe nette effaçant
le bord droit du coeur (signe « de la silhouette »).
B. Tomodensitométrie (TDM) : masse de faible densité
(5 unités Hounsfield [UH]) refoulant l’oreillette droite
dont la paroi est mal analysée en raison des battements
cardiaques.
C. Imagerie par résonance magnétique (IRM) : coupe
frontale pondérée en T1 montrant un signal hyperin-tense
et une formation nodulaire murale (flèches).
D. IRM : coupe axiale pondérée T1 montrant l’interrup-tion
du péricarde antérieur (flèches) au contact de la
tumeur.
– la radiographie de profil : elle aide à situer l’opacité d’avant en
arrière lorsqu’elle présente une interface médiastinopulmonaire
tangente au rayon [59, 65] ;
– l’identification d’un certain nombre de signes propres au
médiastin décrits dans le paragraphe suivant.
Principaux signes [5, 8, 9, 12, 13, 14, 17, 27, 28, 29, 31, 32, 49, 50, 51]
· Signe de la silhouette [14]
Il précise le siège de la lésion, qui se situe dans le même plan que la
structure dont la silhouette a disparu (coeur, aorte, diaphragme)
(fig 10).
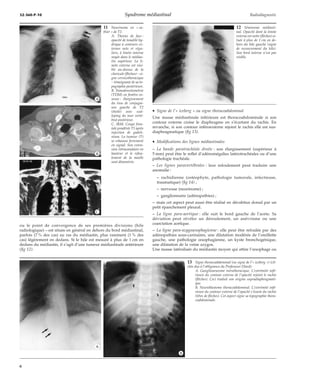
· Signe cervicothoracique
Il localise, sur une radiographie de face, une opacité du défilé
cervicothoracique. Lorsque son bord externe est visible au-dessus
de la clavicule, cette masse est de topographie postérieure : elle est
silhouettée par l’air de l’apex pulmonaire qui est de siège postérieur
(fig 11). À l’inverse, si elle est de topographie antérieure, noyée dans
la graisse du creux sus-claviculaire qui est de siège antérieur, son
bord externe n’est pas visible au-dessus de la clavicule.
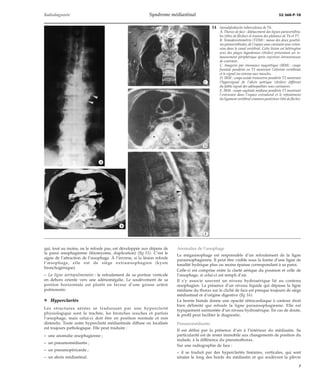
· Signe de la convergence du hile
Il permet de différencier une masse médiastinale d’une grosse artère
pulmonaire. Devant une opacité hilaire lorsque les branches
artérielles pulmonaires convergent vers elle et perdent leur
silhouette sur son bord externe, il s’agit d’une artère pulmonaire. À
l’inverse, si les vaisseaux restent visibles à travers l’opacité, il s’agit
d’une masse médiastinale, habituellement des adénopathies.
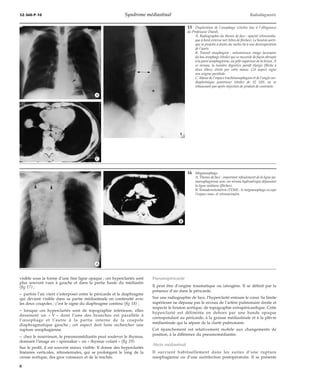
· Signe du recouvrement du hile
Il permet de différencier une masse médiastinale antérieure d’une
cardiomégalie ou d’une péricardite. L’artère pulmonaire gauche –
*A
*B
*C *D
5](https://image.slidesharecdn.com/syndromemdiastinal-141209093856-conversion-gate02/85/Syndrome-mediastinal-5-320.jpg)
![Radiodiagnostic Syndrome médiastinal 32-360-P-10
sous la forme d’une opacité médiastinale, en général de topographie
postérieure et supérieure, parfois caractérisée par la présence d’un
niveau hydroaérique.
¦ Calcifications
Les calcifications médiastinales intéressent les structures
ganglionnaires, cardiovasculaires ou tumorales.
Adénopathies
Les calcifications granuleuses, irrégulières ou groupées en amas,
sont évocatrices de séquelles de tuberculose ou d’histoplasmose.
Une infection à Pneumocystis carinii compliquant un syndrome de
l’immunodéficience acquise (sida) peut aussi engendrer des
calcifications ganglionnaires.
Les calcifications sont parfois fines, arciformes, en « coquille d’oeuf »,
évoquant surtout une silicose et, plus rarement, une sarcoïdose, une
mycose ou un lymphome traité [26].
Calcifications vasculaires
Elles sont parallèles ou semi-circulaires ; elles se superposent au
trajet vasculaire. Elles intéressent surtout l’aorte, mais aussi ses
branches de division dans le cadre de lésions athéromateuses et, plus
rarement, les artères pulmonaires dans l’hypertension artérielle
pulmonaire ancienne.
Calcifications cardiaques
Les calcifications valvulaires sont fréquentes et caractéristiques.
Celles du péricarde dans la péricardite calcifiante dessinent une fine
ligne calcifiée, entourant une plus ou moins grande partie de la
silhouette cardiaque.
Les calcifications tumorales cardiaques sont très rares. Elles sont
irrégulières, groupées en amas avec une mobilité caractéristique sous
scopie.
Calcifications tumorales
Elles ont parfois une valeur d’orientation :
– dans les goitres thyroïdiens, les calcifications sont mobiles avec la
déglutition et se prolongent parfois vers le cou ; elles peuvent être
nodulaires, arciformes, disséminées, périphériques ou centrales ;
– la présence de dents ou d’éléments osseux permet d’affirmer un
tératome ;
– les thymomes contiennent quelquefois des calcifications
nodulaires ou en lamelles périphériques, situées dans le médiastin
antérieur (fig 20) ;
– la présence de calcifications au sein d’une opacité médiastinale
postérieure doit faire évoquer une tumeur neurogène ;
– les phlébolithes orientent vers une tumeur hémangiomateuse ;
– les kystes bronchogéniques peuvent présenter une calcification de
leur paroi.
ÉCHOGRAPHIE
L’échographie transthoracique est un examen de faible coût, d’accès
facile ; elle peut être utilisée pour préciser une image radiographique
anormale ou dans le suivi des masses médiastinales antérieures
[42, 63]. Elle est réalisée par voie antérieure, avec une sonde de 3,5 ou
de 5 MHz, par un abord sus-sternal, parasternal et sous-xiphoïdien
[6]. Elle est très sensible dans la détection des masses du
médiastin antérieur où elle supplante largement la radiographie de
face et de profil [64]. En revanche, la sensibilité reste mauvaise pour
le dépistage des masses du médiastin moyen et surtout postérieur.
Elle apparaît moins performante que la TDM mais demeure très
supérieure aux clichés simples dans l’exploration de la région
prévasculaire – en avant de la veine cave supérieure et de l’aorte
ascendante – et de la région paratrachéale droite.
La visualisation d’une lésion dépend de son échostructure, de la
taille et de la forme de la fenêtre acoustique. La distance qui la
sépare de la sonde intervient également, une masse profonde étant
moins bien décelée qu’une masse superficielle.
Les informations fournies concernent la taille, la morphologie, la
topographie et l’échostructure de la lésion. Les tumeurs solides
apparaissent hypoéchogènes, les kystes anéchogènes. Lorsque
ceux-ci sont au contact du poumon, la totalité du faisceau
ultrasonore peut être réfléchi et le renforcement postérieur peut faire
défaut.
17 Pneumomédiastin.
Présence d’une hyperclarté
linéaire verticale qui sou-lève
la plèvre (tête de flèche),
visible sous la forme d’une
fine ligne opaque.
18 Pneumomédiastin. Si-gne
du « diaphragme con-tinu
» : visibilité anormale
de la partie médiane et anté-rieure
du diaphragme (têtes
de flèches) (cliché dû à
l’obligeance du Professeur
Diard).
19 Pneumomédiastin
chez un enfant de 9 ans. Si-gne
du « thymus volant » :
aspect caractéristique du
soulèvement du lobe gauche
du thymus (têtes de flèches).
Emphysème sous-cutané en
région cervicale et axillaire
(étoiles) (cliché dû à l’obli-geance
du Professeur
Diard).
9](https://image.slidesharecdn.com/syndromemdiastinal-141209093856-conversion-gate02/85/Syndrome-mediastinal-9-320.jpg)
![32-360-P-10 Syndrome médiastinal Radiodiagnostic
*A *B
Mais il importe aussi de rechercher les signes indirects tel que l’effet
de masse engendré, parfois seul élément détectable. Une masse sous-carinaire
est suspectée sur une empreinte extrinsèque au niveau de
l’artère pulmonaire droite.
L’échographie peut aussi être réalisée par voie endooesophagienne,
couplée à une fibroscopie. Cette voie d’abord permet d’accéder aux
ganglions périoesophagiens (chaîne 8 de la classification de
l’American Thoracic Society), sous-carinaires (chaîne 7) et
paratrachéaux-supérieurs gauches (chaîne 2 G). Les adénopathies se
traduisent par des structures nodulaires arrondies ou ovalaires
hypoéchogènes. Cet examen permet aussi une bonne analyse de
l’oreillette gauche et de la partie terminale des veines pulmonaires
gauches.
TOMODENSITOMÉTRIE
La TDM représente actuellement la meilleure technique
d’exploration des masses médiastinales [2, 3]. Elle apporte des
éléments supplémentaires par rapport aux clichés simples dans 44 à
78 % des cas et par rapport aux tomographies dans 23 % des cas [57].
Elle bénéficie d’une excellente sensibilité, permettant de détecter de
petites masses tumorales invisibles sur les clichés simples telles
qu’un thymome, certaines adénomégalies ou un adénome
parathyroïdien [41]. Outre l’évaluation des dimensions, elle assure un
diagnostic topographique précis en montrant le siège de la lésion,
son extension et les rapports avec les organes de voisinage.
¦ Localisation médiastinale d’une masse
La distinction entre l’origine médiastinale, pleurale ou pulmonaire
d’une masse peut être un problème diagnostique difficile. Les
critères utilisés sur le cliché standard par Heitzman [28] et Felson [12],
cités précédemment, ne résolvent pas tous les problèmes. En
particulier, il est habituellement impossible de distinguer une masse
médiastinale d’une pleurésie enkystée du médiastin [28].
La TDM est beaucoup plus performante que la radiographie
standard pour résoudre ce problème [66]. Le critère le plus fiable
repose sur l’analyse de l’interface entre la masse et le poumon.
Lorsqu’elle est lisse et régulière, la masse est médiastinale.
Lorsqu’elle est spiculaire ou nodulaire, son origine est plus
volontiers pulmonaire. En effet, lorsqu’une tumeur croît dans le
médiastin, elle refoule les structures médiastinales normales en
dehors (graisse, gros vaisseaux, plèvre pariétale et viscérale).
Celles-ci recouvrent la lésion et sont responsables d’une interface
lisse entre la masse et le poumon. Cependant, les lymphomes, les
thymomes invasifs, les tumeurs germinales ou les goitres
20 Thymome lymphoépithélial encapsulé.
*C
A. Thorax de face : opacité à limite externe nette (tê-tes
de flèches) n’effaçant ni le bouton aortique, ni
l’artère pulmonaire gauche.
B. Thorax de profil montrant sa topographie anté-rieure,
son caractère lobulé et la présence de fines
calcifications lamellaires (tête de flèche).
C. Tomodensitométrie (TDM) : masse de densité
solide (53 UH), polylobée de l’espace rétrosternal
prévasculaire, présentant de fines calcifications (flè-che).
intrathoraciques dégénérés peuvent avoir une extension
transpleurale et donner, avec le parenchyme pulmonaire envahi, une
interface irrégulière (fig 21).
21 Carcinome thymique. Coupe TDM
axiale : masse de l’espace rétrosternal
préaorticocave à contours polycycliques
et irréguliers (têtes de flèches) en rapport
avec une infiltration parenchymateuse
pulmonaire. Infiltration ganglionnaire
(étoile blanche). Réaction pleurale associée
(astérisque).
La topographie par rapport aux vaisseaux est également importante
à considérer : les lésions médiastinales sont plus volontiers médiales
et les lésions pulmonaires ou pleurales, plus volontiers latérales.
En revanche, l’analyse des angles de raccordement antérieur et
postérieur entre le médiastin et la masse, et l’importance du
déplacement des structures anatomiques du médiastin sont d’une
faible utilité.
La distinction entre masse médiastinale et pleurésie médiastinale
enkystée est le plus souvent possible en scanographie. La pleurésie
médiastinale est latérale par rapport aux vaisseaux et à la graisse
médiastinale ; elle ne déplace pas les structures médiastinales et est
souvent associée à d’autres signes pleuraux.
¦ Analyse topographique et densitométrique
– La localisation et la composition tissulaire de la lésion sont les
bases sémiologiques du diagnostic étiologique [38, 56, 59]. Les
principales étiologies sont rapportées dans le tableau I.
– L’analyse topographique consiste à localiser la masse dans l’un
des compartiments précédemment décrits. L’approche multiplanaire
autorisée par les reconstructions des acquisitions spiralées facilite
l’étude des rapports anatomiques.
10](https://image.slidesharecdn.com/syndromemdiastinal-141209093856-conversion-gate02/85/Syndrome-mediastinal-10-320.jpg)
![Radiodiagnostic Syndrome médiastinal 32-360-P-10
– L’analyse TDM permet une approche de la composition tissulaire
de la lésion. La mesure doit être effectuée sur une plage la plus large
possible tout en évitant les bandes d’artefacts qui modifient
artificiellement la densité. Ainsi la sensibilité de la TDM dans la
détection des structures graisseuses (- 50 à - 150 unités Hounsfield
[UH]) et des calcifications (400 UH) est de 100 %.
– Les structures graisseuses.
Un excès de graisse sans aucun effet de masse sur les structures
vasculaires ni aériques évoque une lipomatose qui peut être diffuse
et qui est constituée par une graisse histologiquement normale. Il se
rencontre chez les sujets obèses, sous corticothérapie ou dans le
cadre de la maladie de Cushing.
Une masse graisseuse dans les angles cardiophréniques peut
correspondre à une hernie diaphragmatique rétrocostoxyphoïdienne.
Le diagnostic est affirmé par la présence de petites structures
linéaires correspondant à des vaisseaux épiploïques et par la mise
en évidence de la continuité avec la graisse intra-abdominale (fig 22).
Une masse tumorale, exclusivement de densité graisseuse, peut
correspondre à un lipome ou à un liposarcome dans sa forme très
bien différenciée [15]. Les liposarcomes typiques comportent, outre la
Tableau I.
Densité tissulaire Densité liquidienne Densité graisseuse Masse
hypervascularisée Tissu composite
Orifice cervicomédiastinal
Goitre thyroïdien Lymphangiome kystique Goitre
Adénome parathyroïdien Kyste du canal thoracique Adénome parathyroïdien
Cancer oesophagien Kyste thymique
Papillomes trachéaux Tumeur thymique kystisée
Tumeurs neurogènes
(pneumogastriques, récur-rentes,
phréniques,
chaînes sympathiques)
Tératome kystique
Certaines tumeurs
neurogènes
Abcès
Lymphome
Tératome
Hématomes
Espace rétrosternal
préaorticocave
Thymome Kyste thymique Lipomatose Carcinome thymique Dysembryome
Lymphome Tumeur kystisée : Lipome Thymome
Dysembryome thymome, lymphome, dysem-bryome,
adénopathies nécrosées,
tumeur neurogène, tumeur testi-culaire
Tératome Lymphome
Goitre plongeant Pseudokyste (hématique) Thymolipome
Liposarcome
Hibernome
Angle cardiophrénique
antérieur
Tumeur thymique Kyste pleuropéricardique Amas graisseux
Tératome Lymphangiome kystique Lipome
Adénopathies Tératome
Tumeur du nerf phrénique Thymolipome
Liposarcome
Hernie diaphragmatique
rétrocostoxiphoïdienne
Angle cardiophrénique
postérieur
Tumeur oesophagienne Dérivé kystique de l’intestin
primitif
Anévrisme aortique
Tumeur neurogène (pneu-mogastrique)
Kyste du canal thoracique Dilatation des sinus
coronaires
Adénopathies Kyste pleuropéricardique
Épanchement péricardique
enkysté
Épanchement pleural enkysté
Espace
paratrachéooesophagien
Tumeur oesophagienne
bénigne ou maligne
Dérivés kystiques de l’intestin
primitif
Lipomatose Paragangliome
Tumeur trachéale Mégaoesophage Lipome
Adénopathies Hématome
Tumeur nerveuse (pneu-mogastriques,
récurrents)
Abcès intramural
oesophagien
Gouttière costovertébrale
Tumeur neurogène Méningocèle Lipomatose circonscrite
paraspinale
Pseudotumeur vasculaire
Hématopoïèse extramé-dullaire
Dérivés kystiques de l’intestin
primitif
Lipome Myélolipome
Spondylodiscite Hématopoïèse extramé-dullaire
Hématome
Kyste canal thoracique
Espace inframédiastinal
postérieur
Adénopathies Kyste du canal thoracique Lipomatose Anévrisme aortique
Thymome invasif Dérivés kystiques de l’intestin
primitif
Varice du système azygos
Mésothéliome Pseudokyste pancréatique
Certaines tumeurs
neurogènes
Tumeur rétropéritonéale
Espace sous- et
rétrocarinaire
Adénopathies Dérivé kystique de l’intestin pri-mitif
(kyste bronchogénique)
Lipomatose
Tumeur oesophagienne Kyste du canal thoracique
Cancer bronchique
Masse à point de départ
cardiopéricardique
11](https://image.slidesharecdn.com/syndromemdiastinal-141209093856-conversion-gate02/85/Syndrome-mediastinal-11-320.jpg)
![32-360-P-10 Syndrome médiastinal Radiodiagnostic
*A *C *D
22 Hernie par la fente de Larrey.
A. Radiographie du thorax de face : présence d’une opacité à bord externe convexe au niveau de l’angle cardiophré-nique
composante graisseuse qui est prédominante, une composante de
densité tissulaire (fig 23).
Les thymolipomes [52] peuvent également présenter une texture
mixte, en partie graisseuse et en partie tissulaire. Ils sont souvent
volumineux et siègent dans les angles cardiophréniques antérieurs.
L’existence d’une connexion avec l’espace rétrosternal préaorticocave
conforte ce diagnostic.
Une masse contenant un mélange de tissu solide, liquidien et
graisseux, est très en faveur du tératome [39]. La composante
graisseuse est habituellement de faible quantité (fig 24).
– La sensibilité de détection en TDM des tumeurs solides est de
98 %. Elle est seulement de 71 % pour celle des tumeurs
kystiques [18] :
– une tumeur solide peut, en effet, présenter une densité
liquidienne (-20 à +20 UH) par la survenue d’une nécrose, d’un
oedème ou d’une involution adipeuse comme dans certaines
tumeurs neurogènes [1, 33, 34, 38, 47, 48, 54, 56] ;
– à l’inverse, une lésion kystique peut afficher une densité élevée
en raison d’un liquide riche en protéines ou en sels calciques, ce
qui est le cas des kystes bronchogéniques (fig 25) [43, 45, 67] ; la
présence d’un saignement ou d’une surinfection peuvent
également augmenter la densité [7]. D’autres critères sont alors
utiles pour faire le diagnostic scanographique de lésion kystique :
l’absence de rehaussement, après injection intraveineuse de
produit de contraste, et la variation de forme selon la position du
patient. Ainsi, dans les kystes pleuropéricardiques, des variations
positionnelles de forme sont possibles en raison de leur plasticité
(fig 26). Le point d’attache de la masse liquidienne avec le
médiastin est à angle aigu [11] ;
– l’analyse de la paroi d’une lésion de densité liquidienne est
essentielle. Une paroi fine sans cloison de refend évoque un kyste
primitif. À l’inverse, épaisse et irrégulière, elle évoque une tumeur
solide nécrosée. La présence de cloisons de refend se voit dans
certaines lésions telles que les kystes thymiques acquis et les
lymphangiomes kystiques [34].
– La mise en évidence d’un niveau entre deux phases de densité
liquidienne peut correspondre à :
– un abcès ;
– la phase précoce d’un hématome par surdosage en
anticoagulants ;
– un kyste hydatique.
– En revanche, la présence d’un niveau entre une phase graisseuse
et une phase liquidienne est très évocatrice d’un tératome [20].
droit (étoile).
B. Tomodensitométrie (TDM) : il s’agit d’une masse de densité graisseuse qui contient des structures linéaires cor-respondant
à des vaisseaux épiploïques (flèche courte).
C, D. Coupes par imagerie par résonance magnétique (IRM) frontale (C) et sagittale (D) pondérées T1 : cette masse
graisseuse apparaît hyperintense (étoile), elle est en continuité avec la graisse sous-diaphragmatique. Les vaisseaux
épiploïques qui traversent l’orifice herniaire sont visibles sous forme de fins liserés hypo-intenses (flèche). Le defect
diaphragmatique est bien visible (flèche longue).
*B
23 Liposarcome. Coupe tomodensitomé-trique
(TDM) axiale : masse cloisonnée
de l’espace rétrosternal préaorticocave
constituée de graisse (astérisque). Il existe,
au sein de cette masse, une plage de densité
tissulaire (tête de flèche).
24 Tératome. Coupe to-modensitométrique
(TDM) :
masse antérieure hétérogène,
comportant des plages de
densité liquidienne (étoile),
une plage graisseuse (flèche
courbe) et des plages de den-sité
tissulaire (flèche droite).
12](https://image.slidesharecdn.com/syndromemdiastinal-141209093856-conversion-gate02/85/Syndrome-mediastinal-12-320.jpg)
![Radiodiagnostic Syndrome médiastinal 32-360-P-10
*A *B
– Certaines masses peuvent présenter des densités spontanées
élevées, en particulier des goitres thyroïdiens et les hématomes
récents.
Les hématomes en phase aiguë (au cours des premières heures) sont
spontanément hyperdenses. Cette densité décroît dans le temps de
façon centripète, créant un halo périphérique hypodense.
– La vascularisation d’une lésion est appréciée par l’étude
dynamique après injection intraveineuse de produit de contraste.
L’absence de rehaussement est habituelle pour les lésions kystiques
ou nécrotiques. À l’inverse, les structures hypervascularisées
prennent le contraste de façon intense (fig 27). C’est le cas des goitres
thyroïdiens, des carcinomes médullaires de la thyroïde, des tumeurs
parathyroïdiennes, des tumeurs vasculaires (hémangiomes,
hémangioépithéliomes, hémangiopéricytomes), de la maladie de
Castelman, des carcinoïdes thymiques, des métastases de sarcomes
et de mélanomes. Certains types de rehaussement sont très
évocateurs. Ainsi un rehaussement périphérique intense au temps
veineux, associé à des flaques de contraste, oriente vers une masse
angiomateuse [55].
– Les épanchements gazeux se traduisent par des hyperclartés
facilement reconnaissables (fig 28).
IMAGERIE PAR RÉSONANCE MAGNÉTIQUE
Comme en TDM, le signal caractéristique de la graisse est utilisé en
IRM pour repérer les structures normales et anormales du médiastin.
L’IRM permet la visibilité spontanée des structures vasculaires. Elle
offre en outre d’autres avantages dans l’étude du médiastin :
– une plus grande résolution en contraste qui permet
d’individualiser et de délimiter une lésion sans injection de produit
de contraste ;
– la possibilité d’une étude multiplanaire qui peut s’avérer
particulièrement utile [62] pour explorer la fenêtre aortopulmonaire,
la loge sous-carinaire, le hile, les récessus péricardiques [22, 30] et les
structures vasculaires.
Cette possibilité facilite aussi l’analyse de processus pathologiques
situés à cheval sur l’orifice cervicomédiatinal (goitre, tumeur
thymique, lymphome, tumeur neurogène) ainsi que les masses
médiastinales à extension sous-diaphragmatique (thymome invasif,
lymphome, dysembryome) auxquelles on peut associer le
mésothéliome malin dont le diagnostic différentiel est parfois
difficile. L’IRM analyse bien l’extension intracanalaire des tumeurs
de la gouttière costovertébrale et, plus particulièrement, des tumeurs
neurogènes. Cet avantage, souligné par de nombreux auteurs [18, 62],
place cet examen au premier plan dans cette indication. L’IRM
montre parfaitement l’extension en hauteur, les rapports de la
tumeur avec la moelle, les méninges (fig 29) et les racines.
Toutefois, les coupes axiales restent globalement les plus
informatives et constituent l’examen de base. Elles dégagent
parfaitement la région prévasculaire, prétrachéale, para-aortique
gauche. Elles individualisent bien les effets de masse avec les
déplacements dans le plan axial [4].
L’analyse sémiologique repose, comme en TDM, sur l’étude de la
topographie et de la composition tissulaire des lésions. L’IRM
[23, 24, 36, 40, 61] permet de reconnaître les formations solides, kystiques
ou graisseuses ; mais les calcifications sont moins bien identifiées
25 Kyste bronchogénique.
A. Coupe tomodensitométrique (TDM) sans injection de produit de contraste :
masse spontanément hyperdense de la loge sous-carinaire (astérisque). Il existe
des calcifications (tête de flèche) visibles au sein de cette structure.
B. Coupe TDM après injection de produit de contraste : cette masse demeure hy-perdense
(astérisque) mais ne présente pas de rehaussement après injection
de produit de contraste, ce qui atteste sa nature kystique.
26 Kyste pleuropéricardique. Tomodensitométrie (TDM) : masse de l’angle
cardiophrénique droit (étoile), homogène de densité hydrique (5 UH) sans pa-roi
identifiable (A) se déformant en décubitus latéral (B) et dont l’attache an-térieure
présente un angle aigu (tête de flèche).
*A
*B
27 Maladie de Castle-man
: multiples formations
nodulaires (tête de flèche)
de 10 à 15 mm de diamètre
évoquant des adénopathies ;
fort rehaussement en den-sité
analogue à celui des
vaisseaux.
28 Pneumomédiastin (at-teinte
pulmonaire d’une
sclérodermie). Clartés aéri-ques
décollant la plèvre mé-diastinale
et disséquant la
graisse médiastinale.
13](https://image.slidesharecdn.com/syndromemdiastinal-141209093856-conversion-gate02/85/Syndrome-mediastinal-13-320.jpg)
![Radiodiagnostic Syndrome médiastinal 32-360-P-10
Les lésions kystisées par des remaniements nécrotiques ou
hémorragiques conservent, en revanche, des parois épaisses. Elles
peuvent survenir sur les goitres, thymomes, les tératomes kystiques,
les tumeurs neurogènes, les séminomes et les adénomégalies.
¦ Lésions hémorragiques [16, 53, 58]
Les hématomes, dans leur phase initiale (au cours des premières
heures), présentent un signal intermédiaire ou hyperintense en T1 et
hyperintense en T2.
Du premier au troisième jour, l’hématome devient hypo-intense en
pondération T1 et T2, en rapport avec la transformation de
l’hémoglobine en désoxyhémoglobine (fig 34).
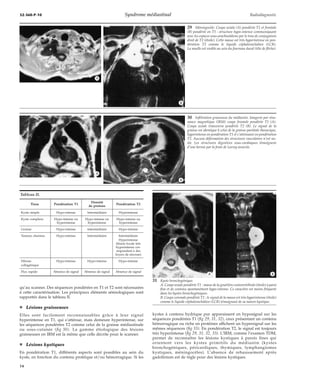
32 Lymphangiome kystique.
A. Coupe sagittale pondérée T1 : volumineuse structure
kystique à parois fines (astérisque), cloisonnée (tête
de flèche), silhouettée par la graisse médiastinale.
B. Coupe axiale pondérée T2 : cette masse est hyperin-tense
comme le liquide céphalorachidien (LCR), témoi-gnant
de sa nature kystique (astérisque).
À la phase subaiguë, à partir du quatrième jour, la transformation
de la désoxyhémoglobine en méthémoglobine entraîne un signal
hyperintense en pondération T1 et T2 qui apparaît à la périphérie
de la lésion.
La phase chronique est marquée par la transformation de la
méthémoglobine en hémosidérine qui s’accumule à la périphérie de
la lésion et se caractérise par une couronne en hyposignal en
pondération T2 (fig 35).
Les saignements répétés sont responsable d’un aspect le plus
souvent hétérogène.
¦ Tumeurs charnues
Elles ont un signal intermédiaire, voisin de celui du muscle sur les
séquences pondérées en T1, et un signal supérieur au muscle et
*A
*B
33 Kyste bronchogénique.
A. Coupe coronale pondérée T1 : masse arrondie de la
loge sous-carinaire (astérisque) spontanément hyperin-tense
en rapport avec un contenu riche en protéines.
B. Cette masse apparaît très hyperintense sur la séquence
pondérée T2 (astérisque) témoignant de sa nature kysti-que.
*A *B
34 Hématome postangioplastie à j2.
A. Coupe tomodensitométrique (TDM) : volumineuse masse spontanément hyperdense attenante au péricarde (as-térisque)
correspondant à l’hématome.
B. Imagerie par résonance magnétique (IRM) en coupe axiale : le signal est hypo-intense (étoile) en T1 (B)
et hétérogène mais plutôt hypo-intense en T2 (C) (astérisque).
*A
*B
*C
15](https://image.slidesharecdn.com/syndromemdiastinal-141209093856-conversion-gate02/85/Syndrome-mediastinal-15-320.jpg)
![32-360-P-10 Syndrome médiastinal Radiodiagnostic
parfois proche de celui de la graisse sur les séquences pondérées en
T2. Comme en TDM, elles présentent un rehaussement après
injection de produit de contraste.
¦ Lésions fibreuses
L’intensité du signal de la fibrose en IRM dépend de l’importance
relative du collagène et du contingent cellulaire. Le tissu fibreux
mature à prédominance collagénique et faible cellularité présente
un hyposignal en T1 et T2 (fig 36). Ceci explique le signal hypo-intense
en T1 et T2 des masses résiduelles des lymphomes traités
par radiothérapie [25] et des médiastinites fibreuses. En revanche, la
fibrose débutante, pauvre en collagène, riche en fibroblastes et en
vaisseaux, présente un signal hyperintense en T2 dû à sa charge
hydrique. Dans les lymphomes hodgkiniens à forme scléronodulaire,
l’intensité de signal en T2 est controversée [25, 37, 46].
35 Hématome rétrooesophagien iatrogène, secondaire à la
pose d’une voie veineuse centrale sous-clavière. Exploration
à 3 semaines.
A. Coupe frontale pondérée T1 : l’hématome est iso-intense
(astérisque), cerné par une couronne hyperin-tense
(têtes de flèches).
B. Coupe axiale pondérée T2 : la collection est hyperin-tense,
surtout en périphérie (tête de flèche noire),
et cernée d’une couronne hypo-intense (tête de flèche
blanche).
¦ Calcifications
Leur détection est moins aisée qu’en TDM. Si elles sont
suffisamment volumineuses, elles sont visibles sous forme d’une
zone d’hyposignal en T1 et T2.
¦ Divers
Certains caractères sémiologiques peuvent orienter vers des types
histologiques particuliers, comme l’a rapporté Fumikazu dans
quelques tumeurs neurogènes [21] du médiastin postérieur.
Les neurofibromes présentent un signal intermédiaire en
pondération T1. En pondération T2, la zone périphérique est très
hyperintense, plus hyperintense que la graisse, en rapport avec une
texture gélatineuse liée à la dégénérescence myxoïde. La zone
centrale, qui correspond à du tissu solide, conserve un signal
*A
*B
36 Fibrose médiastinale par extension d’une fibrose rétropé-ritonéale.
A. Coupe axiale pondérée T1 : présence d’un engaine-ment
de la crosse de l’aorte très hypo-intense (astéris-ques).
B. Coupe axiale pondérée T2 : cet engainement présente
un signal très hypo-intense en T2 en rapport avec
sa nature fibreuse (astérisques).
*A *B
37 Neurofibrome étendu au canal vertébral.
A. Coupe frontale pondérée T1 : masse de signal intermé-diaire
de la gouttière costovertébrale (étoile) avec exten-sion
intracanalaire (tête de flèche).
B. Coupe axiale pondérée T2 : la masse présente une pé-riphérie
hyperintense, plus intense que la graisse (gran-des
têtes de flèches) correspondant à une dégénérescence
myxoïde très évocatrice du neurofibrome. La partie cen-trale
conserve un signal intermédiaire et demeure sépa-rée
de la partie périphérique par un liseré hypo-intense
qui correspond à des fibres de collagène(petite tête
de flèche).
*A
*B
16](https://image.slidesharecdn.com/syndromemdiastinal-141209093856-conversion-gate02/85/Syndrome-mediastinal-16-320.jpg)
![32-360-P-10 Syndrome médiastinal Radiodiagnostic
Références
[1] Baron RL, Lee JK, Sagel SS, Baglan RJ. Thymic cysts follo-wing
radiation therapy for Hodgkin disease. Radiology
1981 ; 141 : 593-597
[2] Batra P, Brown K, Collins JD et al. Mediastinal masses: ma-gnetic
resonance imaging in comparison with computed
tomography. J Nation Med Assoc 1991 ; 83 : 969-974
[3] Batra P,BrownK, Steckel R. Diagnosticimagingtechniques
in mediastinal malignancies. Am J Surg 1988 ; 156 : 4-10
[4] Batra P,BrownK, Steckel RJ, Collins JD,OvenforsCO,Aberle
D. MR imaging of the thorax: a comparison of axial,
coronal, and sagittal imaging planes. J Comput Assist
Tomogr 1988 ; 12 : 75-81
[5] Blank N, Castellino RA. Patterns of pleural reflections of the
left superior mediastinum. Normal anatomy and distor-tions
produced by adenopathy. Radiology 1972 ; 102 :
585-589
[6] Bruggemann A, Greie A, Lepsien G. Real-time sonography
of the mediastinum in adults; a study in 100 healthy volun-teers.
Surg Endosc 1991 ; 5 : 150-153
[7] Brunner DR, Withley NO. A pericardial cyst with high CT
numbers. AJR Am J Roentgenol 1984 ; 142 : 279-280
[8] Capdeville R, Convard JP, Remy J. Le syndrome médiasti-nal.
Encycl Méd Chir (Éditions Scientifiques et Médicales
Elsevie SAS, Paris), Radiodiagnostic – Coeur-poumon,
32-360-P-10, 1980
[9] Caron J, Caron-Poitreau C. Intérêt diagnostique de l’étude
des lignes du médiastin sur l’incidence thoracique de face.
J Radiol Electrol 1976 ; 57 : 911-915
[10] Coussement A. Le poumon normal. Encycl Méd Chir (Édi-tions
Scientifiques et Médicales Elsevie SAS, Paris), Radio-diagnostic
– Coeur-poumon, 32-330-A-10, 1998 : 1-20
[11] Demos TC, Budorick NE, Posniak HV. Benign mediastinal
cysts: pointed appearance on CT. J Comput Assist Tomogr
1989 ; 13 : 132-133
[12] Felson B. The mediastinum. Semin Roentgenol 1969 ; 4 :
41-58
[13] Felson B. Chest roentgenology. Philadelphia : WB Saun-ders,
1973
[14] Felson B, Felson H. Localization of intrathoracic lesions by
means of postero-anterior roentgenograms: silhouette
sign. Radiology 1950 ; 55 : 363-373
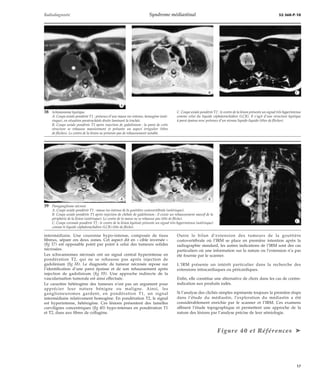
40 Ganglioneurome.
[15] Ferretti G, Pittet L, Pison C, Ranchoup Y, Le March’Hadour
F, Sarrazin R et al. Liposarcome primitif du médiastin :
apport de l’IRM au diagnostic. À propos d’un cas. Rev Mal
Respir 1992 ; 9 : 467-469
[16] Fornes P,Hoeffel C,Hoeffel JC, GalloyMA.Leshématomes:
confrontations anatomo-radiologiques. Radiol J Cepur
1995 ; 15 : 11-32
[17] Fraser RG, Pare JA, Pare PD, Fraser RS. Diseases of the medi-astinum.
In : Diagnosis of diseases of the chest. Philadel-phia
:WB Saunders, 1991 : 2794-2920
[18] Frija J. Tumeur du médiastin. In : Grenier P éd. Pathologie
thoracique de l’adulte. Paris : Flammarion Médecine-
Science, 1988 : 463-478
[19] Frija J, Laval-JeantetM.Techniques et résultatsnormauxde
l’exploration tomodensitométrique du médiastin. Encycl
Méd Chir (Éditions Scientifiques et Médicales Elsevie SAS,
Paris), Radiodiagnostic – Coeur-poumon, 32-535-A-10,
1985 : 1-8
[20] Fulcher AS, Proto AV, Jolles H. Cystic teratoma of the medi-astinum:
demonstration of fat/fluid level. AJRAmJ Roentge-nol
1990 ; 154 : 259-260
[21] Fumikazu S, Shusuke S, Kunihiro K, Atsunori M, Hitoshi U,
Jun A et al. Intrathoracic neurogenic tumors: MR-patho-logic
correlation. AJRAmJ Roentgenol 1992 ; 159 : 279-283
[22] Gamsu G, Sostman D. Magnetic resonance imaging of the
thorax. Am Rev Respir Dis 1989 ; 139 : 254-274
[23] Gamsu G, Stark DD, Webb WR, Moore EH, Sheldon PE.
Magnetic resonance imaging of benign mediastinal
masses. Radiology 1984 ; 151 : 709-713
[24] Gefter WB. Chest applications of MRI: an up date. Radiol
Clin North Am 1988 ; 26 : 573-588
[25] Glazer HS, Lee JKT, LevittRG,Heiken JS, Ling D, TottyWGet
al . Radiation fibrosis: differentiation from recurrent tumor
by MR imaging. Radiology 1985 ; 156 : 721-726
[26] GlazerHS,MolinaPL, SiegelMJ,Sagel SS. High-attenuation
mediastinal masses on unenhanced CT. AJR Am J Roentge-nol
1991 ; 156 : 45-50
[27] Hammon-Kerautret M, Wattinne L, Deffontaines C, Remy-
Jardin M, Remy J. Sémiologie tomodensitométrique des
masses médiastinales. Feuillets Radiol 1992 ; 32 : 1-32
[28] Heitzman ER. The mediastinum: radiologic correlations
with anatomy and pathology. Berlin : Springer Verlag,
1988 : 45-309
A. Coupe coronale pondérée T1 : volumineuse masse pa-ravertébrale
de signal intermédiaire avec quelques élé-ments
hypo-intenses curvilignes.
B. Coupe coronale pondérée T2 : masse hétérogène en
partie hyperintense (astérisque). Les plages nodulaires
et bandes hypo-intenses curvilignes sont dues à la
présence des fibres de collagène (tête de flèche).
[29] HeitzmanER,LaneEJ,HammackDB,RimmlerLJ. Radiologi-cal
evaluation of the aortic-pulmonic window. Radiology
1975 ; 115 : 513-518
[30] Hutin JF. IRM des tumeurs primitives du médiastin. À
proposde41observations. [thèse], UniversitédeBordeaux
II, 1989 : 1-194
[31] Jolles PJ, Shin MS, Jones WP. Aorto-pulmonary window
lesions detection with chest radiography. Radiology 1986 ;
159 : 647-651
[32] Keats TE. The aortic-pulmonary mediastinal stripe. AJRAmJ
Roentgenol 1972 ; 116 : 107-109
[33] Khulman JE, Fishman EK, Wang KP, Zerhouni EA, Stanley
SS. Mediastinal cysts: diagnosis by CT and needle aspira-tion.
AJR Am J Roentgenol 1988 ; 150 : 75-78
[34] Kim HC, Nosher J, Haas A, Sweeney W, Lewis R. Cystic
degeneration of thymic Hodgkin’s disease following radia-tion
therapy. Cancer 1985 ; 55 : 354-356
[35] Lacombe P, Chatel A, Latouche D, Bigot JM, Helenon CH.
La région aortico-pulmonaire : anatomie et anatomie
radiologique normale et pathologie. Ann Radiol1979 ; 22 :
619-633
[36] Lebas JF, Rose Pittet L, Brambilla E, Sarrazin R, Coulomb M.
IRM et tumeurs du médiastin. Confrontation avec la TDM.
J Radiol 1987 ; 68 : 81-88
[37] Lee JK, Glazer HS. Controversy in the MR Imaging appea-rance
of fibrosis. Radiology 1990 ; 177 : 21-22
[38] Lemaitre L,RemyJ, Saint-Michel J.Massesetpseudomasses
médiastinales en tomodensitométrie du thorax. Paris :
Vigot, 1987 : 47-87
[39] Levitt RG, Husband JE, Glazer HS. CT of primary germ-cell
tumors of the mediastinum. AJR Am J Roentgenol 1984 ;
142 : 73-78
[40] Lupetin AR, Dash N. MRI appearance of esophageal dupli-cation
cyst. Gastrointest Radiol 1987 ; 12 : 7-9
[41] MacLoud T, Wittenberg J, Ferrucci JT. Computed tomog-raphy
of the thorax and standard radiographic evaluation
of the chest: a comparative study. J Comput Assist Tomogr
1979 ; 3 : 170-180
[42] Mancuso L, Pitrolo F, Bondi F, Jacoma MA, Margins S,
Marchi S et al. Echocardiographic recognition of mediasti-nal
masses. Chest 1988 ; 93 : 144-148
*A
*B
18](https://image.slidesharecdn.com/syndromemdiastinal-141209093856-conversion-gate02/85/Syndrome-mediastinal-18-320.jpg)
![Radiodiagnostic Syndrome médiastinal 32-360-P-10
[43] Mendelson DS, Rose JS, Efremidis SD, Kirschner PA, Cohen
BA. Bronchogenic cysts with high CT numbers. AJR Am J
Roentgenol 1983 ; 140 : 463-465
[44] Moeller KH, Rosado-De-Christenson ML, Templeton PA.
Mediastinal mature teratoma: imaging features. AJR Am J
Roentgenol 1997 ; 169 : 985-990
[45] Nakata AH, Nakayama C, Kimoto T et al. CT of mediastinal
bronchogenic cyst. J Comput Assist Tomogr 1982 ; 6 :
733-738
[46] Negendank WG, Al Katib AM, Karanes C, Smith M. Lym-phomas:
MR Imaging contrast characteristics with clinical
pathologic correlations. Radiology 1990 ; 177 : 209-216
[47] Owens GR, Arger PH, Mulhern CB, Coleman BG, Gohel V.
Mediastinal pseudo cyst. J Comput Assist Tomogr 1980 ; 4 :
256-259
[48] Pilla TJ, Wolverson MK, Sundaram M, Heiberg E, Shields JB.
CT evaluation of cystic lymphangioma of the mediasti-num.
Radiology 1982 ; 144 : 841-842
[49] Reed JC. Chest radiology: plain film patterns and differen-tial
diagnoses. St Louis : Mosby Year Book, 1991
[50] Remy J. Les lignes du médiastin sur l’incidence thoracique
de face. Société française de Radiologie. Cours de perfec-tionnement
post-universitaire. Paris, 1978
[51] Remy J, Capdeville R, Coussement A. Le poumon patholo-gique.
Paris : Coussement édition, 1983
[52] Rosado-De-Christenson ML, Purgatch RD, Moran CA,
Galobardes J.Thymolipoma:analysis of27cases. Radiology
1994 ; 193 : 121-126
[53] Roubidoux MA. MR Imaging of hemorrhage and iron
deposition in the kidney. Radiographics 1994 ; 14 :
1033-1044
[54] Scatarige JL, Fishman EK, Xuhadja FD, Taylor GA, Siegel-man
S. Low attenuation nodal metastases in testicular car-cinoma.
J Comput Assist Tomogr 1983 ; 7 : 682-687
[55] Seline TH, Gross BH, Francis IR. CT and MR imaging of
mediastinal hemangiomas. J Comput Assist Tomogr 1990 ;
14 : 766-768
[56] Senac JP, Giron J. Sémiologie et classification radioclinique
des masses du médiastin. In : Tomographie thoracique.
Montpellier : Axone, 1986 : 112-175
[57] SonesPJ, TorresWE,Colvin RS,MeierWL,Sprawls P,Rogers
JV. Effectiveness of CT in evaluation intrathoracic masses.
AJR Am J Roentgenol 1982 ; 139 : 469-475
[58] Stephen JS, Keller PL, Berquist TH, Mcleod RA, Stephens
DH. Magnetic resonance imaging of hemorrhage. AJRAmJ
Roentgenol 1985 ; 145 : 921-927
[59] Vasile N. Tomodensitométrie corps entier. Paris : Vigot,
1985
[60] Vix VA, Klatte EC. The lateral chest radiograph in the diag-nosis
of hilar and mediastinal masses. Radiology1970 ; 96 :
307-316
[61] VonSchulthess GK,McMurdoK, Tscholakoff D,DeGeer G,
Gamsu G, Higgins CB. Mediastinal mases: MR imaging.
Radiology 1986 ; 158 : 289-296
[62] Weinreb JC, Naidich DP. Thoracic magnetic resonance
imaging. Clin Chest Med 1991 ; 12 : 33-54
[63] Wernecke K, Potter R, Peters PE, Koh P. Parasternal medias-tinal
sonography: sensitivity in the detection of anterior
mediastinal and subcarinal tumors. AJR Am J Roentgenol
1988 ; 150 : 1021-1026
[64] Wernecke K, Vassalo P, Potter R, Luckener HG, Peters PE.
Mediastinal tumors: sensitivity of detection with sonogra-phy
compared with CT and radiography. Radiology 1990 ;
175 : 137-143
[65] Whalen JP, Meyers MA, Oliphant M, Caragol WJ, Evans JA.
The retrosternal line. A new sign of an anterior mediastinal
mass. AJR Am J Roentgenol 1973 ; 117 : 861-872
[66] Woodring JH, Johnson PJ. Computed tomography distinc-tion
of central thoracic masses. J Thorac Imaging 1991 ; 6 :
32-39
[67] Yernault JC, Kuhn G, Dumortier P, Rocmans P, Ketelbant P,
de Vuyst P. “Solid” mediastinal bronchogenic cyst: mine-ralogic
analysis. AJR Am J Roentgenol 1986 ; 146 : 73-74
19](https://image.slidesharecdn.com/syndromemdiastinal-141209093856-conversion-gate02/85/Syndrome-mediastinal-19-320.jpg)