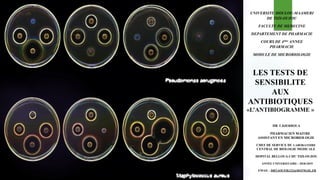
Les tests de sensibilite aux antibiotiques / Antimicrobial susceptibility testing
- 1. UNIVERSITE MOULOU-MAAMERI DE TIZI-OUZOU FACULTE DE MEDECINE DEPARTEMENT DE PHARMACIE COURS DE 4ème ANNEE PHARMACIE MODULE DE MICROBIOLOGIE LES TESTS DE SENSIBILITE AUX ANTIBIOTIQUES «L’ANTIBIOGRAMME » DR T.DJERBOUA PHARMACIEN MAITRE ASSISTANT EN MICROBIOLOGIE CHEF DE SERVICE DU LABORATOIRE CENTRAL DE BIOLOGIE MEDICALE HOPITAL BELLOUA-CHU TIZI-OUZOU ANNÉE UNIVERSITAIRE : 2018-2019 EMAIL : DRTAOUFIK123@HOTMAIL.FR
- 2. PLAN INTRODUCTION ET DEFINITIONS OBJECTIFS DES TESTS DE SENSIBILITE AUX ANTIBIOTIQUES (TSA) MATERIEL ET METHODES DES TESTS DE SENSIBILITE AUX ANTIBIOTIQUES : A) Standardisation de l’antibiogramme : CLSI / EUCAST /AARN et autres organismes de standardisation B) MILIEUX DE TESTS DE SENSIBILITE AUX ANTIBIOTIQUES C) Méthodes de l’antibiogramme C.1) Méthodes qualitatives La diffusion en milieu gélosé C.2) Méthodes quantitatives : Détermination de la concentration minimale inhibitrice Détermination de la concentration minimale bactéricide Evaluation de l’activité de l’association des antibiotiques Détermination du pouvoir bactéricide du sérum et dosage des antibiotique Tests complémentaires de sensibilité aux antibiotiques : recherche des mécanismes de résistance aux antibiotiques Interprétation des tests de sensibilité aux antibiotiques Contrôle qualité de l’antibiogramme Avantages et limites des tests in vitro de sensibilité aux antibiotiques conclusion
- 3. OBJECTIFS PEDAGOGIQUES Décrire les principaux objectifs derrière la pratique de l’antibiogramme Décrire le matériel utilisé et les principales approches techniques de l’antibiogramme Décrire la place de l’antibiogramme dans la décision thérapeutique Décrire le principe et l’intérêt de la standardisation de l’antibiogramme et des controles de qualité
- 4. INTRODUCTION Les antibiotiques (dont les antibactériens) constituent une classe thérapeutique distincte dans le sens ou elle sont destinés a agir sur des cellules ou des organismes vivants ce développant au détriment d’un autre organisme vivant (hôte) Ainsi, les enjeux actuels de l’antibiothérapie antibactérienne sont nombreux : Pouvoir éliminer le/les bactéries causant l’infection Altérer au minimum l’équilibre du microbiote normal Avoir un minimum d’effets indésirables chez l’hote Prévenir l’émergence et la diffusion des bactéries résistances aux antibiotiques Comme tout organisme vivant, les bactéries sont capables de s’adapter a leurs environnement et de développer des stratégies de défense en cas d’agressions extérieures
- 5. OBJECTIFS DES TESTS DE SENSIBILITE AUX ANTIBIOTIQUES L’antibiogramme est un ensemble de technique explorant l’interaction entre la bactérie et les antibactériens , ces tests sont largement utilisés en médecine humaine et animale mais aussi dans de nombreux autres domaines comme l’industrie pharmaceutique En médecine humaine, ces tests ont comme objectifs de: Déterminer l’effet de la présence d’un ou plusieurs antibiotiques sur le comportement d’une bactérie Orienter le choix thérapeutique en adaptant la prescription médicale aux donnés microbiologiques et cliniques Prédire l’impact de l’antibiothérapie sur l’évolution de l’infection Adapter les posologies des antibiotiques a index thérapeutique étroit Dépister / surveiller l’évolution de la résistance acquise aux antibiotiques CES TECHNIQUES SONT PARFOIS APPLIQUES POUR LES TESTS DE SENSIBILITE A D’AUTRES SUBSTANCES COMME LES ANTISEPTIQUES, LES D2SINFECTANTS ET LES HUILES ESSENTIELLES
- 6. MATERIELS ET METHODES APPLIQUEES AUX TESTS DE SENSIBILITE AUX ANTIBIOTIQUES LA STANDARDISATION DES TESTS DE SENSIBILITE AUX ANTIBIOTIQUES
- 7. La standardisation de l’antibiogramme STANDARDISATION, subst, fem [Corresp. à standardiser ] Action de rendre une production conforme à certaines normes de référence; production en série de modèles standard. Synon. normalisation « soumission à un modèle, un type, une mesure ou une valeur standard » Comme tout domaine impliquant « des mesures » et des « protocoles techniques d’analyse», la microbiologie est soumise a des normes et a des contrôles de qualité qui permet de s’assurer de l’exactitude et de l’interprétabilité des résultats en diminuant les erreurs et les anomalies analytiques En plus des normes d’assurance qualité appliquée a la biologie médicale, l’antibiogramme, est soumis a des standards nationaux et internationaux strictes émis par des sociétés savantes spécialisés dans le domaine des antimicrobiens. Des normes sont continuellement réévalués et améliorés puis publiés périodiquement pour mettre a jour les pratiques des laboratoires de microbiologie
- 8. La standardisation de l’antibiogramme La normalisation de l’antibiogramme permet de garantir : -Une harmonisation des pratiques de l’antibiogramme entre les laboratoires de microbiologie -La reproductibilité des résultats -La facilité de l’interpretation des résultats lors de la confrontation clinico-biologique De plus , grâce aux contrôles qualité impératifs a la validité des antibiogrammes, la standardisation permet de : -Préciser la fiabilité de la technique utilisée -évaluer la performance des réactifs utilisé -évaluer l’implication et les performances du facteur humain NB : chaque document publié comporte des protocoles analytiques et des modes opératoires ainsi que des tables d’interpretation des résultats des tests et des controles de qualité, tout faille rend l’antibiogramme ininterpretable
- 9. La standardisation de l’antibiogramme Les principaux organismes experts dans ce domaine sont : 1) Le CLSI : institution américaine active depuis 50 ans activant dans le domaine de l’amélioration des laboratoires cliniques et industriels sous leurs apects qualité, efficacité et sécurité. Le CLSI publie périodiquement des recommandations , celui s’adressant a l’antibiogramme est dit « M100 : Performance Standards for Antimicrobial Susceptibility Testing »
- 10. La standardisation de l’antibiogramme Les principaux organismes experts dans ce domaine sont : 2) L’EUCAST : actif depuis 1997, il est conjointement organisé par l’ESCMID et l’E-CDC ainsi qu’avec la collaboration de plusieurs acteurs européens. l’EUCAST est l’organe européen spécialisé dans la détermination des valeurs d’interpretation des l’antibiogramme ainsi que des aspects techniques des tests in vitro de sensibilité aux antibiotiques. NB : il existe plusieurs autres organies nationaux et internationaux de standardisation comme la CA-SFM (France), la BSAC (Angleterre) , JAID/JSC (Japon)…
- 11. La standardisation de l’antibiogramme Les principaux organismes experts dans ce domaine sont : 3) L’AARN (Algerian Antimicrobial Resistance Network) : répertorié en 2001 et financé jusqu’en 2013 par l’OMS , l’AARN a plusieurs missions : • Promouvoir l’inter-connexion des laboratoires nationaux dans la surveillance de la résistance aux antibiotiques • Assurer le contrôle de qualité externe et interne du processus de surveillance de la résistance aux antibiotiques • Renforcer le système national de veille épidémiologique et d’alerte rapide • Recueillir les données épidémiologiques et en assurer l’exploitation, l’analyse et la diffusion des résultats • Améliorer la formation du personnel du réseau des laboratoires nationaux depuis 2014, ce réseau, bien que placé officiellement sous l'autorité de la direction de la prévention ne reçoit aucune subvention, par conséquent, toutes les activités sont uniquement hébergées au niveau de leurs page web :http://www.sante.dz/aarn
- 12. La standardisation de l’antibiogramme AU TOTAL ! Les recommandations portés par les différents manuels de standardisation permettent de répandre aux questions suivantes : 1. Quel technique est la plus adaptée au germe isolé ? 2. Quels antimicrobiens et a quelles concentrations sont a tester pour le germe isolé ? 3. Quel milieu de culture a utilisé pour le germe isolé ? 4. Quelles modalités techniques a appliquer pour le test ? (concentration en cellules bactériennes, concentrations du/des antibiotiques, diluants, solvants … 5. Quand , comment et pour qui réaliser des complémentaires de sensibilité aux antibiotiques ? 6. Comment interpréter les résultats des tests de sensibilité aux antimicrobiens ? 7. Quelles réponses communiquer au clinicien ? 8. Technique, souches bactériennes, périodicité et interprétation des contrôles de qualité
- 13. MATERIELS UTILISE DANS LES TESTS DE SENSIBILITE AUX ANTIBIOTIQUES
- 14. Les tests de sensibilité aux antibiotiques font appelle a : 1) Milieux de culture adapté aux tests de sensibilité aux antibiotiques : Ce sont des supports de culture dont la composition est minutieusement déterminée et contrôlée et dont l’interaction avec les antibiotique est connue en particulier en matière de diffusion, ceci permet d’éliminer toute interférence risquant de donner de faux résultats. Le milieu le plus utilisé est le Muller Hinton sous forme liquide ou gélosée (solide) En plus du matériel usuel stérile d’ensemmencement et de préparation des échantillons (boites de Petri, anses de platine, pipettes pasteur, poires, tubes stériles…) Il est a noter que : Pour les germes exigeants en facteurs de croissance, le Muller Hinton peut etre additionnée de sang de Mouton Dans certains cas, les tests de sensibilité aux antibiotiques sont validés sur d’autres milieux de culture comme la GC agar pour Neisseria spp ou HTM pour Haemophilus spp GC agarMH au sang
- 15. 2) Matériel pour la préparation des suspensions bactériennes : selon les recommandation internationales, tout les antibiogrammes doivent être préparés a partir d’une culture pure et fraiche (18h de culture sur milieu solide) . la suspension bactérienne (inoculum) doit contenir un nombre bien déterminé de bactéries, le nombre le plus retrouvé est de 1,5X108 cellules /mL . AGITATEUR VORTEX DENSITOMETRE McF GAMME ETALON McF La préparation de la suspension se fait par : -Trituration de quelques colonies bactériennes dans un solvant (Eau distillée ou physiologique le plus souvent) -Mesure de la turbidité de la suspension est faite soit visuellement (Gamme étalon de turbidité) soit automatiquement (densitomètre McFarland (0,5 McF) ou Spectrophotométrie (0,08-1 a 625 nm) 0,5 McF = 0,08-1 a 625 nm= 1,5X108 cellules /mL SPECTROPHOTOMETRE DE PAILLASSE
- 16. 3) Les antibactériens : Les molécules utilisés pour les TSA sont sous diverses formes selon la technique envisagée, sur chaque support nous pouvons trouver une ou plusieurs molécules 3.1) Les disques d’antibiotiques : ce sont des disques de papier imprégné d’une concentration déterminée d’antibiotique. Disques d’antibiotiques avec système de dépôt et de stockage Disques d’antibiotique (étui contenant 04 cartouches contenant chacune 50 disques d’antibiotique)
- 17. 3) Les antibactériens : Les molécules utilisés pour les TSA sont sous diverses formes selon la technique envisagée : 3.2) Les Bandelettes: ce sont des supports imprégnées d’un gradient de concentration de l’antibiotique 3.3) Les poudre titrés : permettent de préparer la concentration / gamme de concentrations désirée qui seront par la suite incorporés aux milieux de culture, déposés en spots ou sur disque de papier
- 18. METHODES UTILISE DANS LES TESTS DE SENSIBILITE AUX ANTIBIOTIQUES 1) Les techniques d’ensemencement et de dépôt des antibiotiques 2) Les méthodes qualitatives : diffusion en milieu gélosé 3) Les méthodes quantitatives : détermination des concentrations minimales inhibitrices et bactéricides 4) Autres approches de tests de sensibilité aux antibiotiques
- 19. 4,1 ) Les techniques d’ensemmencement : L’objectif de l’ensemencement est d’obtenir une concentration fixe et homogène de cellules bactériennes en contact avec l’antibiotique permettant ainsi de tester son effet , a différentes doses sur une même quantité de bactéries. • Pour les milieux liquides, l’ensemencement est réalisé par transfert d’un volume de la suspension bactérienne au milieu de culture liquide • Pour les milieux solides, l’ensemencement est fait selon l’approche désirée par : La technique Kirby-Bauer (CLSI) : consiste a imbiber un écouvillon dans la suspension bactérienne et d’ensemencer le milieux de culture de haut en bas avec des stries sérés, cette opération est répétée trois fois en tournant la boite de Pétri de 60° avant de procéder a l’ensemencement. Au bout de 18-24h d’incubation la culture se présente sous forme de colonies très confluentes. Ce type d’ensemencement est rapide mais est imprécis.
- 20. 4,1 ) Les techniques d’ensemmencement (inoculation): La technique par inondation (EUCAST-SFM) : Consiste a inonder la gélose avec un volume précis de la suspension bactérienne , les boites sont ensuite séchés. Technique plus longue mais plus précise.
- 21. 4,1 ) Les techniques d’ensemmencement : Le dépôt en spot : réservée aux CMI, un spot est déposé a l’aide d’un écouvillon ou a l’aide d’un petit volume de la suspension bactérienne directement sur la gélose L’ensemencement en stries : Utilisé lors de la détermination des CMB, il consiste en l’utilisation d’une anse calibrée (10μl) et d’effectuer plusieurs stries , chacune correspondant a une dilution approximative de 1/10 • L’ensemencement automatique : il existe des automates qui peuvent réaliser toutes les étapes et tout les types de tests de sensibilité aux antibiotiques et ce de la préparation des dilutions jusqu’à la lecture de l’antibiogramme
- 24. 4,2 ) Les techniques qualitatives : La diffusion simple en milieu gélosé Méthode des disques d’antibiotiques Principe : il s’agit de mettre un disque d’antibiotique au contacte d’une gélose pré-ensemencée par la souche a tester.
- 25. Exemple du choix des antibiotiques a tester selon la bactérie étudiée : extrait du manuel de standardisation de l’antibiogramme de l’AARN (2016)
- 26. Exemple du choix des milieux de TSA, des inoculum et des conditions d’incubation selon la bactérie étudiée : extrait du manuel de standardisation de l’antibiogramme de l’AARN (2016)
- 27. 4,2 ) Les techniques qualitatives : La diffusion simple en milieu gélosé Méthode des disques d’antibiotiques Principe Dès le moment ou le disque touche la gélose, la charge en molécule(s) antibiotiques qu’il contient diffuse de manière radiale Avec le temps un GRADIENT DE CONCENTRATION s’établit ou la concentration de l’antibiotique est INVERSEMENT PROPORTIONNELLE A LA DISTANCE DU DISQUE. Si l’antibiotique est actif sur la bactérie, au voisinage du disque apparait un diamètre ou aucune culture n’est visible =) DIAMETRE D’INHIBITION Plus l’antibiotique est actif sur la souche testée (bactérie sensible) plus la diamètre d’inhibition est grand. L’inverse est vrai (souche résistante).
- 28. C1 > C2 > C3 > C4 C2 C3 C4 C1 Gradient d’antibiotique décroissant Disque d’antibiotique Diamètre d’inhibition Zone d’inhibition de la culture Colonies
- 30. 4,2 ) Les techniques qualitatives : La diffusion simple en milieu gélosé Méthode des disques d’antibiotiques Lecture: Après 18h a 24h d’incubation dans les conditions recommandés , les diamètres d’inhibition sont mesurés a l’aide d’une règle ou d’un pied a coulisse
- 31. 4,2 ) Les techniques qualitatives : La diffusion simple en milieu gélosé Méthode des disques d’antibiotiques Interprétation: Plus l’antibiotique est actif sur la souche testée (bactérie sensible) plus la diamètre d’inhibition est grand. L’inverse est vrai (souche résistante). Chaque point du diamètre d’inhibition correspond a une concentration en antibiotique Ainsi il existe une corrélation inverse entre le diamètre d’inhibition et la concentration en antibiotique =) Plus le diamètre est élevé (loin du disque), plus la concentration active sur le germe est faible =) Plus le diamètre est faible (proche du disque), plus la concentration nécessaire pour inhiber le germe est grande Il s’agit d’une détermination indirecte de la concentration minimale inhibitrice
- 32. 4,2 ) Les techniques qualitatives : La diffusion simple en milieu gélosé Méthode des disques d’antibiotiques Interprétation: Lors de l’évaluation d’un nouvel antibiotique sur une bactérie, la détermination de son activité passe par le test d’un très grand nombre de souches de chacune des bactéries d’intérèt médical. Chaque souche donnera pour cet antibiotique un diamètre d’inhibition. L’étude statistique de l’ensemble de ces diamètres d’inhibition corrélé aux donnés chimiques, aux propriétés pharmacologique et toxicologique de l’antibiotique donne naissance a des « Seuils » a partir desquels la bactérie est considérée comme « répondante ou non» a l’antibiotique e,n question, ces diamètres sont dits « DIAMETRES CRITIQUES » ou « Breakpoints » exprimé en mm qui sont au nombre de deux -Un diamètre critique supérieur (D) -Un diamètre critique inférieur (d) AU TOTAL : pour chaque bactérie , des break points sont définies par voie expérimentale pour chaque antibiotique utilisé en thérapeutique
- 33. 4,2 ) Les techniques qualitatives : La diffusion simple en milieu gélosé Méthode des disques d’antibiotiques Interprétation: La détermination des Breakpoints a un double intérêt : Ceci a un double intérêt : - Déterminer le spectre d’activité de l’antibiotique = Spectre clinique de l’antibiotique =) espèces sensibles, modérément sensibles, inconstamment sensibles et résistantes (sur quelles bactérie cet antibiotique est actif ?) -Déterminer le degré d’activité d’un antibiotique vis-à-vis d’souche bactérienne faisant partie du spectre clinique de sensibilité de l’antibiotique (est que l’antibiotique est toujours actif sur ce germe ?) SPECTRE CLINIQUE DE L’ERYTHROMYCINE SUR 04 ESPECES BACTERIENNES Catégories cliniques de sensibilité aux antibiotiques chez Neisseria meningitidis isolés en Algérie en 2016 (AARN) NT + non testé
- 34. Espèces résistantes Espèces habituellement sensibles Espèces modérément sensibles Espèces inconstamment sensibles SPECTRE CLINIQUE DE L’ANTIBIOTIQUE CATEGORIE CLINIQUE D’UNE BACTERIE TESTS DE SENSIBILITE AUX ANTIBIOTIQUES SOUCHE SENSIBLE SOUCHE INTERMEDIAIRE SOUCHE RESISTANTE
- 35. 4,2 ) Les techniques qualitatives : La diffusion simple en milieu gélosé Méthode des disques d’antibiotiques Interprétation: Les « DIAMETRES CRITIQUES » permet de catégoriser les souches isolés en 3 catégories cliniques: -Bactéries sensible (S) : dont le diamètre d’inhibition est supérieur ou égale au diamètre critique supérieur, Les souches S sont celles pour lesquelles la probabilité de succès thérapeutique est acceptable. Nous nous attendons à un effet thérapeutique dans le cas d'un traitement à dose habituelle par voie générale -Bactéries résistantes (R): dont le diamètre d’inhibition est inférieur ou égale au diamètre critique inférieur. Les souches R sont celles pour lesquelles il existe une forte probabilité d'échec thérapeutique. Nous ne pouvons pas nous attendre à un effet thérapeutique quel que soit le traitement. Les souches de sensibilité intermédiaire ou sensibilité dose dépendante (I): dont le diamètre d’inhibition est situé entre les deux bornes. Les souches I sont celles pour lesquelles le succès thérapeutique est imprévisible. Elles forment un ensemble hétérogène pour lequel la seule valeur de la CMI n'est pas prédictive (zone d’incertitude).
- 36. 4,3 ) Les techniques quantitatives (1): Détermination de la concentration minimale inhibitrice Définition: il s’agit de la concentration en antibactérien qui provoque un arrêt de la multiplication bactérienne La définition exacte est adaptée a chaque technique utilisée pour la détermination de la CMI (observation macroscopique) Principe: Mettre une souche bactérienne en culture avec un gamme de dilution d’un antibiotique donnée et d’en observer les effet. Technique : 4,3,1) CMI par dilution en milieu liquide : la CMI correspond a la concentration pour laquelle aucune culture n’est visible Cette technique, précise mais lourde ne permet d’étudier la CMI que d’un isolat bactérien a la fois Adapté aux tests individuels Il existe une variante miniaturisée : la micro-dilution en milieu liquide Les CMI en milieu liquide est adaptée a une grande variété d’antibiotiques et permet par extension la détermination de la CMB
- 38. 4,3 ) Les techniques quantitatives (1): Détermination de la concentration minimale inhibitrice 4,3,1) CMI sur milieu solide : il existe deux principales méthodes : A) La dilution en milieu gélosé: consiste a préparer une gamme de dilution de l’antibiotique et de l’incorporer dans plusieurs boites de Pétri. L’inoculation ce fait sous forme de spotes Adaptée aux grandes séries B) Méthodes des bandelettes d’antibiotiques (E-Test): consiste a utiliser des bandelettes imprégnés d’une gamme de concentration de l’antibiotique Si l’antibiotique est actif, la bactérie ne cultivera qu’a voisinage des concentrations tolérés par celle-ci, le point de contact entre la culture bactérienne et la bandelette constitue la CMI Les méthodes en milieu gélosé sont Méthode simple, rapide (E-test) adaptés aux petites et grandes séries avec une bonne sensibilité/spécificité mais posent parfois des problèmes d’interpretation
- 40. 4,3 ) Les techniques quantitatives (1): Détermination de la concentration minimale inhibitrice Interprétation: comme pour la diffusion , l’interpretation est basée sur les CMI critiques de catégorisation clinique. En revanche, ces techniques rendent la concentration exacte au clinicien
- 41. Problèmes de lecture rencontrés avec les E-test
- 42. 4,4 ) Les techniques quantitatives (2): Détermination de la concentration minimale bactéricide Définition: il s’agit de la concentration en antibactérien qui provoque la mort de 99,99% de l’inoculum (soit ne laisse que 0,01% de survivants. La cinétique de bactéricide consiste a observer la rapidité avec laquelle ce phénomène a lieu. Principe et technique : il s’agit de mettre en culture tout les tubes / puits a partir de la CMI , sur un milieu gélosé stérile , et de compter dans chacun des tubes/puits de CMI le nombre de bactéries survivantes
- 43. La CMB corrélée a la CMI permet de déterminer si l’antibiotique est bactériostatique ou bactéricide Exemples : Antibiotiques bactériostatiques CMB éloignée des CMI : CMB > 32 x CMI les macrolides, tétracyclines, rifamycines, sulfamides Antibiotiques bactéricides : CMB proches des CMI : CMB < 32 x CMI aminosides - β-lactamines - quinolones - glycopeptides
- 44. 4,5 ) Autres tests de sensibilité aux antibiotiques: Dépistage et confirmation des résistances aux antibiotiques: La résistance aux antibiotiques peut etre due a l’expression par la bactérie d’un ou plusieurs mécanismes de résistance Cette résistance peut etre patente (résistance totale a de hautes concentrations d’antibiotique) mais peut parfois etre exprimée de manière plus timide avec des conséquences variables allant de la nécessité d’augmentation de doses jusqu’à l’echec thérapeutique La recherche des mécanismes de résistance est de pratique courante au laboratoire , elle peut se faire en parallèle avec l’antibiogramme ou sur géloses chromogènes (détermination phénotypique) mais peut parfois nécessiter la recherche directe des gènes de résistance (méthodes génotypiques). Pour certaines bactéries, en particulier présentant un risque vital accru ou un risque épidémique important, la détermination peut être effectué par techniques rapides (agglutination, chromatographie) ou génotypique Entérobactérie productrice d’une BLSE Détection des souches MRSA par agglutination Bacilles a Gram négatif produisant une Carbapenemase sur milieu chromogène L’érythomycine induisant une résistance A la clindamycine chez S.aureus
- 45. Methodes genotypiques Recherche des gènes mutants par hybridation in Situ Recherche des gènes mutants par Multiplex Q-PCR
- 46. 4,5 ) Autres tests de sensibilité aux antibiotiques: Etudes des associations d’antibiotiques : praticable sur deux ou plusieurs antibiotiques, ces techniques regroupent les mêmes approches employés pour la détermination de la CMI et de la CMB. Cette détermination regroupe : -L’étude de l’éffet (Temps/concentration) de chacun des antibiotiques a tester -L’étude de l’éffet de l’association a diverses concentrations de l’une ou l’autre de l’antbiotique puis sa catégorisation de son effet en : -Bactériostatique -Bactéricide ---) bactéricidie rapide / bactéricidie lente -Synergie / indifférence / addition / antagonisme Détérmination de l’activité d’un liquide biologique et dosage des antibiotiques: necessaire pour éviter tout accident lié au sous dosage (échecs) ou surdosage (toxicité) de certains antibiotiques ainsi que devant certaines pathologies difficiles a traiter . le dosage peut se faire par plusieurs méthodes dont les microbiologiques, immunologiques ou chromatographique. Etudes des associations d’antibiotiques
- 47. 4,6 ) INTERPRETATION DES TESTS DE SENSIBILITE AUX ANTIBIOTIQUES Elle revête deux principaux volets : la catégorisation clinique de la bactérie et l’effet de(s) antibiotiques sur la bactérie 4,6,1) la catégorisation clinique de la bactérie: L’interpretation des tests qualitatifs et quantitatifs est donnée par les différents standards. Elle nécessite parfois le recours a des tests complémentaires phénotypiques et génotypiques. Dans ce sens la communication clinicien microbiologiste est primordiale En plus de permettre l’initiation d’une antibiothérapie en cas d’indication , les TSA permettent de l’adapter au contexte clinique. La découverte de certains mécanismes de résistance peut entrainer des mesures de vigilance supplémentaires autour du patient pour éviter la propagation des gènes de résistance.
- 48. Antibiotiques temps dépendants : Plus la bactérie est exposée de manière durable plus l’effet antibactérien est prononcé Ex: β-lactamines, les glycopeptides Cette observation est à la base du mode d'administration proposé doses fractionnées, en continu pour les ATB temps dépendants Antibiotiques concentration dependent : Plus la dose administrée est élevée , plus l’effet bactéricide est intense et rapide. Ex :les amino sides, les fluoroquinolones L'obtention in vivo de concentration élevée semble déterminante Cette observation est à la base du mode d'administration proposé dose journalière pour les ATB concentration dépendants 4,6.2 ) Détérmination de l’effet de(s) antibiotiques sur la bactérie
- 49. 5 ) CONTRÔLE DE QUALITE DE L’ANTIBIOGRAMME Pour assurer la qualité et la fiabilité des résultats, les TSA sont soumis a des contrôles périodiques de qualité qui en analyse tout les aspects : -Milieux de culture -Antibiotiques -Environnement d’incubation -compétences du personnel … La périodicité et les modalités d’execution et d’interpretation des CQ des TSA sont rapportés dans les differents standards Un des aspects particulier des CQ étant l’utilisation de « BACTERIES INDICATRICES » qui sont des bactéries très bien caractérisées sur les plans phénotypiques et génotypiques, les plus utilisés sont issues de ‘AMERICAN TYPE CULTURE COLLECTION ou ATCC. Plusieurs sont utilisés selon le besoin ex : Escherichia coli ATCC 25922-Staphylococcus aureus ATCC 25923-Pseudomonas aeruginosa 27853 pour le contrôle de routine de la qualité des milieux de culture , des antibiotiques et des pratiques Staphylococcus aureus ATCC 43300 comme marqueur de la résistance aux β-lactamines Klebsiella pneumoniae ATCC BAA-1706 comme exemple de production d’une enzyme détruisant les β-lactamines Outre leurs utilisation dans ce contexte , ces bactéries sont le fondement des CQ de microbiologie et sont équivalents aux étalons en chimie.
- 50. 6 ) LIMITES DES TSA: • Limites techniques La réalisation d'un antibiogramme est soumise au respect de conditions techniques qui sont parfois incomplètement et insuffisamment respectées. les techniques de l'antibiogramme ont été standardisées uniquement pour les bactéries cultivant rapidement sur milieux usuels , elle ne sont pas applicables aux bactéries a culture très lente ou intracellulaires obligatoires (méthodes spécifiques) Certain anibiotiques sont très difficiles a évaluer en raison de leurs propriétés physicochimiques ou du type d’intéraction avec la bactérie comme les polymixines, les glycopeptides ou la fosfomycine Limites dans l'interprétation des résultats Incertitude sur l'étiologie de l'infection L'antibiogramme ne peut apporter une aide que dans la mesure où il est effectué sur la bactérie véritablement responsable de l'infection (Infection documentée). Absence de parallélisme entre les situations in vitro et in vivo. L'antibiogramme ne peut prédire le comportement d'un antibiotique in vivo. Celui-ci est fonction de multiples facteurs : -dose administrée et diffusion au site de l'infection ; -Pénétration intracellulaire (cas d’infection a bactérie intracellulaire obligatoire - Influence des facteurs physiologiques ou pathologiques sur la pharmacocinétique de l'antibiotique ; - Transformation de la molécule in vivo ; - Etat physiologique de la bactérie au sein du foyer infectieux - Émergence d'une résistance au cours du traitement Pour cela les standards et les techniques de TSA sont en constante évolution
- 51. 7 ) Conclusion et a retenir ! • En médecine, les tests de sensibilité aux antibiotiques ont pour finalité d’adapter au mieux la thérapeutique antibactérienne • Leurs execution, interpretation et controles sont soumis a des standards internationaux de qualité garantissant leurs fiabilité • Il existe plusieurs techniques adaptés au terrain, les investigation actuelles de développement des TSA se penchent sur les micro méthodes, les techniques rapides et les méthodes génotypiques. • Le test de diffusion de disque en milieu solide est le plus utilisé en routine • La pratique des CMI est surtout limitée par l’accés aux réactifs • La détérmination des CMB est reservée aux nouvelles molécules mais aussi est pratiquée dans des contextes particuliers (associations) • La determination de l’activité des associations d’antibiotiques, du pouvoir bactéricide des liquides biologiques ainsi que le dosage des antibiotique est effectué sur demande du clinicien mais necesssite la sensibilisation de ceux-ci • La recherche des mécanismes de résistance est délicate en particulier si le mécanisme est peu exprimé, le manque d’accés aux techniques génotypiques rend la tache plus difficile • Les controles de qualité périodiques garantissent aussi bien au prestataire qu’au bénéficiaire l’assurance d’une analyse de qualité • • Les TSA ont leurs limites , pour cela les techniques et les standards sont en constante révision